Clear Sky Science · pt
O complemento intracelular Fator H promove a progressão tumoral por meio da modulação do ciclo celular e do citoesqueleto de actina
Por que esse ajudante oculto do câncer importa
O câncer costuma ser descrito como uma batalha entre tumores em crescimento e o sistema imunológico. Este estudo revela que uma das próprias moléculas do sistema imune, uma proteína chamada Fator H, pode silenciosamente mudar de lado. Em vez de atuar apenas na corrente sanguínea para controlar a inflamação, o Fator H é encontrado dentro das células tumorais e nas células de suporte próximas, onde ajuda os cânceres a crescer, sobreviver e potencialmente se disseminar. Compreender essa “dupla vida” inesperada abre novas formas de prever quão agressivo será um tumor e de projetar terapias mais inteligentes.
Uma proteína conhecida em um lugar inesperado
O Fator H é mais conhecido como guardião do sistema complemento, uma parte da imunidade inata que ajuda a eliminar micróbios e células danificadas do sangue. Níveis elevados de Fator H ao redor de tumores já haviam sido associados a prognósticos piores em vários cânceres, incluindo o câncer renal de células claras. Ainda assim, seu papel padrão, na corrente sanguínea, não explicou completamente por que pacientes cujos tumores superproduzem Fator H tendem a ter desfechos ruins. Ao combinar dados de pacientes, sequenciamento de célula única e biologia celular, os autores mostram que muitas células dentro de tumores renais — especialmente fibroblastos associados ao câncer e células renais malignas — produzem ativamente seu próprio Fator H e retêm uma porção dele dentro da célula em vez de secretá‑lo.
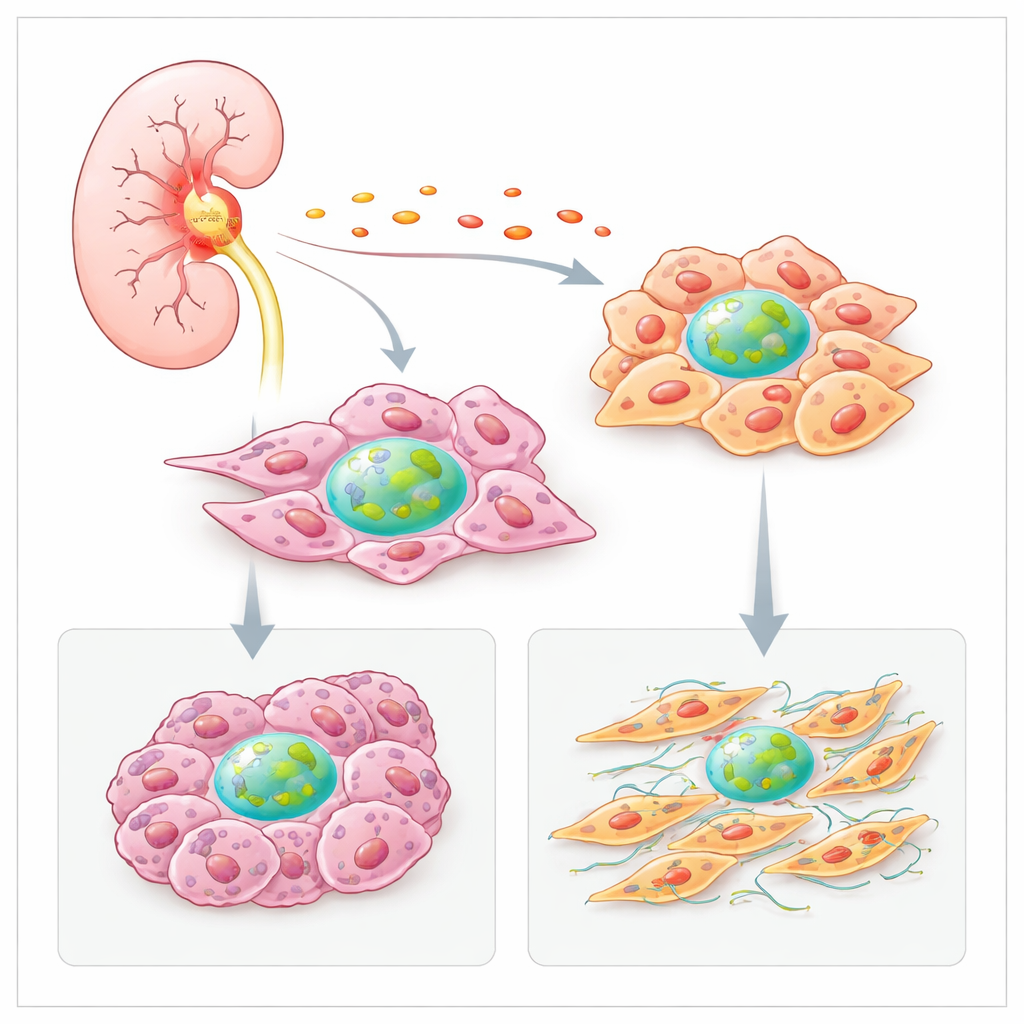
A inflamação aumenta a produção de Fator H
A equipe primeiro perguntou por que tumores produzem mais Fator H do que tecido renal saudável. Eles analisaram grandes conjuntos de dados de câncer e mapas espaciais de fatias tumorais e descobriram que áreas ricas em fibroblastos e células cancerosas também continham altos níveis do gene do Fator H. Essas áreas frequentemente se sobrepunham a assinaturas de moléculas inflamatórias, como a citocina IL‑6. Em células cancerígenas renais cultivadas, a IL‑6 aumentou fortemente a produção de Fator H, enquanto outros sinais inflamatórios a elevaram nos fibroblastos. Isso sugere que o próprio ambiente tumoral inflamado estimula as células locais a aumentar seu Fator H, reforçando um círculo vicioso de crescimento e sobrevivência.
No núcleo, ajudando as células a ignorar sinais de parada
Ao olhar dentro das células, os pesquisadores descobriram uma forma menor, intracelular do Fator H que aparece em vários compartimentos, incluindo o núcleo. Lá, ela interage fisicamente com controladores-chave do ciclo celular, particularmente um fator de transcrição chamado E2F3, que ajuda a impulsionar as células do estado de repouso para o de divisão. Quando o gene do Fator H foi silenciado, fibroblastos e células cancerosas reduziram sua replicação, acumularam‑se na fase de repouso e mostraram p53 mais ativo, uma proteína “guardião” conhecida que pode interromper o crescimento ou desencadear a morte celular. Importante: simplesmente adicionar Fator H secretado externamente não restaurou esse efeito, ressaltando que o reservatório interno é o que mantém o p53 sob controle e permite a proliferação contínua.
Remodelando o esqueleto celular para crescimento e movimento
Em células de câncer renal, mas não em fibroblastos, o Fator H intracelular também se ligou a componentes do complexo de captação de actina, que regula como os filamentos de actina crescem e estabilizam a estrutura interna da célula. Quando o Fator H foi silenciado, as células cancerosas ficaram mais arredondadas, perderam suas fibras de tensão organizadas e tiveram dificuldade para formar esferoides tridimensionais compactos — um substituto experimental para o crescimento e a coesão tumoral. Silenciar tanto o Fator H quanto a proteína de captação não agravou os defeitos, sugerindo que atuam na mesma via. Essas alterações ocorreram mesmo quando o p53 foi bloqueado, indicando que o Fator H apoia de forma independente tanto a divisão celular quanto as mudanças estruturais que podem favorecer invasão e metástase.
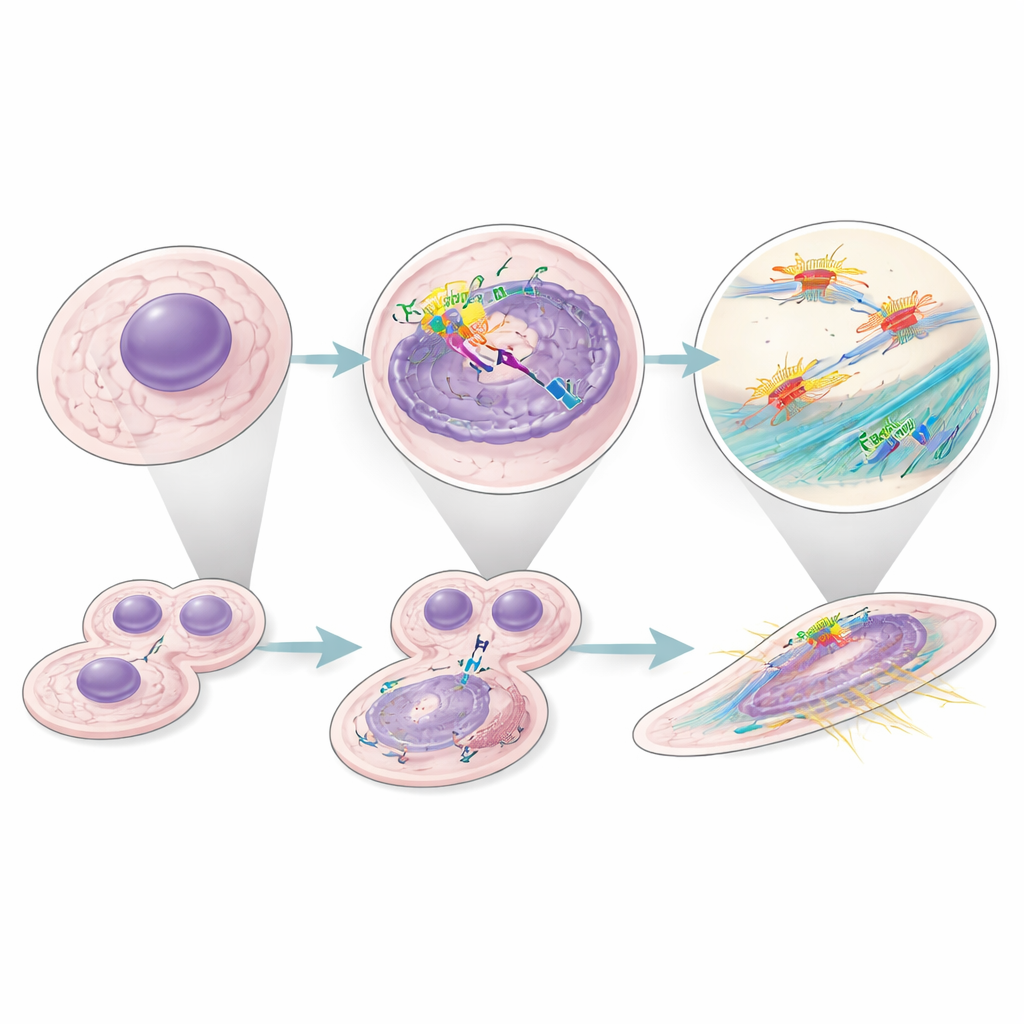
Um impacto mais amplo em vários cânceres
Para verificar se esse comportamento era exclusivo de tumores renais, os autores exploraram muitos conjuntos de dados de RNA de célula única e de bulk de cânceres humanos. Em tumores onde a alta expressão de Fator H previu pior sobrevida, assinaturas de fibroblastos também se associaram a desfechos piores. Dentro dos tumores renais, eles identificaram um estado celular maligno específico que expressava fortemente Fator H, apresentava programas ativos do ciclo celular e esteve associado a menor sobrevida dos pacientes. Em conjunto, esses achados sugerem que o Fator H intracelular age como um agente pró‑tumoral amplo, operando dentro tanto das células cancerosas quanto dos fibroblastos de suporte em vários tipos de câncer.
O que isso significa para pacientes e terapias
Este trabalho derruba a ideia de que o Fator H é apenas um regulador circulante das reações imunes. Em vez disso, ele surge como um ajudante intracelular multitarefa que incentiva os tumores a crescer, facilitando a progressão das células pelo ciclo de divisão e ajustando seu arcabouço interno para movimento. Isso ajuda a explicar por que a superexpressão de Fator H é um sinal de alerta tão forte no câncer. Também significa que drogas projetadas para bloquear o Fator H na superfície tumoral ou no sangue podem não desarmar completamente suas funções ocultas internas. Terapias futuras provavelmente precisarão atingir seus papéis externos e internos para retardar efetivamente a progressão tumoral.
Citação: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Palavras-chave: fator H do complemento, carcinoma de células claras do rim, fibroblastos associados ao câncer, microambiente tumoral, regulação do ciclo celular