Clear Sky Science · nl
Intracellulair complement Factor H bevordert tumorgroei via modulatie van de celcyclus en het actinecytoskelet
Waarom deze verborgen kankermedewerker ertoe doet
Kanker wordt vaak beschreven als een strijd tussen groeiende tumoren en het immuunsysteem. Deze studie onthult dat een van de moleculen van het immuunsysteem zelf, een eiwit genaamd Factor H, stilletjes van kant kan veranderen. In plaats van alleen in het bloed te werken om ontsteking te reguleren, wordt Factor H aangetroffen binnen tumorcellen en nabije ondersteunende cellen, waar het kankers helpt groeien, overleven en mogelijk uitzaaien. Inzicht in deze onverwachte "dubbele rol" opent nieuwe mogelijkheden om te voorspellen hoe agressief een tumor zal zijn en hoe je slimmer therapieën kunt ontwerpen.
Een bekend eiwit op een onverwachte plek
Factor H staat vooral bekend als beschermer van het complementsysteem, een onderdeel van de aangeboren immuniteit dat helpt microben en beschadigde cellen uit het bloed te verwijderen. Hoge niveaus van Factor H rond tumoren waren al gekoppeld aan slechtere uitkomsten bij verschillende kankers, waaronder heldercellig nierkanker. Toch kon zijn gebruikelijke rol in het bloed niet volledig verklaren waarom patiënten waarvan de tumoren te veel Factor H produceren doorgaans slechter af zijn. Door patiëntgegevens, single‑cell sequencing en celbiologie te combineren, laten de auteurs zien dat veel cellen binnen niertumoren — met name kanker‑geassocieerde fibroblasten en maligne nierrijke cellen — actief hun eigen Factor H aanmaken en een deel daarvan binnen de cel houden in plaats van het uit te scheiden.
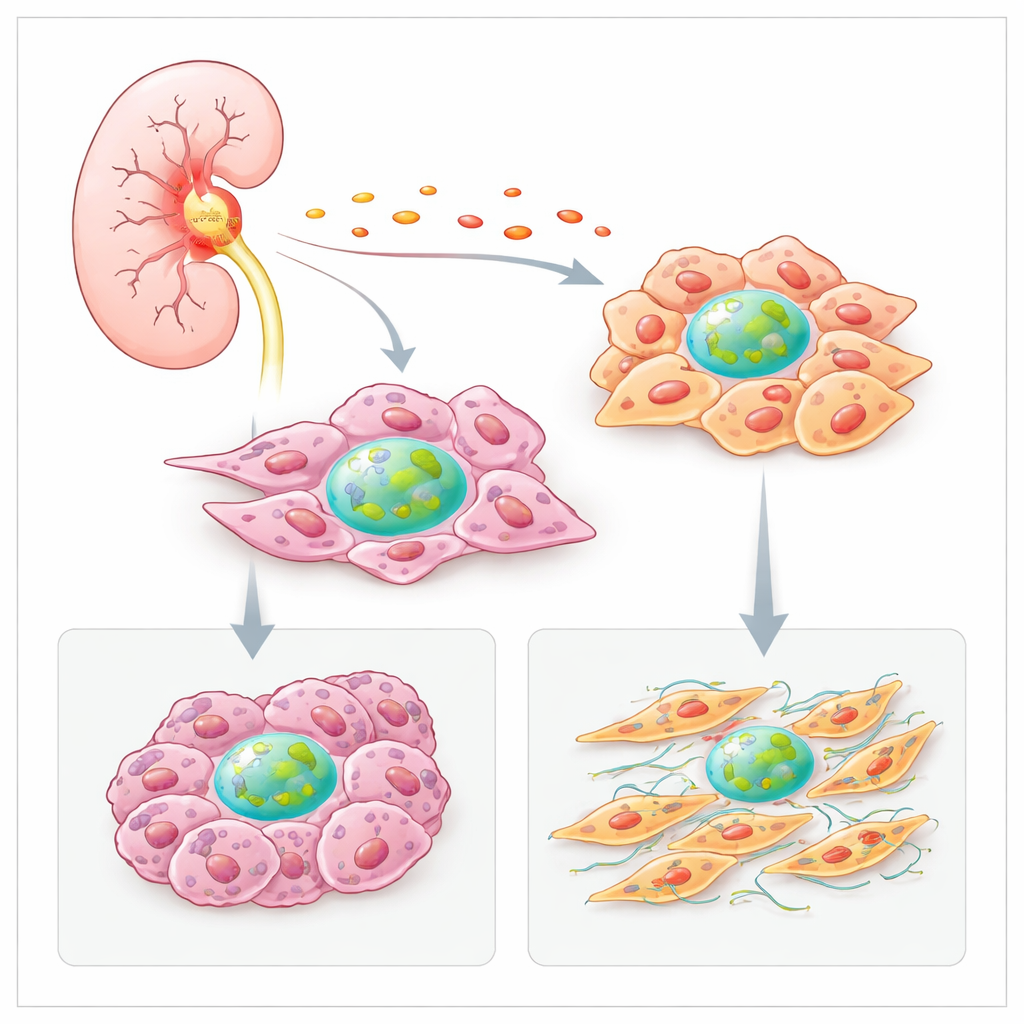
Ontsteking zet de productie van Factor H hoger
Het team vroeg zich eerst af waarom tumoren meer Factor H produceren dan gezond nierweefsel. Ze analyseerden grote kankerdatasets en ruimtelijke kaarten van tumorsecties en vonden dat gebieden rijk aan fibroblasten en kankercellen ook hoge niveaus van het Factor H‑gen bevatten. Deze hete zones overlappen vaak met handtekeningen van ontstekingsmoleculen, zoals het cytokine IL‑6. In gekweekte nierkankercellen verhoogde IL‑6 sterk de productie van Factor H, terwijl andere ontstekingssignalen deze productie in fibroblasten opvoerden. Dit suggereert dat de ontstoken tumormicroomgeving lokale cellen aanzet om hun eigen Factor H op te voeren, waardoor een vicieuze cirkel van groei en overleving ontstaat.
In de kern helpt het cellen stoptekens te negeren
Bij onderzoek binnenin de cellen ontdekten de onderzoekers een kleinere, intracellulaire vorm van Factor H die in meerdere compartimenten voorkomt, waaronder de celkern. Daar gaat het fysiek in wisselwerking met sleutelregelaars van de celcyclus, in het bijzonder een transcriptiefactor genaamd E2F3 die cellen helpt van rust naar celdeling te schakelen. Wanneer het Factor H‑gen werd uitgeschakeld, vertraagden fibroblasten en kankercellen hun replicatie, stapelden ze zich op in de rustfase en vertoonden ze meer actieve p53, een veelgeprezen "bewaker"-eiwit dat groei kan stoppen of celdood kan veroorzaken. Belangrijk is dat het eenvoudig toevoegen van normale, uitgescheiden Factor H van buitenaf dit effect niet herstelde, wat benadrukt dat de interne voorraad is wat p53 in toom houdt en voortdurende proliferatie mogelijk maakt.
Het skelet van de cel hervormen voor groei en beweging
In nierkankercellen, maar niet in fibroblasten, bond intracellulair Factor H ook aan componenten van het actine‑cappingcomplex, dat regelt hoe actinedraden groeien en het interne geraamte van de cel stabiliseren. Wanneer Factor H werd uitgeschakeld, werden kankercellen ronder, verloren ze hun georganiseerde stressvezels en hadden ze moeite compacte driedimensionale sferen te vormen — een experimentele proxy voor tumorgroei en cohesie. Het gelijktijdig uitschakelen van zowel Factor H als het capping‑eiwit verergerde de defecten niet, wat suggereert dat ze in dezelfde route werkzaam zijn. Deze veranderingen traden op zelfs wanneer p53 werd geblokkeerd, wat aangeeft dat Factor H onafhankelijk zowel celdeling als structurele veranderingen ondersteunt die invasie en metastase kunnen bevorderen.
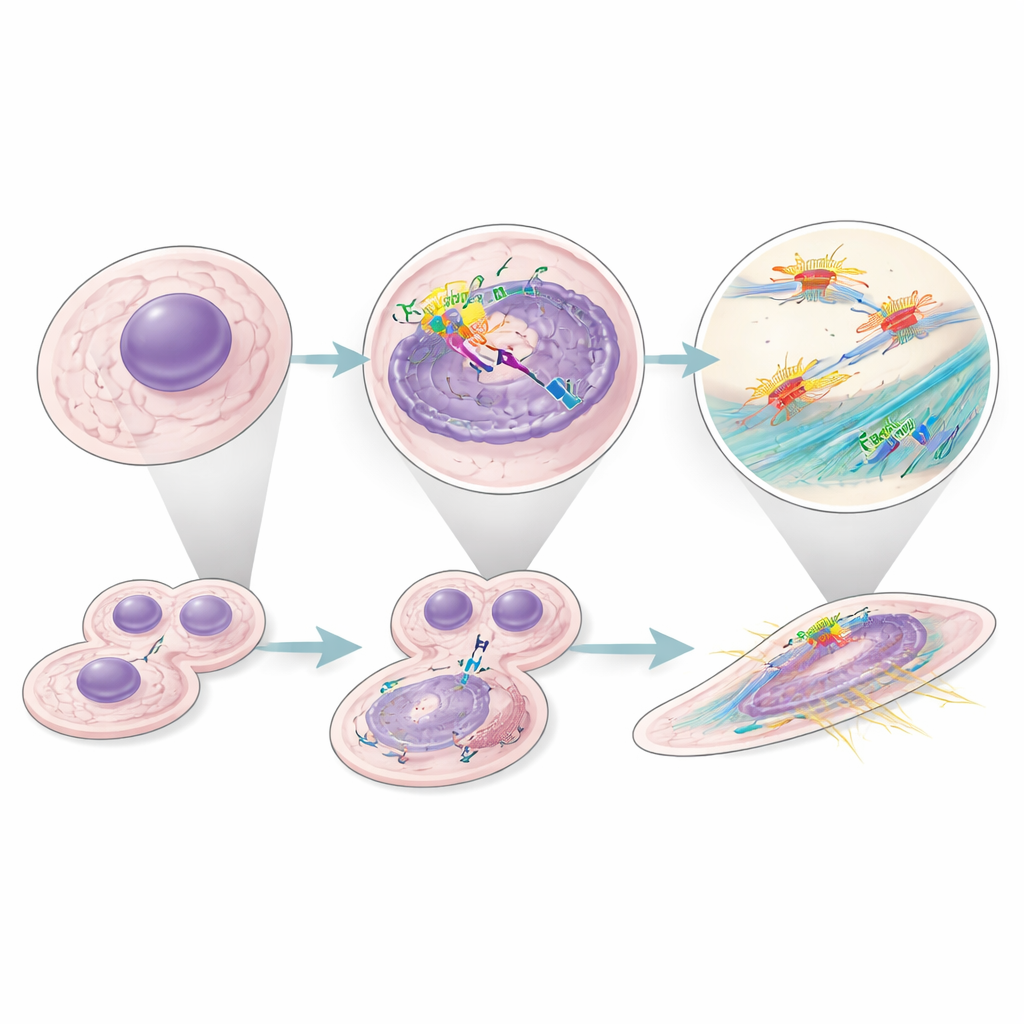
Een bredere impact in veel kankers
Om te onderzoeken of dit gedrag uniek is voor niertumoren, doorzochten de auteurs vele single‑cell en bulk RNA‑datasets van menselijke kankers. In tumoren waar hoge Factor H‑expressie slechtere overleving voorspelde, waren fibroblasthandtekeningen ook gekoppeld aan slechtere uitkomsten. Binnen niertumoren identificeerden ze een specifieke maligne celtoestand die sterk Factor H uitsprak, actieve celcyclusprogramma’s toonde en geassocieerd was met kortere patiëntoverleving. Samen suggereren deze bevindingen dat intracellulair Factor H fungeert als een breed pro‑tumoragent, werkzaam binnen zowel kankercellen als hun ondersteunende fibroblasten in meerdere kankertypen.
Wat dit betekent voor patiënten en therapieën
Dit werk doorbreekt het idee dat Factor H alleen een circulerende regulator van immuunreacties is. In plaats daarvan komt het naar voren als een multitaskende, intracellulaire helper die tumoren aanmoedigt te groeien door cellen gemakkelijker door de delingscyclus te loodsen en hun interne geraamte fijn af te stemmen voor beweging. Dit helpt verklaren waarom overexpressie van Factor H zo’n sterke waarschuwingsfactor bij kanker is. Het betekent ook dat geneesmiddelen die ontworpen zijn om Factor H op het tumormembraan of in het bloed te blokkeren mogelijk zijn verborgen, interne functies niet volledig uitschakelen. Toekomstige therapieën zullen waarschijnlijk beide, zowel externe als interne rollen, moeten aanpakken om tumorgroei effectief te vertragen.
Bronvermelding: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Trefwoorden: complementfactor H, heldercel niercelcarcinoom, kanker-geassocieerde fibroblasten, tumormicroomgeving, regulatie van de celcyclus