Clear Sky Science · de
Intrazelluläres Komplementfaktor H fördert das Tumorwachstum durch Modulation des Zellzyklus und des Aktin-Zytoskeletts
Warum dieser verborgene Krebshelfer wichtig ist
Krebs wird oft als ein Kampf zwischen wachsenden Tumoren und dem Immunsystem beschrieben. Diese Studie zeigt, dass eines der eigenen Moleküle des Immunsystems, ein Protein namens Faktor H, stillschweigend die Seiten wechseln kann. Statt nur im Blutkreislauf Entzündungen zu steuern, findet sich Faktor H innerhalb von Tumorzellen und in benachbarten Stützzellen, wo er Tumoren beim Wachstum, Überleben und möglicherweise bei der Ausbreitung hilft. Das Verständnis dieses unerwarteten „Doppellebens“ eröffnet neue Möglichkeiten, aggressives Tumorverhalten vorherzusagen und gezieltere Therapien zu entwickeln.
Ein bekanntes Protein an einem unerwarteten Ort
Faktor H ist vor allem als Wächter des Komplementsystems bekannt, einem Teil der angeborenen Immunität, der dabei hilft, Mikroben und beschädigte Zellen aus dem Blut zu entfernen. Hohe Konzentrationen von Faktor H in Tumorumgebungen waren bereits mit schlechteren Prognosen bei mehreren Krebsarten, einschließlich des klarzelligen Nierenzellkarzinoms, verbunden. Seine übliche, blutgebundene Rolle konnte jedoch nicht vollständig erklären, warum Patienten mit tumoraler Überproduktion von Faktor H schlechtere Verläufe haben. Durch die Kombination von Patientendaten, Einzelzellsequenzierung und Zellbiologie zeigen die Autorinnen und Autoren, dass viele Zellen innerhalb von Nierentumoren – insbesondere tumorassoziierte Fibroblasten und maligne Nierenzellen – aktiv ihren eigenen Faktor H produzieren und einen Teil davon in der Zelle behalten, anstatt ihn zu sezernieren.
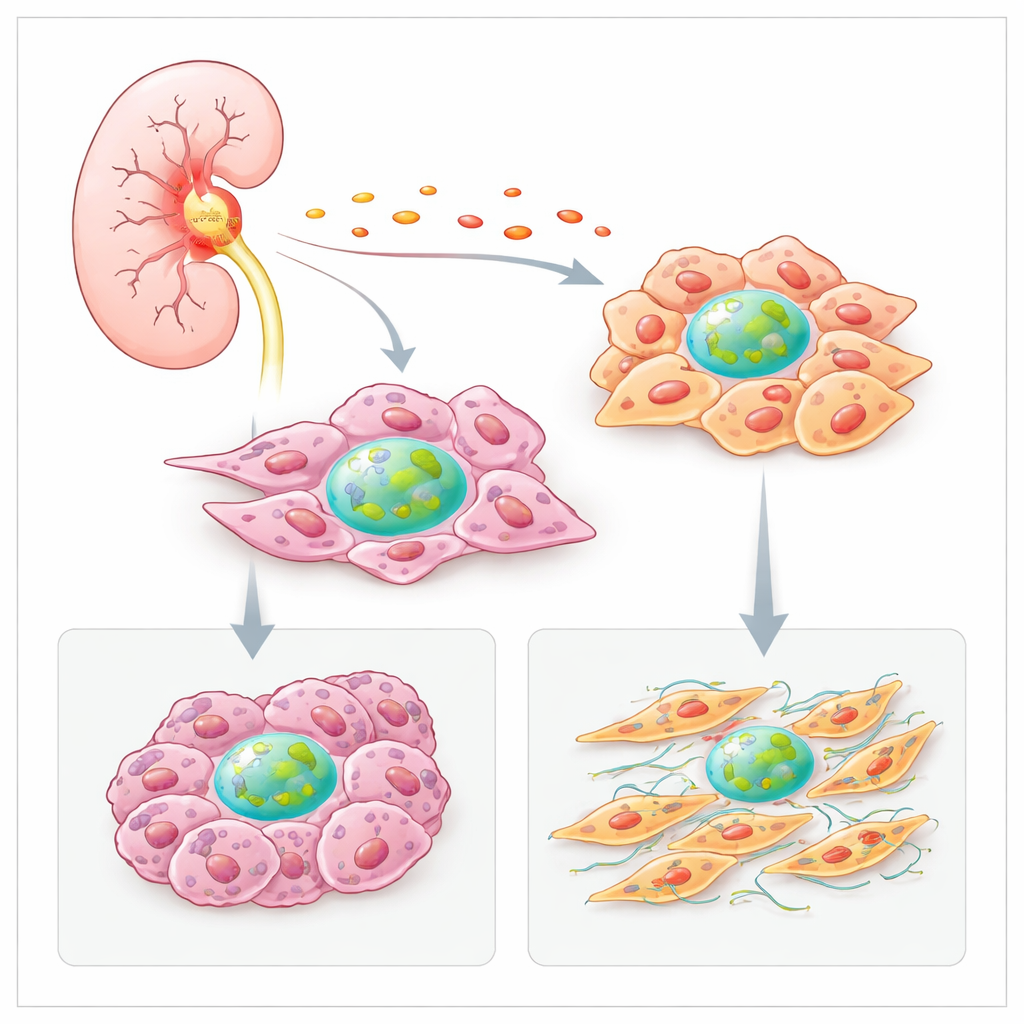
Entzündung erhöht die Faktor-H-Produktion
Die Forschergruppen fragten zunächst, warum Tumoren mehr Faktor H produzieren als gesundes Nierengewebe. Sie analysierten große Krebsdatensätze und räumliche Karten von Tumorschnitten und fanden, dass Bereiche mit vielen Fibroblasten und Krebszellen auch hohe Werte des Faktor-H-Gens aufwiesen. Diese Hotspots überschritten sich häufig mit Signaturen entzündlicher Moleküle, wie dem Zytokin IL‑6. In kultivierten Nierenkrebszellen steigerte IL‑6 stark die Produktion von Faktor H, während andere entzündliche Signale die Produktion in Fibroblasten erhöhten. Das legt nahe, dass die entzündete Tumorumgebung lokale Zellen dazu antreibt, ihren eigenen Faktor H hochzufahren und so einen Teufelskreis aus Wachstum und Überleben verstärkt.
Im Zellkern: Hilft Zellen, Stoppzeichen zu ignorieren
Beim Blick ins Zellinnere entdeckten die Forschenden eine kleinere, intrazelluläre Form von Faktor H, die in mehreren Kompartimenten auftritt, darunter auch im Zellkern. Dort interagiert sie physisch mit zentralen Steuerern des Zellzyklus, insbesondere mit einem Transkriptionsfaktor namens E2F3, der Zellen vom Ruhezustand in die Teilung treiben hilft. Bei Stilllegung des Faktor-H-Gens verlangsamten sich die Teilung von Fibroblasten und Krebszellen, sie sammelten sich in der Ruhephase an und zeigten verstärkte Aktivität von p53, einem bekannten „Wächter“-Protein, das Wachstum stoppen oder Zelltod auslösen kann. Bedeutend ist, dass das einfache Hinzufügen von normalem, sezerniertem Faktor H von außen diesen Effekt nicht aufhob, was unterstreicht, dass der intrazelluläre Bestand dafür verantwortlich ist, p53 in Schach zu halten und kontinuierliche Proliferation zu ermöglichen.
Umgestalten des Zellgerüsts für Wachstum und Bewegung
In Nierenkrebszellen, aber nicht in Fibroblasten, band intrazelluläres Faktor H zudem Komponenten des Aktin-Capping-Komplexes, der das Wachstum von Aktinfilamenten reguliert und das interne Gerüst der Zelle stabilisiert. Nach Stilllegung von Faktor H wurden Krebszellen runder, verloren ihre organisierten Stressfasern und taten sich schwer, kompakte dreidimensionale Sphäroide zu bilden – ein experimenteller Ersatz für Tumorwachstum und Zusammenhalt. Die gleichzeitige Stilllegung von Faktor H und des Capping-Proteins verschlechterte die Defekte nicht weiter, was darauf hindeutet, dass sie entlang desselben Weges wirken. Diese Veränderungen traten selbst dann auf, wenn p53 blockiert war, was darauf hinweist, dass Faktor H sowohl die Zellteilung als auch die strukturellen Anpassungen, die Invasion und Metastasierung begünstigen können, unabhängig unterstützt.
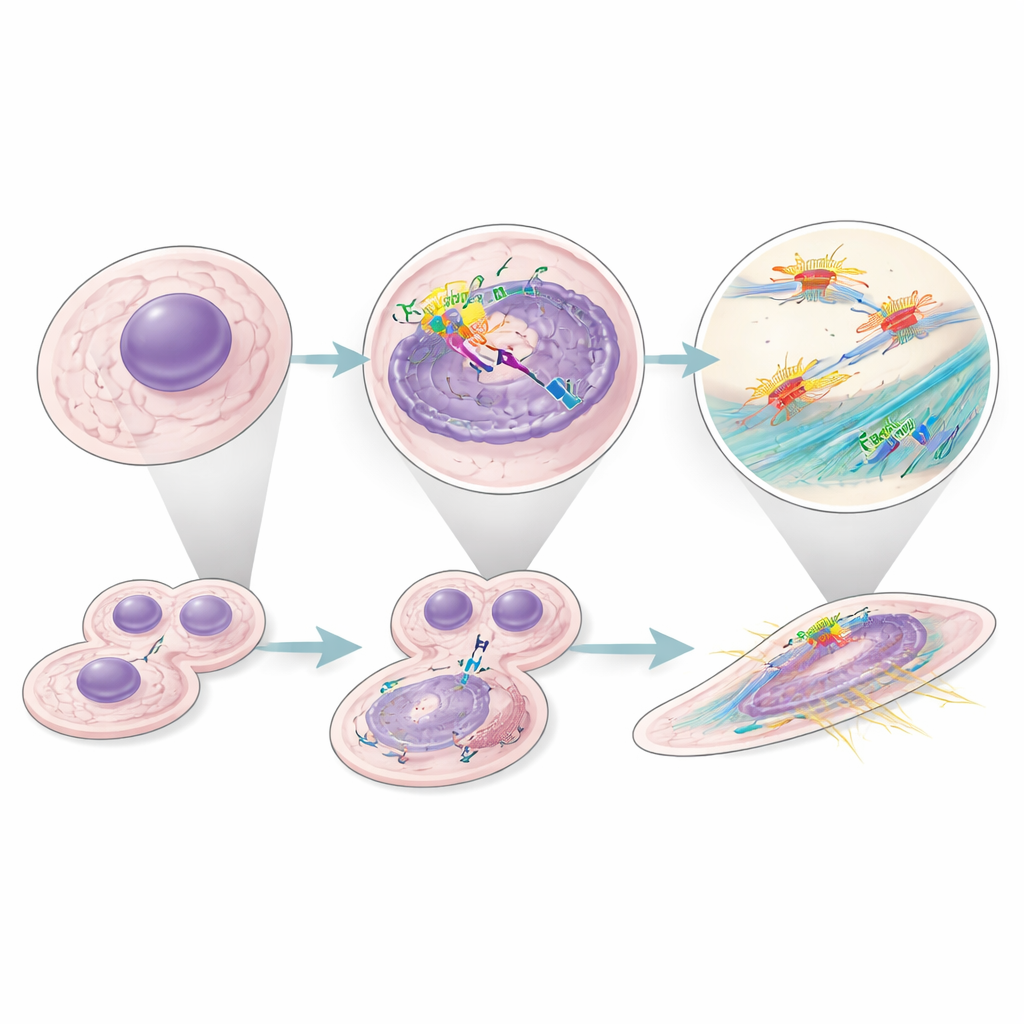
Eine breitere Wirkung in vielen Krebsarten
Um zu prüfen, ob dieses Verhalten auf Nierentumoren beschränkt ist, durchsuchten die Autorinnen und Autoren zahlreiche Einzelzell- und Bulk-RNA-Datensätze aus menschlichen Krebserkrankungen. In Tumoren, in denen hohe Faktor-H-Expression ein schlechtes Überleben vorhersagte, waren auch Fibroblasten-Signaturen mit ungünstiger Prognose verknüpft. Innerhalb von Nierentumoren identifizierten sie einen spezifischen malignen Zellzustand, der stark Faktor H exprimierte, aktive Zellzyklusprogramme zeigte und mit verkürzter Patient*innenüberlebenszeit assoziiert war. Zusammengenommen deuten diese Befunde darauf hin, dass intrazelluläres Faktor H als breit wirkender tumorfördernder Faktor fungiert, der sowohl in Krebszellen als auch in ihren unterstützenden Fibroblasten in mehreren Krebsarten aktiv ist.
Was das für Patient*innen und Therapien bedeutet
Diese Arbeit widerlegt die Vorstellung, dass Faktor H nur ein zirkulierender Regulator von Immunreaktionen ist. Stattdessen tritt es als multitaskingfähiger, intrazellulärer Helfer zutage, der Tumoren fördert, indem er Zellen die Teilung erleichtert und ihr inneres Gerüst für Bewegung feinabstimmt. Das erklärt, warum eine Überexpression von Faktor H ein so starkes Warnsignal beim Krebs ist. Es bedeutet auch, dass Wirkstoffe, die Faktor H nur an der Tumoroberfläche oder im Blut blockieren, seine verborgenen, intrazellulären Funktionen möglicherweise nicht vollständig außer Kraft setzen. Zukünftige Therapien müssen wahrscheinlich sowohl seine externen als auch seine internen Rollen anvisieren, um das Tumorwachstum effektiv zu verlangsamen.
Zitation: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Schlüsselwörter: Komplementfaktor H, klarzellige Nierenzellkarzinom, tumorassoziierte Fibroblasten, Tumormikroumgebung, Zellzyklusregulation