Clear Sky Science · zh
ENA1 缺失在免疫受抑小鼠菌血症模型中削弱了布拉氏酵母(Saccharomyces ‘boulardii’)益生菌的毒力
为何有益的酵母有时会变成有害
许多人服用益生菌酵母片来缓解肠道不适或在使用抗生素期间预防腹泻。其中最受欢迎的选择之一常以布拉氏酵母(Saccharomyces boulardii)名义出售。尽管它对许多患者有帮助,但临床医生注意到一个令人担忧的趋势:在一些病重或免疫受损的人群中,这种“友好”酵母会从肠道进入血液,导致严重甚至致命的感染。本研究探讨了一个对现代医学至关重要的问题:我们能否重新设计这种益生菌,使其保留肠道益处,同时大大降低引发危险性血流感染的能力?
对脆弱患者的日益担忧
世界各地的医院越来越多地报告,在重症监护病房、术后或严重疾病期间,这种益生菌酵母出现在患者血液中的病例。这些患者通常防御力减弱,并使用导管等侵入性器械,为微生物提供了进入体内的新途径。在某些医院,与这种益生菌相关的感染发生率几乎可与经典致病真菌相当。然而,迄今为止,大多数关于这种酵母的研究要么关注其健康益处,要么关注如何将其工程化用于产生药物,而很少关注其对脆弱患者构成风险的具体原因。作者们旨在通过在同一项目中同时研究其有益与有害特性来弥补这一空白。
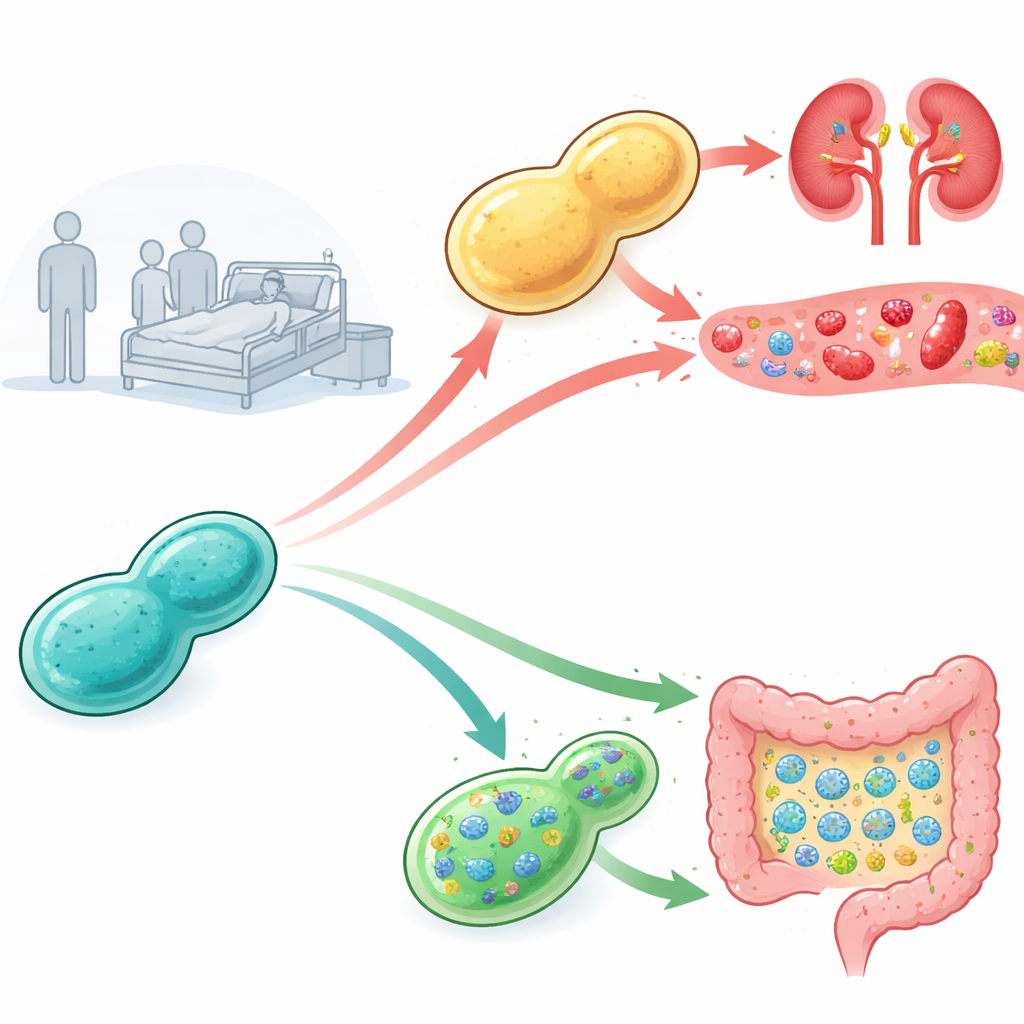
在小鼠体内追踪毒力
研究人员从商业产品和医院患者处收集了益生菌酵母,并在免疫受抑的小鼠中测试了各株的致病性。从商业产品分离的酵母注射后所有小鼠存活,但来自患者的某些分离株导致高死亡率和肾脏中大量真菌生长,这是严重菌血症的标志。为了解原因,团队在感染前后分离出许多亚系并在实验室平板上用不同应激条件挑战它们。他们注意到,毒力较高的患者分离株,尤其是通过小鼠体内传代后的版本,对含钠或锂盐的高盐条件具有异常耐受性,提示耐受苛刻内环境的能力可能与致病性有关。
解除一个关键生存泵的武装
酵母的耐盐性取决于将离子泵入或泵出细胞的膜转运蛋白。作者关注了两个这样的基因,ENA1 和 NHA1,它们帮助细胞抵御盐和碱性应激。使用 CRISPR 基因编辑,他们在六个不同的益生菌背景中分别敲除每个基因,包含商业与临床分离株。结果对其中一个基因格外明确:删除 ENA1 后,所有测试菌株在小鼠中的危害显著降低。所有动物在短期菌血症实验中存活,肾脏中的真菌水平保持相对较低,即便起始菌株本来毒力很强。相比之下,删除 NHA1 并未提供一致的安全性提升,有时反而使某些菌株更具害性,这突出表明基因改变的影响会强烈依赖于更广泛的遗传背景。
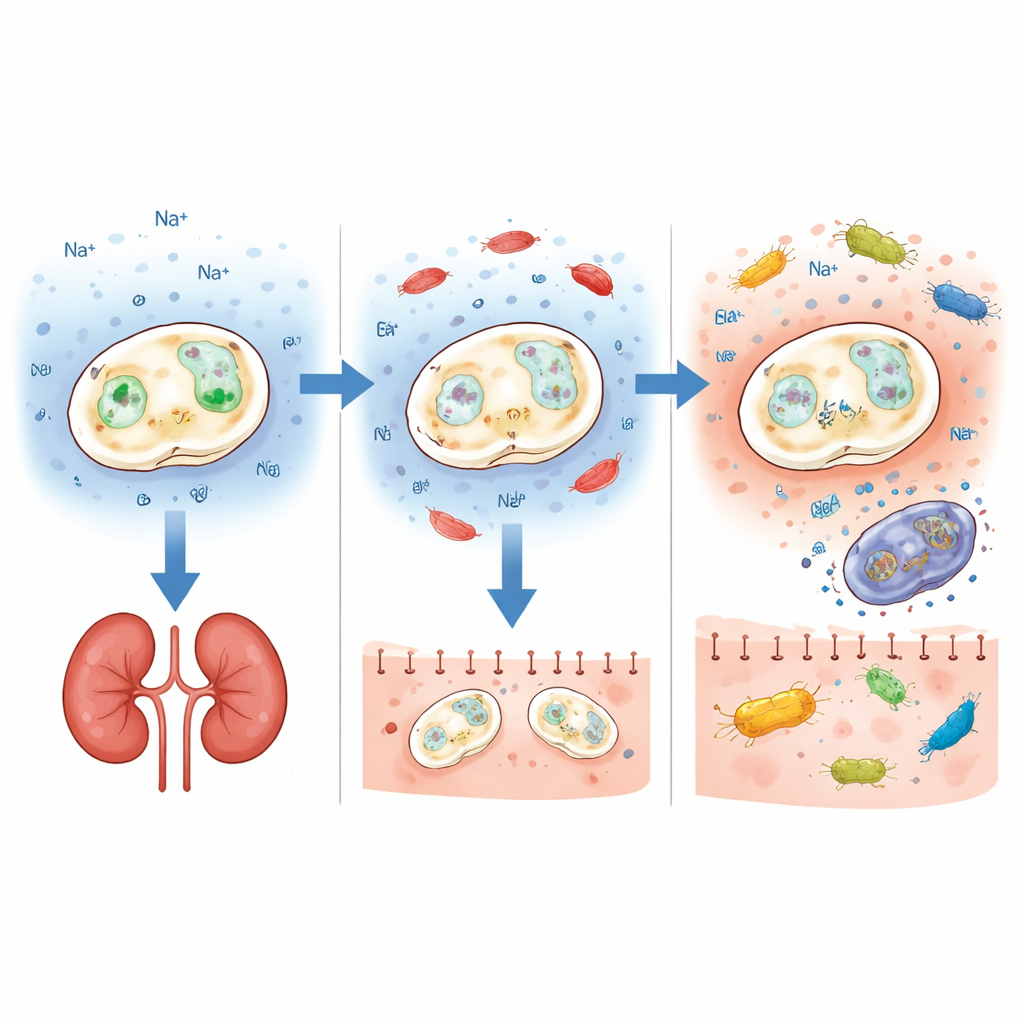
保留益处,并增加额外武器
只有在仍履行其肠道功能时,较安全的益生菌才有用。因此,团队检查了缺失 ENA1 的菌株是否仍能在标准培养基和类肠道条件下良好生长,包括中等酸度、胆盐以及小肠和大肠不同部位的 pH 值。ENA1 敲除株的表现与原始益生菌大体相似,仅在异常高的碱性或高盐条件下出现困难,而这些条件并不典型于健康肠道。在口服每日给药的活体小鼠中,改造酵母在肠道中的定殖水平与商业菌株相当,停药后被清除的速度也相似。该改变株还以与原始益生菌类似的方式改变了肠道细菌群落的组成和多样性,表明其整体肠道影响仍然保留。
为未来疗法构建更安全的平台
除了安全性,作者还展示了“定制”益生菌的潜能。作为概念验证的步骤,他们用编码抗李斯特菌(Listeria)短抗菌肽 Leucocin C 的 DNA 替换了 ENA1 基因。工程化酵母仍然在小鼠中表现出显著降低的菌血症致病能力,在实验室测试中生长良好,能耐受商业生产中使用的冻干工艺,并分泌出在培养中抑制李斯特菌的活性肽。综合来看,这些结果表明敲除 ENA1 可构建一个有前景的平台菌株:这种酵母在脆弱患者中极不可能引发危及生命的菌血症,但仍保留其益生功能,并可进一步装备以对抗有害细菌。简言之,该研究表明,可以将有时存在风险的“帮手”转变为未来肠道疗法中更安全、可编程的盟友。
引用: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
关键词: 益生菌酵母, 菌血症, 基因编辑, 微生物组, 定制益生菌