Clear Sky Science · pt
Deficiência de ENA1 atenua a virulência da levedura probiótica Saccharomyces ‘boulardii’ em modelo murino de fungemia em imunossuprimidos
Por que uma levedura útil às vezes pode se tornar prejudicial
Muitas pessoas tomam comprimidos de levedura probiótica para acalmar o intestino irritado ou prevenir diarreia durante tratamento com antibióticos. Uma das opções mais populares é uma levedura frequentemente vendida pelo nome Saccharomyces boulardii. Embora ajude muitos pacientes, médicos observam uma tendência preocupante: em alguns indivíduos muito doentes ou imunocomprometidos, essa levedura amistosa pode escapar do intestino para a corrente sanguínea e causar infecções graves, às vezes letais. Este estudo investiga uma questão premente para a medicina moderna: podemos redesenhar esse probiótico para que mantenha seus benefícios intestinais, mas fique muito menos capaz de causar infecções perigosas na corrente sanguínea?
Preocupações crescentes em pacientes frágeis
Hospitais ao redor do mundo relatam cada vez mais casos em que a levedura probiótica aparece no sangue de pacientes em unidades de terapia intensiva, após cirurgias ou durante enfermidades graves. Essas pessoas frequentemente têm defesas enfraquecidas e dispositivos invasivos, como cateteres, que oferecem novas rotas de entrada aos microrganismos. Em alguns hospitais, infecções associadas a essa levedura probiótica ocorrem quase tão frequentemente quanto as causadas por fungos patogênicos clássicos. Ainda assim, até agora, a maior parte das pesquisas sobre essa levedura focou seja em seus benefícios à saúde, seja em formas de usá‑la para produzir medicamentos, com pouca atenção ao que realmente a torna arriscada para pacientes vulneráveis. Os autores procuraram preencher essa lacuna estudando simultaneamente seus lados benéfico e prejudicial no mesmo projeto.
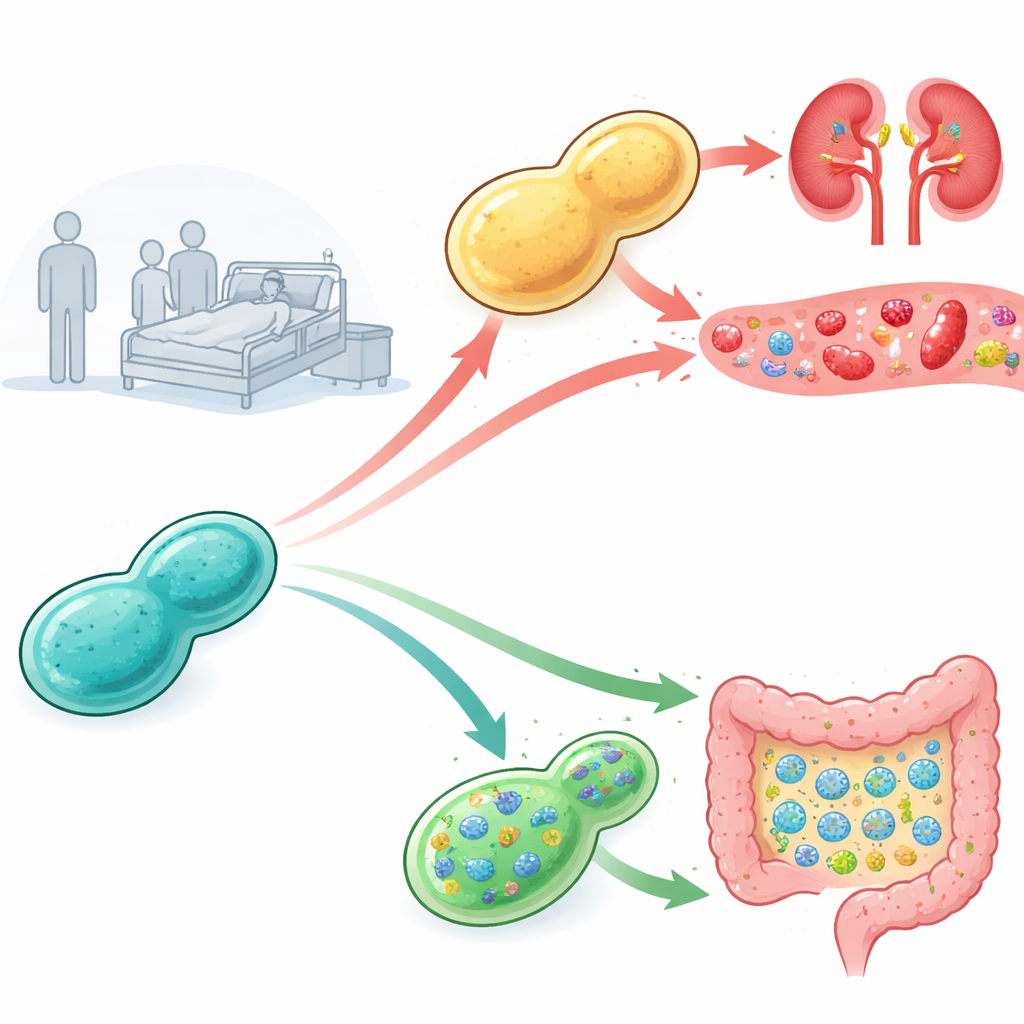
Rastreando a virulência em camundongos
Os pesquisadores coletaram levedura probiótica de produtos comerciais e de pacientes hospitalares e testaram o grau de periculosidade de cada amostra em camundongos com o sistema imune comprometido. Todos os camundongos injetados com levedura de produtos comerciais sobreviveram, mas algumas leveduras derivadas de pacientes causaram altas taxas de mortalidade e forte crescimento fúngico nos rins, sinal de infecção sanguínea grave. Para entender o motivo, a equipe isolou muitas sublinhagens da levedura antes e depois da infecção e as expôs a diferentes estresses em placas de laboratório. Observou‑se que as amostras mais virulentas de pacientes, e especialmente as variantes que haviam passado pelos camundongos, eram incomumente tolerantes a condições salinas contendo sais de sódio ou lítio, sugerindo que a capacidade de resistir a ambientes internos agressivos pode estar ligada à sua habilidade de causar doença.
Desarmando uma bomba de sobrevivência-chave
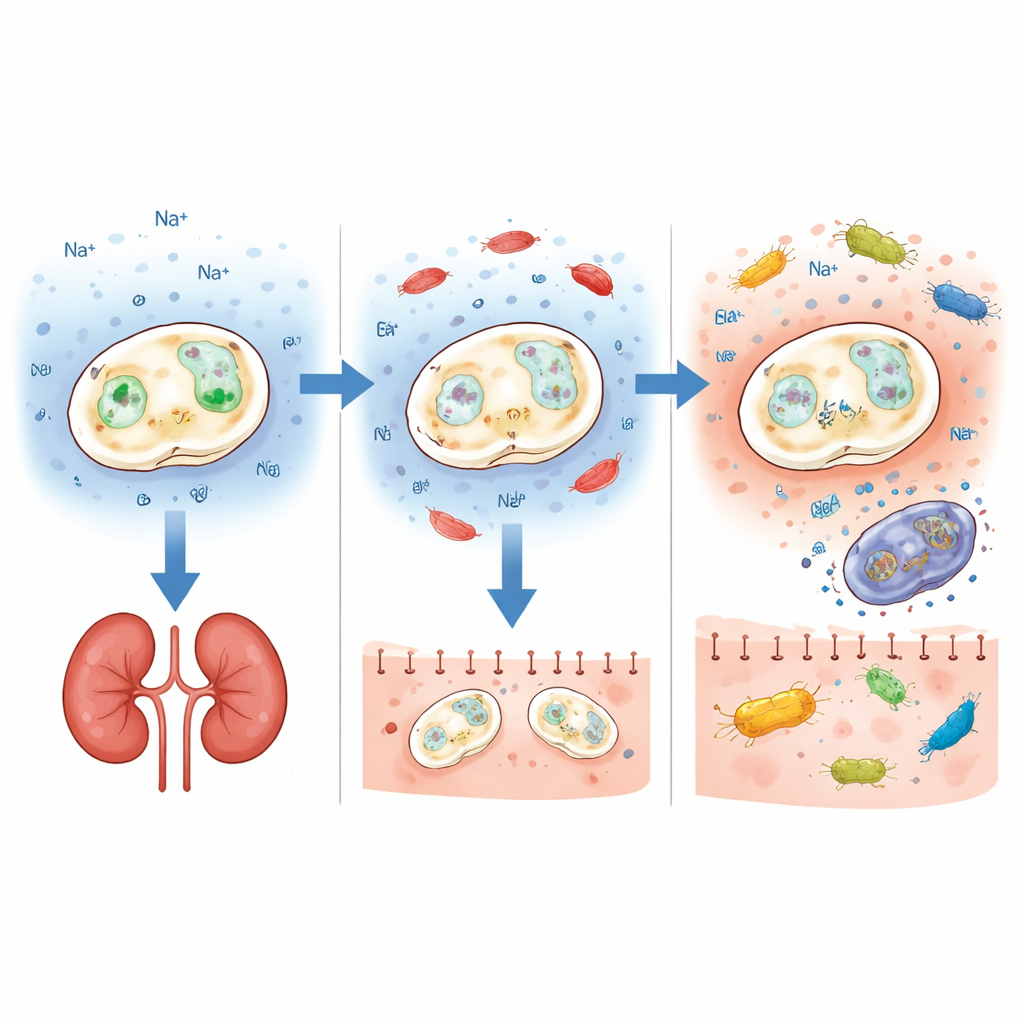
A tolerância ao sal em leveduras depende de transportadores de membrana que bombeiam íons para dentro e para fora da célula. Os autores concentraram‑se em dois genes desse tipo, ENA1 e NHA1, que ajudam as células a sobreviver ao estresse por sal e alcalinidade. Usando edição gênica por CRISPR, deletaram cada gene separadamente em seis diferentes fundos probióticos, incluindo isolados comerciais e clínicos. Os resultados foram claramente impressionantes para um dos genes: quando ENA1 foi removido, todas as linhagens testadas causaram muito menos dano em camundongos. Todos os animais sobreviveram à infecção sistêmica de curto prazo, e os níveis fúngicos nos rins permaneceram relativamente baixos, mesmo quando a linhagem inicial era originalmente bastante virulenta. Em contraste, a deleção de NHA1 não conferiu um benefício consistente de segurança e às vezes até tornou linhagens mais nocivas, ressaltando como o impacto de uma alteração genética pode depender fortemente do contexto genético mais amplo.
Preservando os benefícios e adicionando uma arma extra
Um probiótico mais seguro só é útil se ainda desempenhar sua função no intestino. A equipe, portanto, verificou se as linhagens deficientes em ENA1 ainda cresciam bem em meios de cultura padrão e sob condições semelhantes às do intestino, incluindo acidez moderada, sais biliares e os níveis de pH encontrados ao longo do intestino delgado e do cólon. O knockout de ENA1 comportou‑se de forma muito parecida com o probiótico original, exceto que teve dificuldades apenas sob condições incomumente muito alcalinas ou salinas, não típicas de um intestino saudável. Em camundongos vivos recebendo doses diárias por via oral, a levedura modificada colonizou o intestino em níveis similares aos da linhagem comercial e foi eliminada em ritmo parecido após a interrupção da administração. A linhagem alterada também deslocou a composição e a diversidade da comunidade bacteriana intestinal de maneira muito semelhante ao probiótico original, sugerindo que seu impacto geral no intestino permaneceu intacto.
Construindo uma plataforma mais segura para terapias futuras
Além da segurança, os autores mostraram o que um probiótico “sob medida” poderia fazer. Em um passo de prova de conceito, substituíram o gene ENA1 por DNA codificando Leucocin C, um pequeno peptídeo antibacteriano direcionado contra Listeria, um importante patógeno transmitido por alimentos. A levedura engenheirada ainda apresentou habilidade drasticamente reduzida de causar infecções sanguíneas em camundongos, cresceu bem em testes de laboratório, resistiu a procedimentos de liofilização usados na produção comercial e secretou um peptídeo ativo que inibiu Listeria em cultura. Tomados em conjunto, esses resultados sugerem que a deleção de ENA1 cria uma linhagem‑plataforma promissora: uma levedura muito menos propensa a causar fungemia potencialmente fatal em pacientes frágeis, que ainda preserva seu comportamento probiótico e pode ser equipada adicionalmente para combater bactérias nocivas. Em termos simples, o estudo demonstra ser possível transformar um ajudante por vezes arriscado em um aliado mais seguro e programável para futuras terapias intestinais.
Citação: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
Palavras-chave: levedura probiótica, fungemia, edição gênica, microbioma, probióticos sob medida