Clear Sky Science · fr
La déficience en ENA1 atténue la virulence de la levure probiotique Saccharomyces ‘boulardii’ dans un modèle murin d fongémie chez des souris immunodéprimées
Pourquoi une levure utile peut parfois devenir nuisible
Beaucoup de personnes prennent des gélules de levure probiotique pour apaiser un intestin dérangé ou prévenir la diarrhée lors d’un traitement antibiotique. L’un des choix les plus populaires est une levure souvent commercialisée sous le nom Saccharomyces boulardii. Bien qu’elle aide de nombreux patients, les médecins constatent une tendance inquiétante : chez certains sujets très malades ou immunodéprimés, cette levure pourtant « amie » peut s’échapper de l’intestin, gagner la circulation sanguine et provoquer des infections graves, parfois mortelles. Cette étude pose une question cruciale pour la médecine moderne : peut‑on redesigner ce probiotique pour qu’il conserve ses bénéfices intestinaux tout en devenant beaucoup moins susceptible de provoquer des infections sanguines dangereuses ?
Des préoccupations croissantes chez les patients fragiles
Des hôpitaux du monde entier rapportent de plus en plus de cas où la levure probiotique est retrouvée dans le sang de patients en unité de soins intensifs, après une chirurgie ou lors d’une maladie sévère. Ces personnes ont souvent des défenses amoindries et des dispositifs invasifs comme des cathéters, qui offrent aux microbes de nouvelles portes d’entrée dans l’organisme. Dans certains établissements, les infections liées à cette levure probiotique surviennent presque aussi souvent que celles causées par des champignons pathogènes classiques. Pourtant, jusqu’à présent, la plupart des recherches sur cette levure se sont concentrées soit sur ses bienfaits pour la santé, soit sur son éventuelle utilisation comme usine à médicaments, accordant peu d’attention aux facteurs qui la rendent risquée pour les patients vulnérables. Les auteurs ont voulu combler cette lacune en étudiant à la fois ses aspects utiles et dangereux dans le même projet.
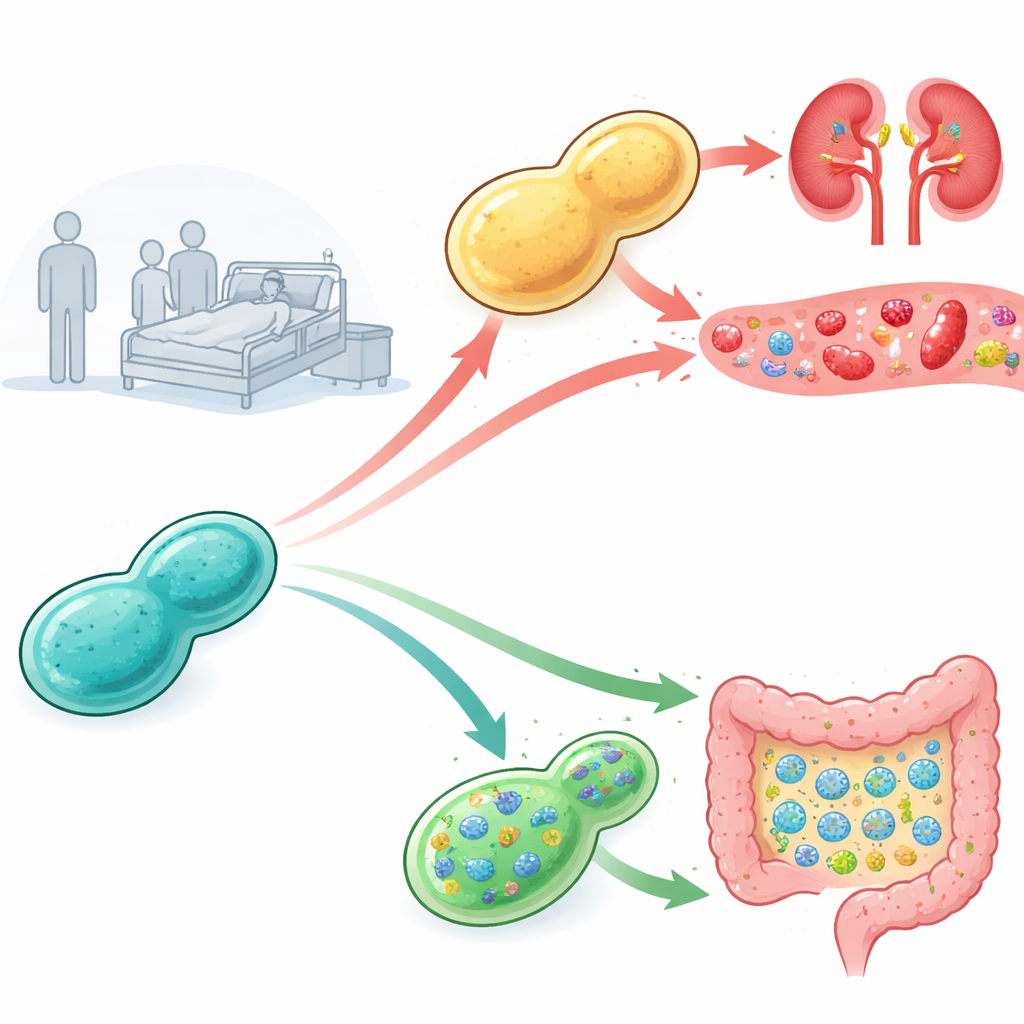
Suivre la virulence chez la souris
Les chercheurs ont prélevé la levure probiotique dans des produits commerciaux et chez des patients hospitalisés, puis ont évalué la dangerosité de chaque souche chez des souris immunodéprimées. Toutes les souris injectées avec des levures issues de produits commerciaux ont survécu, mais certaines levures d’origine clinique ont provoqué des taux de mortalité élevés et une forte prolifération fongique dans les reins, signe d’une infection sanguine sévère. Pour comprendre pourquoi, l’équipe a isolé de nombreuses sous‑lignées de la levure avant et après l’infection et les a soumises à différents stress sur milieux solides. Ils ont observé que les isolats plus virulents provenant des patients, et en particulier les versions ayant transité par les souris, présentaient une tolérance inhabituelle aux conditions salines contenant des sels de sodium ou de lithium, ce qui suggère que la capacité à résister à des environnements internes sévères pourrait être liée à leur potentiel pathogène.
Désarmer une pompe clé de survie
La tolérance au sel chez la levure dépend de transporteurs membranaires qui expulsent ou font entrer des ions dans la cellule. Les auteurs se sont concentrés sur deux gènes de ce type, ENA1 et NHA1, qui aident les cellules à survivre au stress salin et alcalin. À l’aide de l’édition génique CRISPR, ils ont supprimé chacun de ces gènes séparément dans six souches probiotiques différentes, incluant des isolats commerciaux et cliniques. Les résultats ont été frappants pour un gène : lorsque ENA1 était supprimé, toutes les souches testées causaient beaucoup moins de dommages chez la souris. Les animaux survivaient à l’infection sanguine à court terme et les niveaux fongiques dans les reins restaient relativement faibles, même lorsque la souche de départ était initialement très virulente. En revanche, la suppression de NHA1 n’a pas conféré un avantage de sécurité cohérent et a parfois rendu certaines souches plus dangereuses, soulignant combien l’effet d’une modification génétique dépend fortement du contexte génétique global.
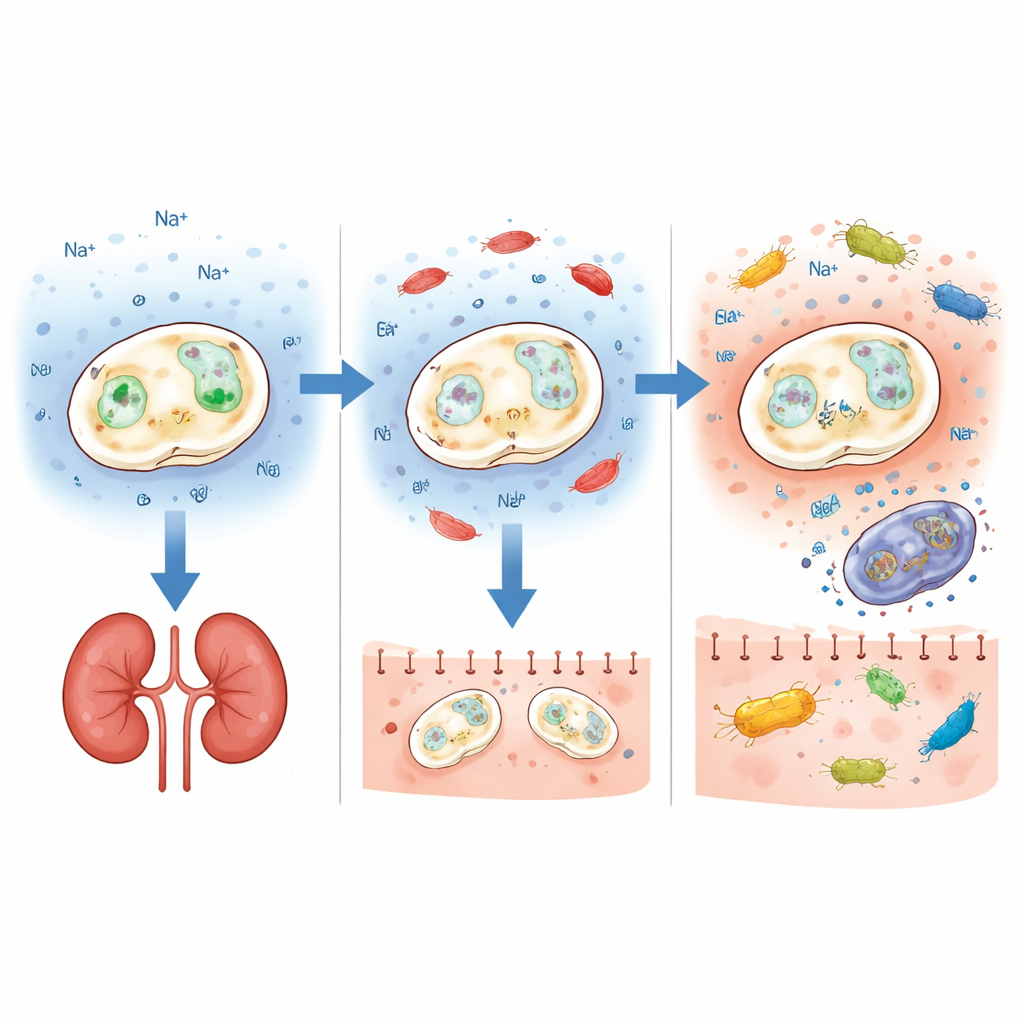
Conserver les bénéfices, ajouter une arme supplémentaire
Un probiotique plus sûr n’a d’intérêt que s’il conserve sa fonction dans l’intestin. L’équipe a donc vérifié si les souches déficientes en ENA1 pouvaient encore pousser correctement en milieux de culture standards et dans des conditions proches de l’intestin, incluant une acidité modérée, les sels biliaires et les pH rencontrés le long de l’intestin grêle et du côlon. Le mutant ENA1 se comportait beaucoup comme le probiotique d’origine, à l’exception d’une fragilité uniquement face à des conditions alcalines ou très salines exceptionnelles, peu représentatives d’un intestin sain. Chez des souris vivantes recevant des doses quotidiennes par voie orale, la levure modifiée colonisait l’intestin à des niveaux similaires à la souche commerciale et était éliminée à un rythme comparable après l’arrêt de l’administration. La souche altérée a également modifié la composition et la diversité de la communauté bactérienne intestinale de façon très proche de celle du probiotique original, suggérant que son impact global sur l’intestin est resté intact.
Construire une plate‑forme plus sûre pour des thérapies futures
Au‑delà de la sécurité, les auteurs ont montré ce qu’un probiotique « sur mesure » pourrait accomplir. Dans une étape de preuve de concept, ils ont remplacé le gène ENA1 par un ADN codant la Leucocine C, un court peptide antibactérien ciblant Listeria, un pathogène alimentaire sérieux. La levure modifiée a conservé une capacité fortement réduite à provoquer des infections sanguines chez la souris, poussait bien en laboratoire, supportait les procédures de lyophilisation utilisées en production commerciale et sécrétait un peptide actif qui inhibait Listeria en culture. Ensemble, ces résultats suggèrent que l’invalidation d’ENA1 crée une souche plateforme prometteuse : une levure beaucoup moins susceptible de provoquer une fongémie mortelle chez les patients fragiles, tout en conservant son comportement probiotique et pouvant être équipée pour lutter contre des bactéries nuisibles. En termes simples, l’étude démontre qu’il est possible de transformer un auxiliaire parfois risqué en un allié plus sûr et programmable pour de futures thérapies intestinales.
Citation: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
Mots-clés: levure probiotique, fongémie, édition de gènes, microbiome, probiotiques sur mesure