Clear Sky Science · es
La deficiencia de ENA1 atenúa la virulencia de la levadura probiótica Saccharomyces ‘boulardii’ en un modelo murino de fungemia en inmunosuprimidos
Por qué una levadura útil a veces puede volverse dañina
Mucha gente toma cápsulas de levadura probiótica para calmar el malestar intestinal o prevenir la diarrea durante el tratamiento con antibióticos. Una de las opciones más populares es una levadura que suele venderse bajo el nombre Saccharomyces boulardii. Aunque ayuda a muchos pacientes, los médicos detectan una tendencia preocupante: en algunas personas muy graves o con el sistema inmune debilitado, esta levadura amistosa puede desplazarse desde el intestino hasta el torrente sanguíneo y causar infecciones graves, a veces mortales. Este estudio plantea una pregunta urgente para la medicina moderna: ¿podemos rediseñar este probiótico para que conserve sus beneficios intestinales pero tenga mucha menos capacidad de provocar infecciones peligrosas en sangre?
Preocupación creciente en pacientes frágiles
Los hospitales de todo el mundo informan cada vez más casos en los que la levadura probiótica aparece en la sangre de pacientes en unidades de cuidados intensivos, tras cirugías o durante enfermedades graves. Estas personas suelen tener defensas debilitadas y dispositivos invasivos como catéteres, que ofrecen a los microbios nuevas puertas de entrada al organismo. En algunos centros, las infecciones vinculadas a esta levadura probiótica ocurren casi con la misma frecuencia que las provocadas por hongos patógenos clásicos. Sin embargo, hasta ahora la mayor parte de la investigación sobre esta levadura se ha centrado en sus beneficios para la salud o en formas de usarla como plataforma para producir fármacos, prestando poca atención a lo que realmente la convierte en un riesgo para pacientes vulnerables. Los autores se propusieron cerrar esa brecha estudiando sus aspectos beneficiosos y dañinos en el mismo proyecto.
Rastreando la virulencia en ratones
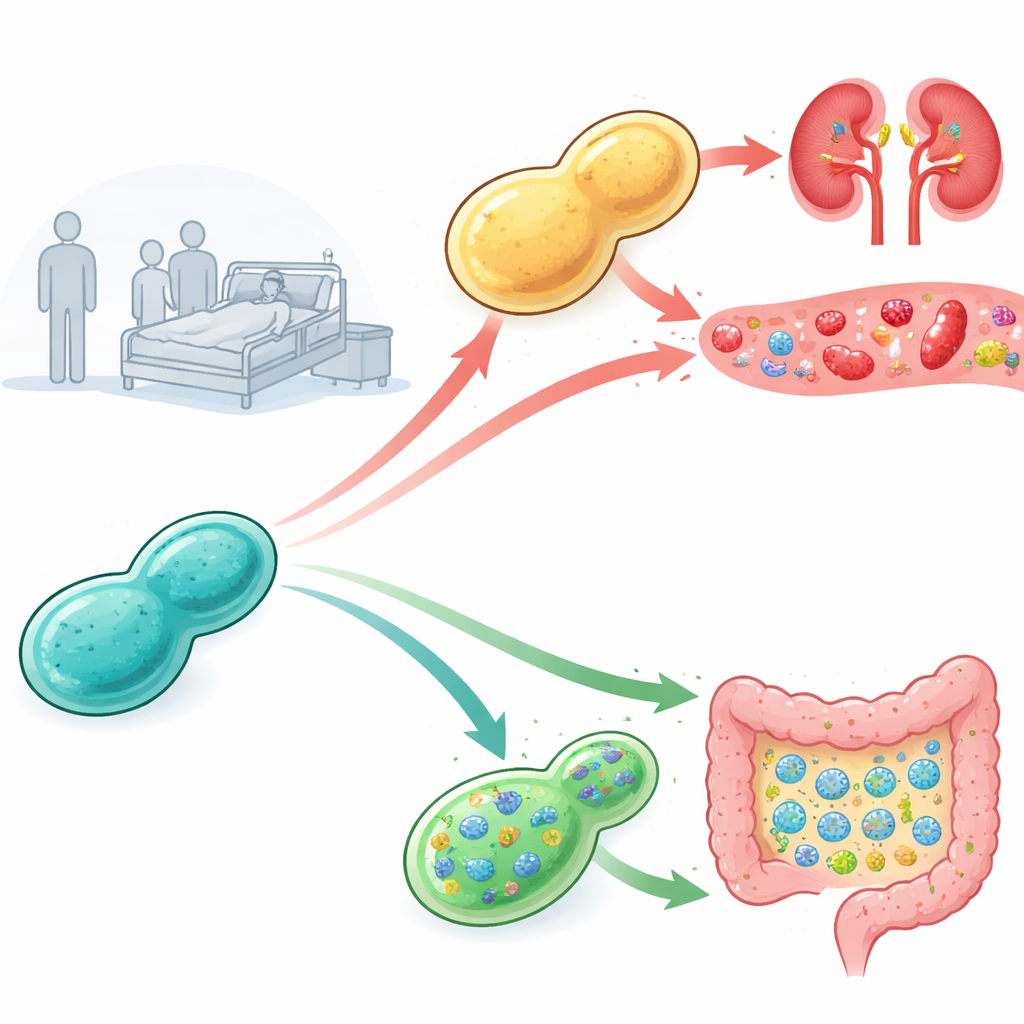
Los investigadores recogieron levaduras probióticas de productos comerciales y de pacientes hospitalizados y probaron cuán peligrosas eran en ratones con el sistema inmune debilitado. Todos los ratones inyectados con levaduras de productos comerciales sobrevivieron, pero algunas levaduras derivadas de pacientes causaron altas tasas de mortalidad y una fuerte proliferación fúngica en los riñones, indicio de infección sanguínea severa. Para entender por qué, el equipo aisló muchas sublínies de la levadura antes y después de la infección y las sometió a diferentes tensiones en placas de laboratorio. Observaron que los aislados clínicos más virulentos, y en especial las variantes que habían pasado por ratones, eran inusualmente tolerantes a condiciones salinas que contenían sales de sodio o litio, lo que sugiere que la capacidad de resistir ambientes internos adversos podría estar ligada a su potencial para causar enfermedad.
Desactivar una bomba clave de supervivencia
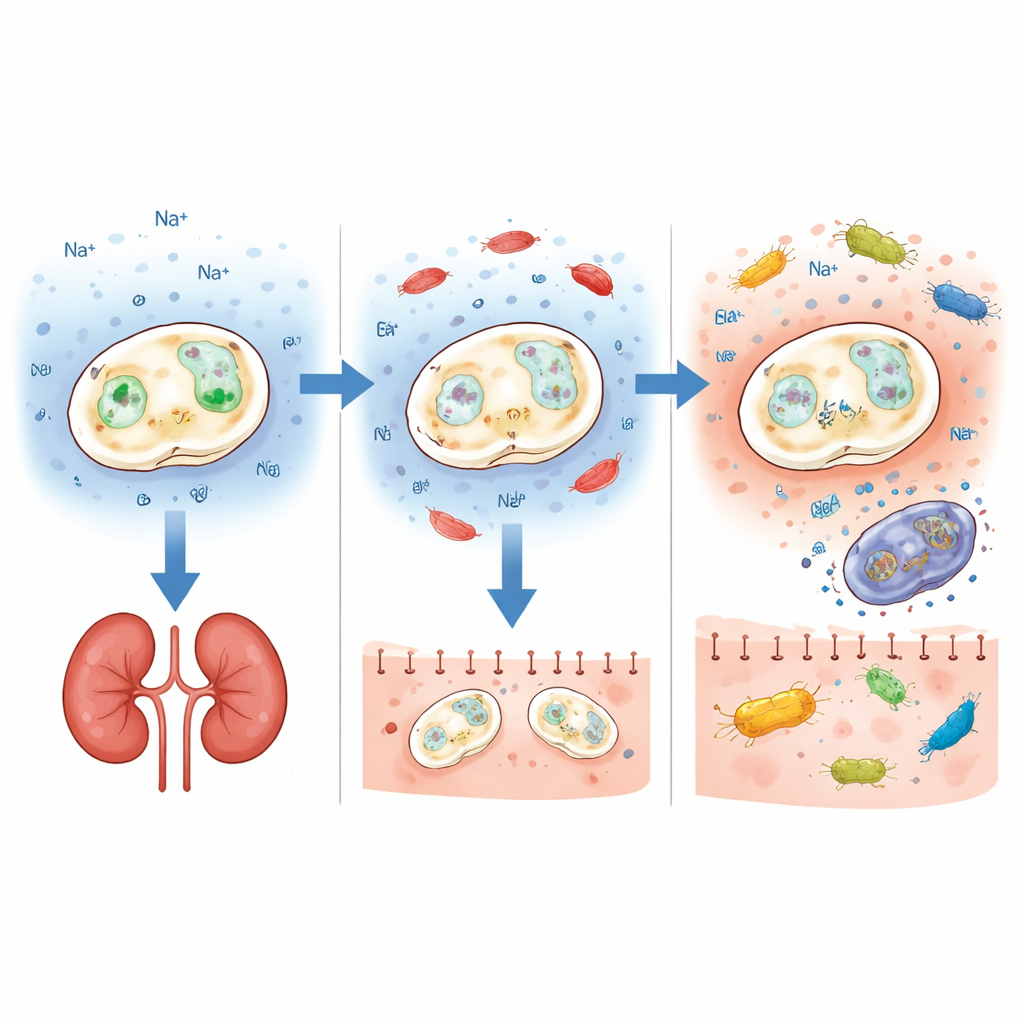
La tolerancia a la sal en levaduras depende de transportadores de membrana que expulsan o introducen iones en la célula. Los autores se centraron en dos genes de ese tipo, ENA1 y NHA1, que ayudan a las células a sobrevivir al estrés salino y alcalino. Empleando edición génica con CRISPR, eliminaron cada gen por separado en seis fondos probióticos distintos, incluidos aislamientos comerciales y clínicos. Los resultados fueron claramente concluyentes para un gen: cuando se eliminó ENA1, todas las cepas probadas causaron mucho menos daño en ratones. Todos los animales sobrevivieron a la infección sanguínea a corto plazo y los niveles fúngicos en los riñones se mantuvieron relativamente bajos, incluso cuando la cepa inicial era originalmente bastante virulenta. En contraste, la eliminación de NHA1 no aportó un beneficio de seguridad consistente y en ocasiones incluso hizo a las cepas más dañinas, lo que subraya cómo el efecto de un cambio genético puede depender fuertemente del contexto genético global.
Conservar los beneficios y añadir un arma adicional
Un probiótico más seguro solo es útil si sigue cumpliendo su función en el intestino. Por ello, el equipo comprobó si las cepas deficientes en ENA1 podían seguir creciendo bien en medios de cultivo estándar y en condiciones similares a las intestinales, incluida una acidez moderada, sales biliares y los niveles de pH propios del intestino delgado y grueso. El knockout de ENA1 se comportó de manera muy parecida al probiótico original, salvo que tuvo dificultades únicamente bajo condiciones altamente alcalinas o salinas, poco habituales en un intestino sano. En ratones vivos a los que se administraron dosis orales diarias, la levadura modificada colonizó el intestino a niveles similares a la cepa comercial y se eliminó a un ritmo comparable una vez interrumpida la administración. La cepa alterada también modificó la composición y la diversidad de la comunidad bacteriana intestinal de forma muy parecida al probiótico original, lo que sugiere que su impacto intestinal global se mantuvo intacto.
Construyendo una plataforma más segura para terapias futuras
Más allá de la seguridad, los autores mostraron lo que podría hacer un probiótico "diseñado". En un paso de prueba de concepto, reemplazaron el gen ENA1 por ADN que codifica Leucocin C, un péptido antibacteriano corto dirigido contra Listeria, un patógeno alimentario grave. La levadura modificada mostró aún una capacidad drásticamente reducida para causar infecciones sanguíneas en ratones, creció bien en pruebas de laboratorio, sobrevivió a procedimientos de liofilización usados en producción comercial y secretó un péptido activo que inhibió a Listeria en cultivo. En conjunto, estos resultados sugieren que la eliminación de ENA1 crea una cepa plataforma prometedora: una levadura con mucha menos probabilidad de causar fungemia potencialmente mortal en pacientes frágiles, que conserva su comportamiento probiótico y que puede equiparse para combatir bacterias dañinas. En términos sencillos, el estudio demuestra que es posible transformar a un ayudante a veces riesgoso en un aliado más seguro y programable para futuras terapias intestinales.
Cita: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
Palabras clave: levadura probiótica, fungemia, edición génica, microbioma, probióticos diseñados