Clear Sky Science · nl
ENA1‑tekort vermindert de virulentie van probioticumgist Saccharomyces ‘boulardii’ in een immunosuppressief muis‑fungaemie‑model
Waarom een behulpzame gist soms schadelijk kan worden
Veel mensen slikken probiotische gistpillen om een onrustige maag te kalmeren of diarree te voorkomen tijdens antibioticagebruik. Een van de populairste keuzes is een gist die vaak wordt verkocht onder de naam Saccharomyces boulardii. Hoewel deze veel patiënten helpt, zien artsen een verontrustende trend: bij sommige zeer zieke of immuungecompromitteerde mensen kan deze vriendelijke gist van de darm naar de bloedbaan migreren en ernstige, soms dodelijke, infecties veroorzaken. Deze studie stelt een dringende vraag voor de moderne geneeskunde: kunnen we dit probioticum zo herontwerpen dat het zijn darmvoordelen behoudt maar veel minder in staat is gevaarlijke bloedbaaninfecties te veroorzaken?
Opmarsende zorgen bij kwetsbare patiënten
Ziekenhuizen wereldwijd melden steeds vaker gevallen waarin de probioticumgist in het bloed van patiënten op de intensivecare, na een operatie of tijdens ernstige ziekte wordt aangetroffen. Deze mensen hebben vaak verzwakte afweer en invasieve hulpmiddelen zoals katheters, die microben nieuwe routes naar het lichaam geven. In sommige ziekenhuizen komen infecties die verband houden met deze probiotische gist bijna even vaak voor als die door klassieke ziekteverwekkende schimmels. Tot nu toe richtte onderzoek naar deze gist zich echter meestal op óf de gezondheidsvoordelen óf het gebruik ervan voor het produceren van geneesmiddelen, met weinig aandacht voor wat het risico voor kwetsbare patiënten veroorzaakt. De auteurs wilden deze kloof dichten door zowel de behulpzame als de schadelijke aspecten binnen hetzelfde project te bestuderen.
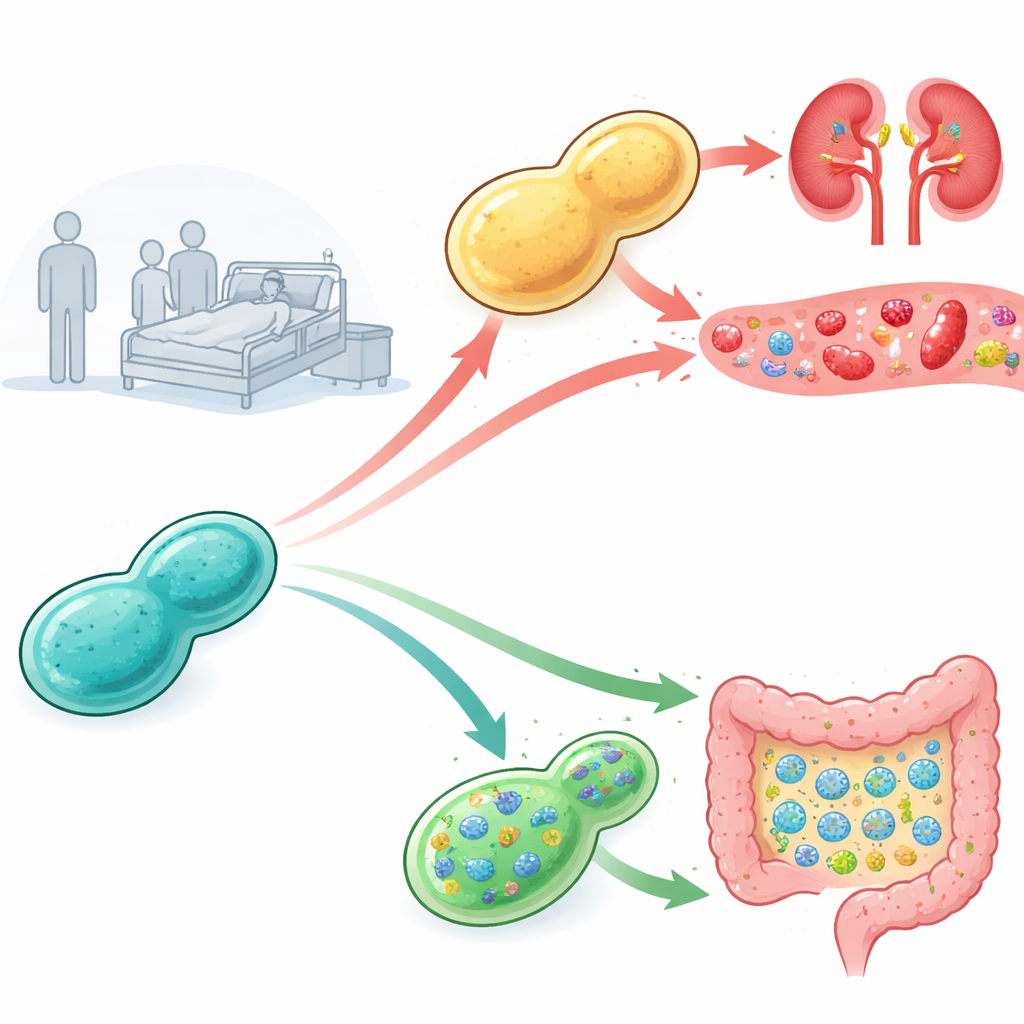
Virulentie volgen in muizen
De onderzoekers verzamelden probiotische giststammen uit commerciële producten en uit ziekenhuispatiënten en testten hoe gevaarlijk elk exemplaar was in muizen met een verzwakt immuunsysteem. Alle muizen die injecties met gist uit commerciële producten kregen overleefden, maar sommige stammen afkomstig van patiënten veroorzaakten hoge sterftecijfers en sterke schimmelgroei in de nieren, wat duidde op ernstige bloedbaaninfectie. Om te begrijpen waarom isoleerde het team vele sub‑lijnages van de gist vóór en na infectie en onderwierp ze aan verschillende stressvrachten op laboratoriumplaten. Ze merkten op dat de meer virulente patiëntisolaten, en vooral de varianten die door muizen waren gegaan, ongewoon tolerant waren voor zoute omstandigheden met natrium‑ of lithiummetalen, wat suggereert dat het vermogen om harde interne omstandigheden te weerstaan verband kan houden met hun ziekteverwekkende capaciteit.
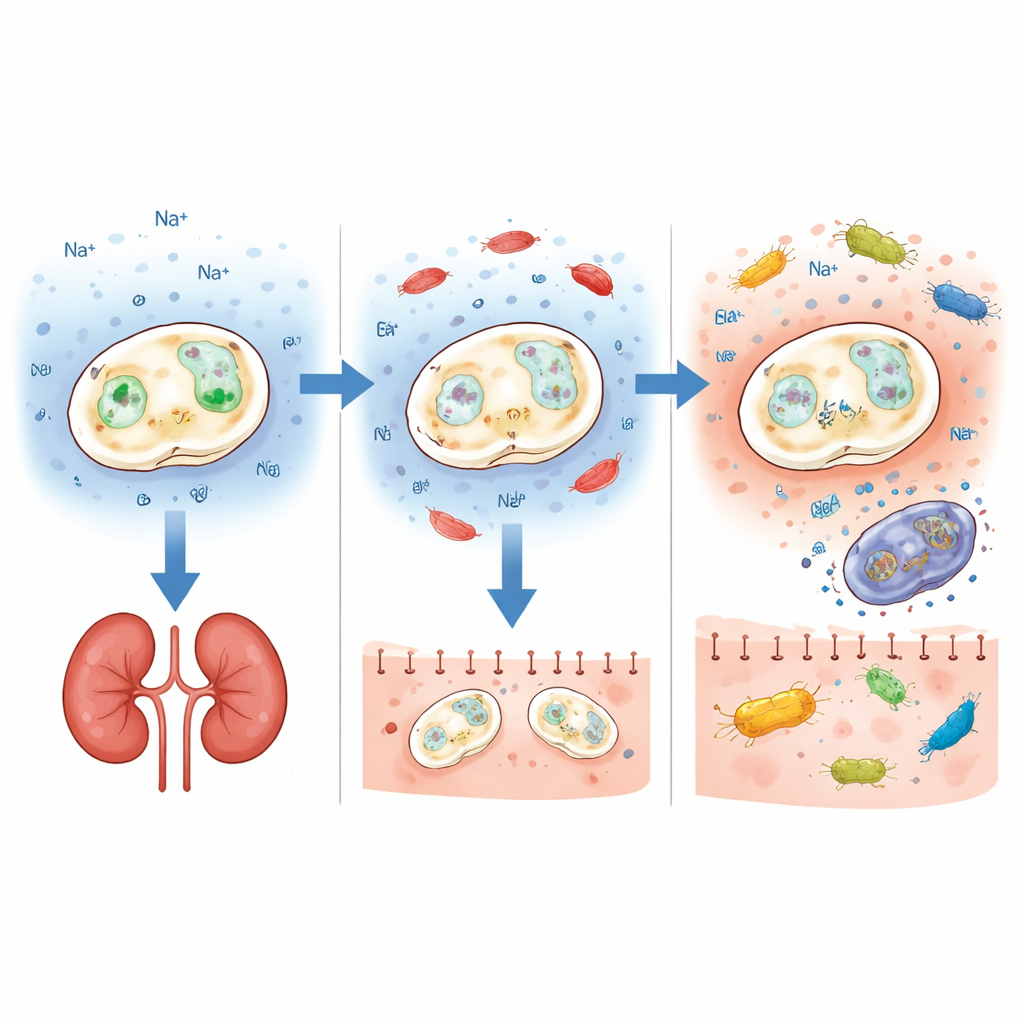
Een belangrijk overlevingspompsysteem ontwapenen
Zouttolerantie in gist hangt af van membraantransporteiwitten die ionen in en uit de cel pompen. De auteurs richtten zich op twee van zulke genen, ENA1 en NHA1, die cellen helpen zout‑ en alkalische stress te overleven. Met CRISPR‑genbewerking verwijderden ze elk gen afzonderlijk in zes verschillende probiotische achtergronden, waaronder commerciële en klinische isolaten. De resultaten waren overtuigend voor één gen: wanneer ENA1 werd verwijderd, veroorzaakte elke geteste stam veel minder schade in muizen. Alle dieren overleefden een kortdurende bloedbaaninfectie en de schimmelbelasting in de nieren bleef relatief laag, zelfs wanneer de oorspronkelijke stam redelijk virulent was. Het verwijderen van NHA1 gaf daarentegen geen consistent veiligheidsvoordeel en maakte sommige stammen zelfs schadelijker, wat onderstreept hoe de impact van een genetische wijziging sterk kan afhangen van de bredere genetische achtergrond.
De voordelen behouden, met een extra wapen
Een veiliger probiotica is alleen nuttig als het nog steeds zijn bedoelde werk in de darm doet. Het team controleerde daarom of ENA1‑deficiënte stammen nog goed konden groeien in standaard kweekmedia en onder darmachtige omstandigheden, waaronder matige zuurgraad, galzouten en de pH‑waarden die voorkomen in de dunne en dikke darm. De ENA1‑knockout gedroeg zich grotendeels als het oorspronkelijke probioticum, behalve dat het moeite had onder uitzonderlijk hoge alkalische of zoute condities die niet typisch zijn voor een gezonde darm. In levende muizen die dagelijks orale doses kregen, koloniseerde de gewijzigde gist de darm tot vergelijkbare niveaus als de commerciële stam en werd op vergelijkbare wijze gewist zodra de toediening stopte. De gewijzigde stam verschuift ook de samenstelling en diversiteit van de darmbacteriële gemeenschap op ongeveer dezelfde manier als het originele probioticum, wat suggereert dat de algemene impact op de darm intact bleef.
Een veiliger platform voor toekomstige therapieën bouwen
Buiten de veiligheid toonden de auteurs ook wat een "ontworpen" probioticum kan doen. In een proof‑of‑concept stap vervingen ze het ENA1‑gen door DNA dat Leucocin C codeert, een kort antibacterieel peptide gericht tegen Listeria, een ernstige voedselovergedragen pathogeen. De gemodificeerde gist toonde nog steeds sterk verminderde capaciteit om bloedbaaninfecties bij muizen te veroorzaken, groeide goed in laboratoriumtests, overleefde vriesdroogprocedures die in commerciële productie worden gebruikt en scheidde een actief peptide uit dat Listeria in kweek remde. Samengevat suggereren deze resultaten dat het uitschakelen van ENA1 een veelbelovende platformstam creëert: een gist die veel minder waarschijnlijk levensbedreigende fungaemie veroorzaakt bij kwetsbare patiënten, maar toch zijn probiotische gedrag behoudt en verder kan worden uitgerust om schadelijke bacteriën te bestrijden. In eenvoudige bewoordingen laat de studie zien dat het mogelijk is een soms risicovolle helper om te vormen tot een veiliger, programmeerbaar bondgenoot voor toekomstige darmgerichte therapieën.
Bronvermelding: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
Trefwoorden: probioticumgist, fungaemie, genbewerking, microbioom, ontworpen probiotica