Clear Sky Science · de
ENA1-Mangel verringert die Virulenz der Probiotikahefe Saccharomyces ‚boulardii‘ im Fungaemie‑Modell immunsupprimierter Mäuse
Warum eine nützliche Hefe manchmal schädlich werden kann
Viele Menschen nehmen probiotische Hefepillen ein, um einen gereizten Darm zu beruhigen oder Durchfall während einer Antibiotikabehandlung zu verhindern. Eine der beliebtesten Optionen ist eine Hefe, die häufig unter dem Namen Saccharomyces boulardii verkauft wird. Obwohl sie vielen Patientinnen und Patienten hilft, beobachten Ärztinnen und Ärzte einen besorgniserregenden Trend: Bei sehr kranken oder immungeschwächten Personen kann diese freundliche Hefe aus dem Darm ins Blut übertreten und schwere, teils tödliche Infektionen verursachen. Diese Studie stellt eine drängende Frage für die moderne Medizin: Können wir dieses Probiotikum so umgestalten, dass es seine Nutzen im Darm behält, aber deutlich weniger in der Lage ist, gefährliche Blutbahninfektionen zu verursachen?
Zunehmende Sorge bei besonders anfälligen Patientengruppen
Krankenhäuser weltweit melden zunehmend Fälle, in denen die probiotische Hefe im Blut von Patientinnen und Patienten auf Intensivstationen, nach Operationen oder bei schweren Erkrankungen nachgewiesen wird. Diese Personen haben oft geschwächte Abwehrkräfte und invasive Hilfsgeräte wie Katheter, die Mikroben neue Eintrittspforten in den Körper eröffnen. In einigen Kliniken treten Infektionen mit dieser Probiotikahefe fast so häufig auf wie die durch klassische krankheitsverursachende Pilze. Bislang richtete sich die meiste Forschung an dieser Hefe entweder auf ihre gesundheitlichen Vorteile oder auf Möglichkeiten, sie gentechnisch zur Arzneimittelproduktion zu nutzen; wenig Aufmerksamkeit galt bislang den Faktoren, die sie für verletzliche Patientinnen und Patienten riskant machen. Die Autorinnen und Autoren wollten diese Lücke schließen, indem sie beide Seiten — den nützlichen und den schädlichen — im selben Projekt untersuchten.
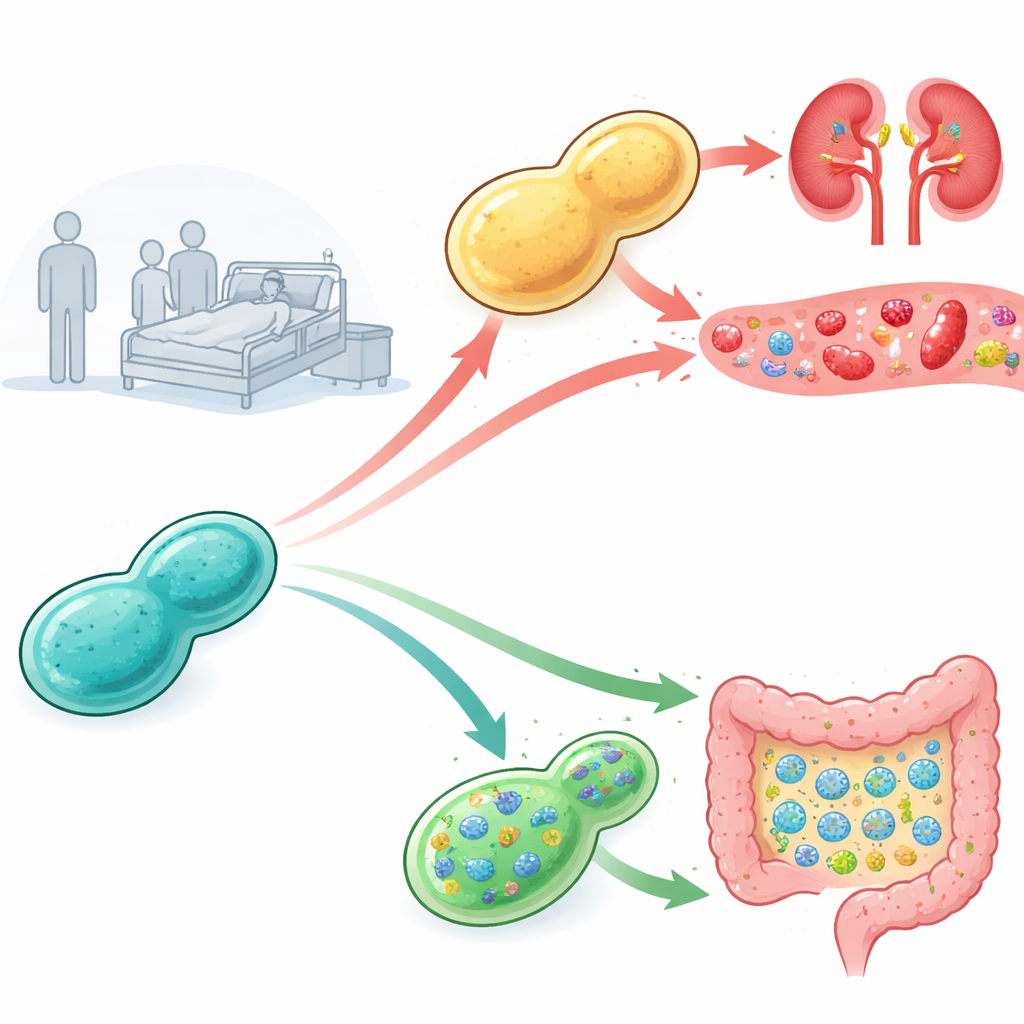
Die Virulenz im Inneren von Mäusen verfolgen
Die Forschenden sammelten probiotische Hefen aus Handelsprodukten und von Krankenhauspatientinnen und -patienten und prüften, wie gefährlich jede einzelne in immunsupprimierten Mäusen war. Alle Mäuse, die mit Hefen aus Handelspräparaten injiziert wurden, überlebten, doch einige aus Patientenproben isolierte Stämme führten zu hohen Sterberaten und starker Pilzwachstumsbelastung in den Nieren — ein Zeichen schwerer Blutbahninfektionen. Um den Gründen dafür nachzugehen, isolierte das Team zahlreiche Sublinien der Hefe vor und nach der Infektion und setzte sie in Plattenversuchen unterschiedlichen Stressbedingungen aus. Sie bemerkten, dass die virulenteren Patientenisolate, und besonders die Varianten, die zuvor Mäuse passiert hatten, ungewöhnlich tolerant gegenüber salzhaltigen Bedingungen mit Natrium‑ oder Lithiumsalzen waren. Dieser Befund deutet darauf hin, dass die Fähigkeit, harsche innere Umgebungen zu überstehen, mit ihrem Krankheitspotenzial verknüpft sein könnte.
Eine wichtige Überlebenspumpe entwaffnen
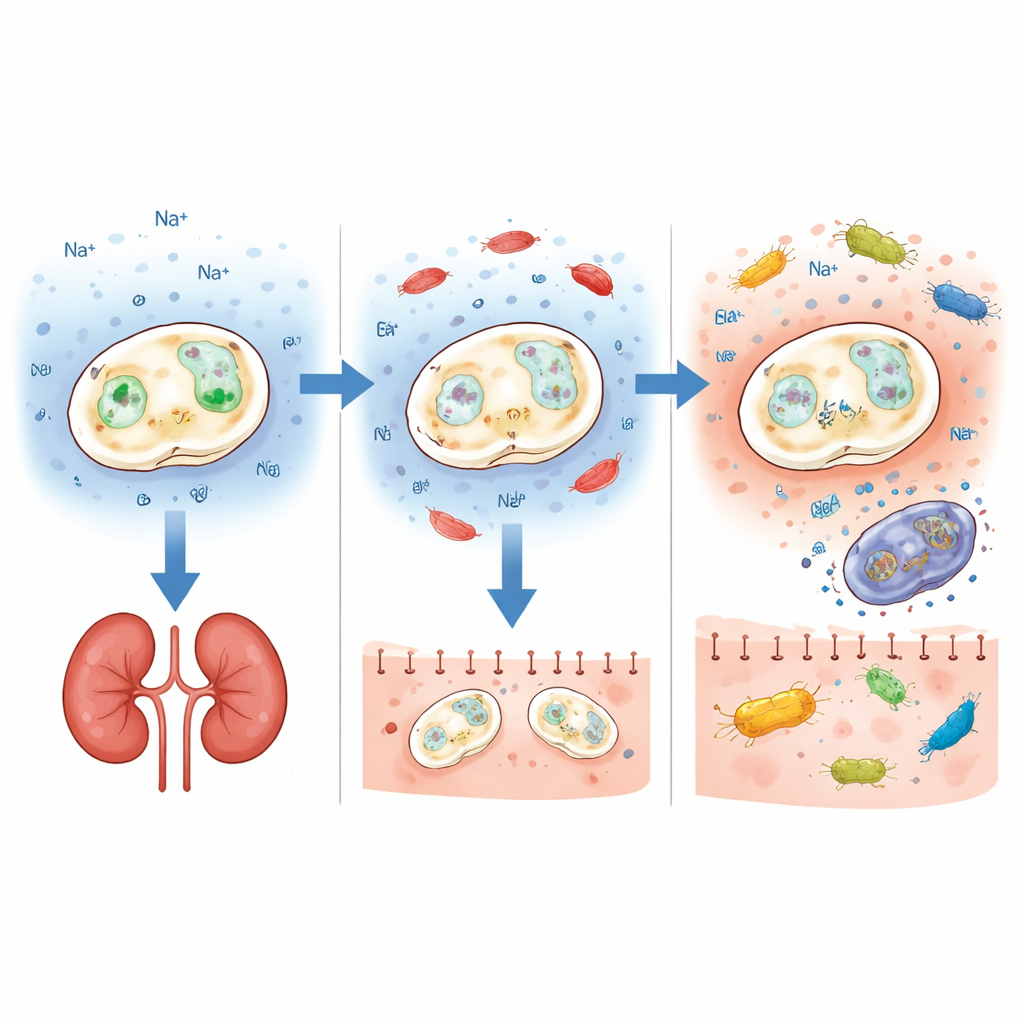
Salztoleranz bei Hefen beruht auf Membrantransportern, die Ionen in die Zelle hinein und aus ihr heraus pumpen. Die Autorinnen und Autoren konzentrierten sich auf zwei solche Gene, ENA1 und NHA1, die den Zellen helfen, Salz‑ und alkalischen Stress zu überstehen. Mit CRISPR‑Geneditierung löschten sie jedes Gen separat in sechs verschiedenen Probiotika‑Hintergründen, darunter kommerzielle und klinische Isolate. Die Ergebnisse waren für ein Gen auffallend klar: Nach Entfernung von ENA1 verursachte jeder getestete Stamm deutlich weniger Schaden in Mäusen. Alle Tiere überlebten die kurzfristige Blutbahninfektion, und die Pilzlast in den Nieren blieb vergleichsweise niedrig, selbst wenn der Ausgangsstamm ursprünglich recht virulent gewesen war. Im Gegensatz dazu brachte die Deletion von NHA1 keinen konsistenten Sicherheitsvorteil und machte manche Stämme sogar gefährlicher — ein Hinweis darauf, dass die Wirkung einer genetischen Veränderung stark vom übrigen genetischen Hintergrund abhängen kann.
Die Vorteile behalten, eine zusätzliche Waffe hinzufügen
Ein sichereres Probiotikum ist nur sinnvoll, wenn es seine beabsichtigte Funktion im Darm weiterhin erfüllt. Das Team prüfte daher, ob ENA1‑defiziente Stämme nach wie vor gut in Standardnährmedien und unter darmähnlichen Bedingungen wachsen können, einschließlich mäßiger Säure, Gallensalzen und der pH‑Werte entlang des Dünn‑ und Dickdarms. Der ENA1‑Knockout verhielt sich weitgehend wie das ursprüngliche Probiotikum; er hatte nur unter ungewöhnlich stark alkalischen oder salzhaltigen Bedingungen Schwierigkeiten, wie sie im gesunden Darm nicht typisch sind. In lebenden Mäusen, die täglich Dosen oral erhielten, kolonisierte die veränderte Hefe den Darm in ähnlicher Höhe wie der kommerzielle Stamm und wurde nach Absetzen der Gabe in ähnlichem Tempo eliminiert. Der veränderte Stamm veränderte zudem Zusammensetzung und Diversität der bakteriellen Darmgemeinschaft in sehr ähnlicher Weise wie das ursprüngliche Probiotikum, was darauf hindeutet, dass seine Gesamtwirkung im Darm erhalten blieb.
Eine sicherere Plattform für künftige Therapien bauen
Über die Sicherheit hinaus zeigten die Autorinnen und Autoren, was ein „Designer“‑Probiotikum leisten könnte. In einem Proof‑of‑Concept‑Schritt ersetzten sie das ENA1‑Gen durch DNA, die Leucocin C codiert — ein kurzes antibakterielles Peptid, das gegen Listeria, einen schweren lebensmittelbedingten Erreger, gerichtet ist. Die gentechnisch veränderte Hefe zeigte weiterhin eine drastisch verringerte Fähigkeit, Blutbahninfektionen in Mäusen zu verursachen, wuchs gut in Labortests, überstand Gefriertrocknungsverfahren, die in der kommerziellen Produktion verwendet werden, und sezernierte ein aktives Peptid, das Listeria in Kultur hemmte. Zusammengenommen deuten diese Ergebnisse darauf hin, dass das Ausschalten von ENA1 eine vielversprechende Plattformlinie schafft: eine Hefe, die deutlich weniger wahrscheinlich lebensbedrohliche Fungaemien bei verletzlichen Patientinnen und Patienten verursacht, dennoch ihr probiotisches Verhalten beibehält und sich zusätzlich dazu einsetzen lässt, schädliche Bakterien zu bekämpfen. Einfach gesagt demonstriert die Studie, dass es möglich ist, einen mitunter riskanten Helfer in einen sichereren, programmierbaren Verbündeten für künftige darmbasierte Therapien zu verwandeln.
Zitation: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
Schlüsselwörter: probiotische Hefe, Fungaemie, Genbearbeitung, Mikrobiom, Designer‑Probiotika