Clear Sky Science · ja
ENA1欠損は免疫抑制マウスの菌血症モデルにおけるSaccharomyces ‘boulardii’プロバイオティクス酵母の病原性を低下させる
なぜ有益な酵母が時に有害になるのか
多くの人が、胃腸の不調を和らげたり抗生物質治療中の下痢を防いだりするためにプロバイオティクスの酵母サプリを服用します。最も人気のある選択肢の一つが、しばしばSaccharomyces boulardiiの名で販売されている酵母です。多くの患者に利益をもたらす一方で、医師たちは憂慮すべき傾向を観察しています:非常に病状が重い、あるいは免疫が弱っている一部の人では、この“良い”酵母が腸から血流へと移行し、深刻で時に致命的な感染を引き起こすことがあるのです。本研究は現代医療にとって差し迫った問いを投げかけます:このプロバイオティクスを再設計して腸内での有益な作用を保ちながら、血流感染を引き起こす能力を大幅に低下させることは可能か?
脆弱な患者で高まる懸念
世界中の病院で、集中治療室や術後、重篤な病状時にプロバイオティクス酵母が患者の血液中から検出される事例が増えています。これらの患者は防御機構が弱く、カテーテルのような侵襲的デバイスを使っていることが多く、微生物が体内に入る新たな経路を提供します。一部の病院では、このプロバイオティクス酵母に関連する感染は従来の病原真菌による感染とほぼ同頻度で発生しています。しかしこれまで、この酵母に関する研究は主にその健康効果や薬剤生産のための工学的応用に偏っており、脆弱な患者にとってどのような要因がリスクになっているかにはほとんど注意が払われてきませんでした。著者らは、有益性と有害性の双方を同じプロジェクトで調べることで、このギャップを埋めようとしました。
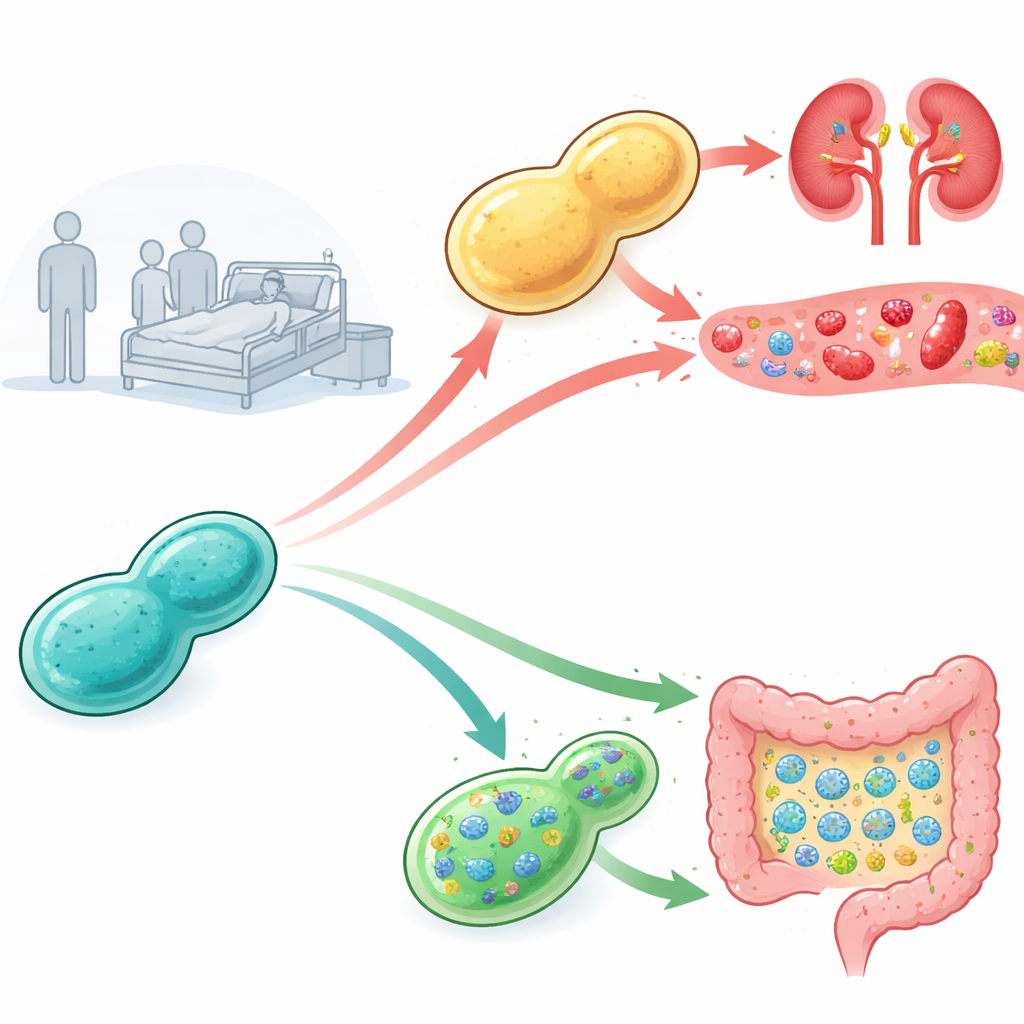
マウス内での病原性の追跡
研究者たちは市販製品および病院由来のプロバイオティクス酵母を収集し、免疫が抑えられたマウスでそれぞれがどれほど危険かを試験しました。市販製品由来の酵母を注射されたマウスは全て生存しましたが、一部の患者由来分離株は高い死亡率と腎臓での著しい真菌増殖を引き起こし、深刻な菌血症の徴候を示しました。なぜそうなるのかを探るために、チームは感染の前後で多くの亜系統を単離し、実験プレート上でさまざまなストレスにさらしました。より高い病原性を示した患者分離株、特にマウスを経由した系統は、ナトリウムやリチウム塩を含む高塩条件に異常に耐性があることに気づき、過酷な体内環境への耐性が病原性に結びついている可能性が示唆されました。
重要な生存ポンプの無力化
酵母の塩耐性は、イオンを細胞外へ送り出したり取り込んだりする膜輸送体に依存します。著者らはENA1とNHA1という二つの遺伝子に注目しました。これらは塩やアルカリストレスを克服するのに役立ちます。CRISPR遺伝子編集を用いて、市販株と臨床分離株を含む6つの異なるプロバイオティクス背景で各遺伝子を個別に欠失させました。結果は一方の遺伝子について非常に明確でした:ENA1を取り除くと、試験された全ての株でマウスへの害が著しく減少しました。短期の菌血症では全ての動物が生存し、腎臓中の真菌量も比較的低く保たれ、元々かなり病原性の高かった株であっても同様でした。対照的にNHA1の欠失は一貫した安全性向上をもたらさず、場合によっては株をより有害にすることさえあり、遺伝子変化の影響が広い遺伝的背景に強く依存することを強調しました。
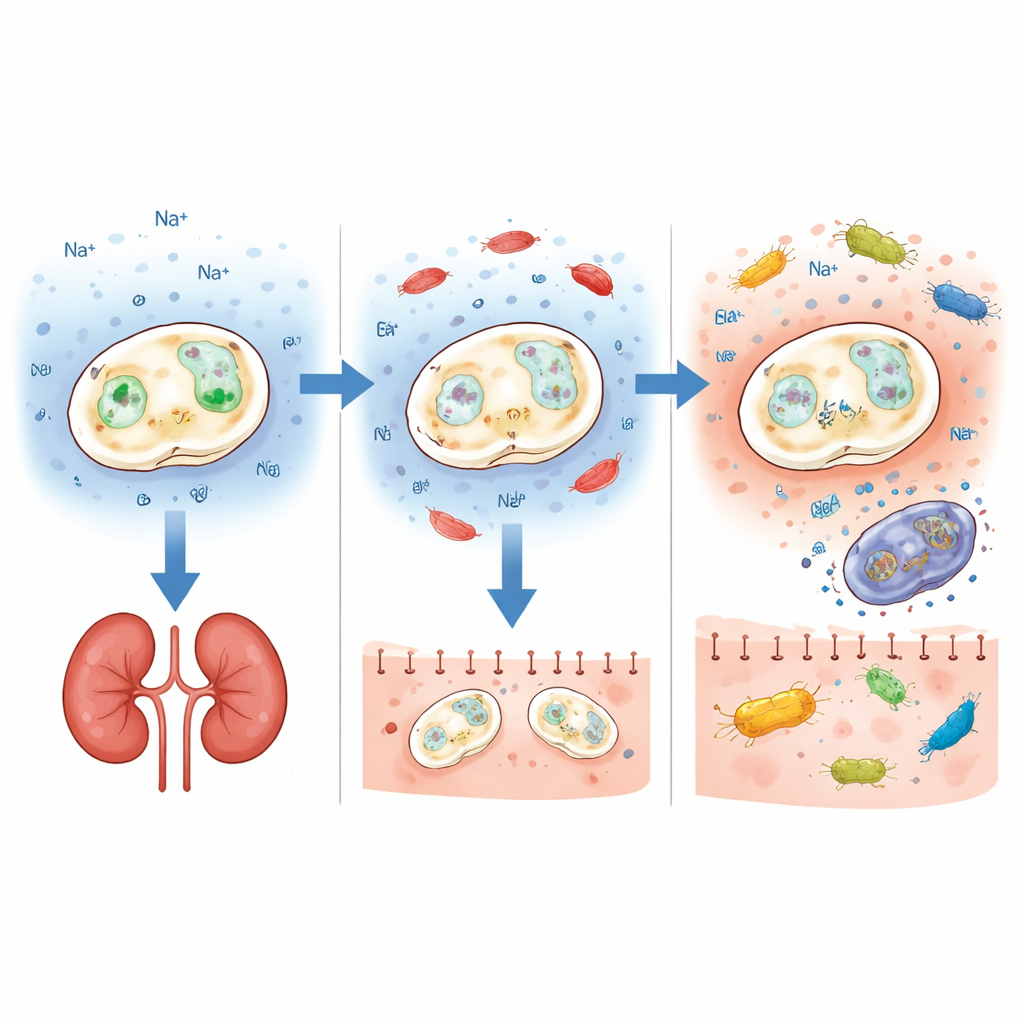
利益を保ちつつ付加的な武器を追加
より安全なプロバイオティクスは、腸内での本来の働きを維持できて初めて有用です。そこでチームはENA1欠損株が標準的な培地や腸様条件、すなわち中程度の酸性、胆汁塩、回腸や大腸に見られるpHレベル下で十分に増殖できるかを確認しました。ENA1ノックアウト株は元のプロバイオティクスとほぼ同様に振る舞い、ただし健康な腸では典型的でない非常に高いアルカリ性や高塩条件の下でのみ生育が困難でした。生きたマウスに経口で毎日投与した場合、改変酵母は市販株と同程度に腸内をコロナイズし、投与停止後の排除も同じ速度で進みました。改変株は腸内細菌コミュニティの組成や多様性に与える影響も元のプロバイオティクスと大差なく、全体として腸内での効果は維持されていることを示唆しました。
将来の治療のためのより安全なプラットフォームの構築
安全性に加え、著者らは「デザイナープロバイオティクス」が何を成し得るかを示しました。概念実証として、彼らはENA1遺伝子をリステリアという深刻な食中毒病原体を標的とする短い抗菌ペプチド、ロイコシンCをコードするDNAに置き換えました。改変された酵母は依然としてマウスでの菌血症を引き起こす能力が大幅に低下し、実験室試験でも良好に増殖し、市販生産で用いられる凍結乾燥手順にも耐え、リステリアを培養で抑制する活性ペプチドを分泌しました。これらを総合すると、ENA1の欠失は有望なプラットフォーム株を生み出すことを示唆しています:脆弱な患者で致命的となり得る菌血症を起こしにくく、それでいてプロバイオティクスとしての挙動を保ち、有害な細菌と戦うための追加装備が可能な酵母です。簡潔に言えば、本研究は時にリスクを伴う“助っ人”を、より安全でプログラム可能な腸内療法の味方へと変えることが可能であることを示しています。
引用: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
キーワード: プロバイオティクス酵母, 菌血症, 遺伝子編集, マイクロバイオーム, デザイナープロバイオティクス