Clear Sky Science · tr
ENA1 eksikliği, immünsüpresif fare fungemi modeliyle Saccharomyces ‘boulardii’ probiyotik mayasının virülansını azaltır
Neden Yardımcı Bir Maya Bazen Zararlı Hale Gelir
Birçok insan, mide rahatsızlığını hafifletmek veya antibiyotik tedavisi sırasında ishalin önüne geçmek için probiyotik maya kapsülleri alır. En popüler seçeneklerden biri sıklıkla Saccharomyces boulardii adıyla satılan bir mayadır. Birçok hastaya yardımcı olmasına karşın doktorlar endişe verici bir eğilim görüyor: çok hasta veya bağışıklığı baskılanmış bazı kişilerde bu dost maya bağırsaktan kana geçip ciddi, bazen öldürücü enfeksiyonlara yol açabiliyor. Bu çalışma modern tıp için acil bir soruyu gündeme getiriyor: bu probiyotiği bağırsaktaki faydalarını koruyacak ancak kan dolaşımında tehlikeli enfeksiyon yapma yeteneğini önemli ölçüde azaltacak şekilde yeniden tasarlayabilir miyiz?
Kırılgan Hastalardaki Artan Endişeler
Dünyanın birçok hastanesinde, probiyotik mayanın yoğun bakım ünitelerindeki, ameliyat sonrası veya şiddetli hastalık sırasında kan örneklerinde görüldüğü vakalar giderek daha sık bildiriliyor. Bu kişiler genellikle zayıflamış savunma mekanizmalarına sahip ve kateter gibi invaziv cihazlar mikroplara vücuda yeni geçiş yolları sağlıyor. Bazı hastanelerde bu probiyotik maya ile ilişkili enfeksiyonlar, klasik hastalık yapıcı mantarlardan kaynaklanan enfeksiyonlar kadar sık görülüyor. Ancak şimdiye kadar bu mayaya dair araştırmaların çoğu ya sağlık yararlarına ya da ilaç üretmek üzere gen mühendisliğine odaklandı; kırılgan hastalar için neden risk oluşturduğuna ise az dikkat verildi. Yazarlar, aynı projede hem faydalı hem de zararlı yönlerini inceleyerek bu boşluğu doldurmayı amaçladılar.
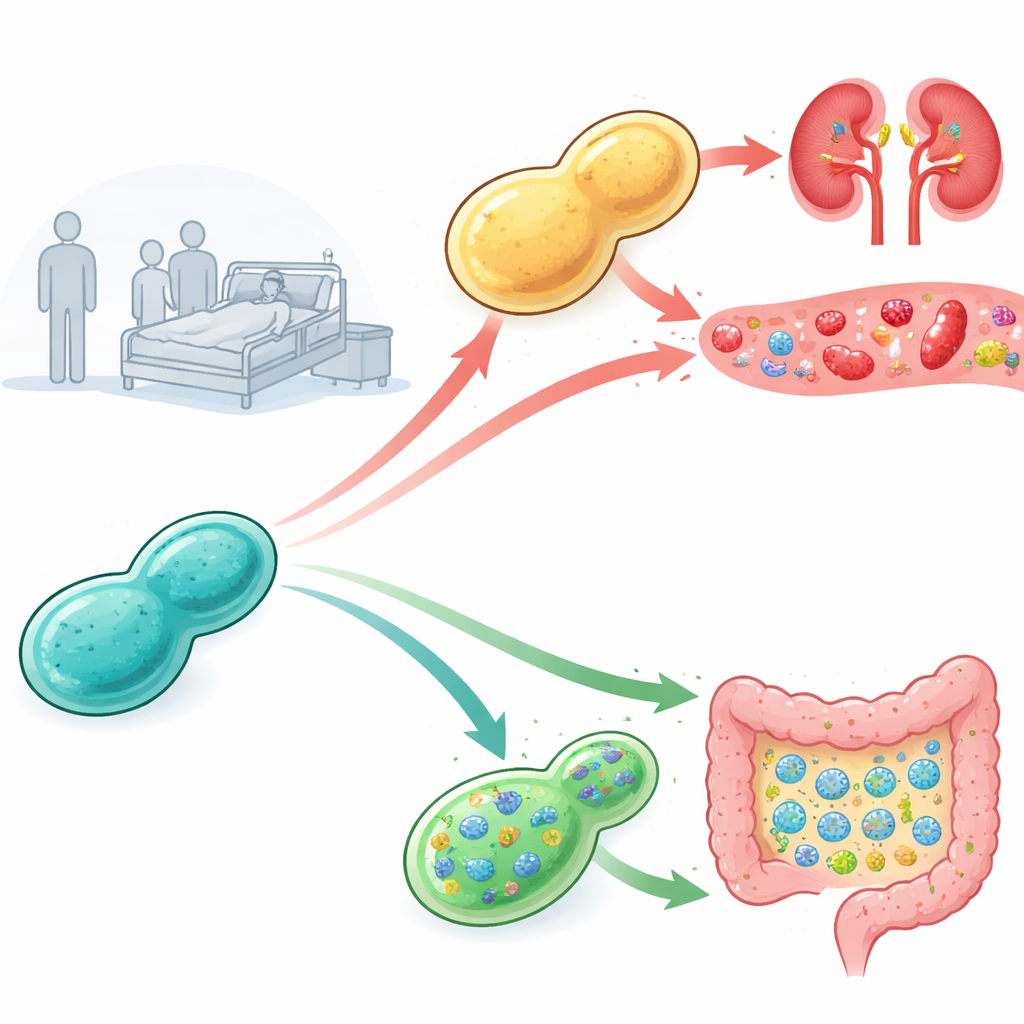
Fare İçinde Virülansı İzlemek
Araştırmacılar, ticari ürünlerden ve hastanede izole edilen hasta örneklerinden probiyotik mayalar topladı ve her birinin bağışıklığı zayıflatılmış farelerde ne kadar tehlikeli olduğunu test etti. Ticari ürünlerden izole edilen mayalarla enjeksiyon yapılan tüm fareler sağ kalırken, bazı hasta kaynaklı izolatlar yüksek ölüm oranlarına ve böbreklerde yoğun mantar büyümesine yol açtı; bu, ciddi kan dolaşımı enfeksiyonunun bir göstergesiydi. Nedenlerini anlamak için ekip, enfeksiyondan önce ve sonra mayanın birçok alt-lezonunu izole etti ve bunları laboratuvar plakalarında farklı stres koşullarında zorladı. Daha virülent olan hasta izolatlarının ve özellikle farelerden geçmiş olan versiyonların sodyum veya lityum tuzları içeren tuzlu koşullara olağandışı derecede dayanıklı olduğunu fark ettiler; bu, sert iç ortam koşullarına dayanabilme yeteneğinin hastalık yapma kapasitesiyle ilişkili olabileceğine işaret ediyordu.
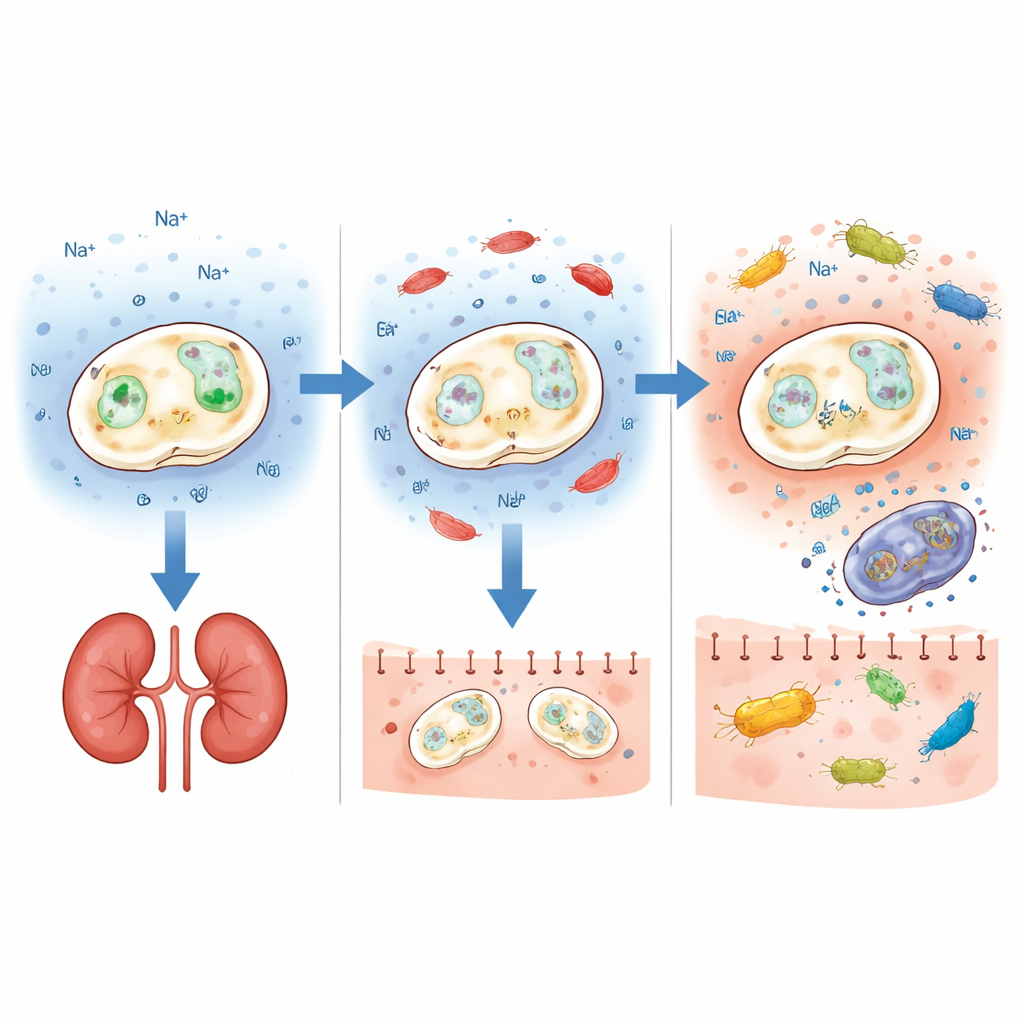
Ana Bir Korunma Pompasını Devre Dışı Bırakmak
Meydandaki tuz toleransı, iyonları hücre içine ve dışına pompalayan membran taşıyıcılarına bağlıdır. Yazarlar, hücrelerin tuz ve alkalin stresine dayanmasına yardımcı olan ENA1 ve NHA1 adlı iki gene odaklandı. CRISPR gen düzenleme kullanarak, ticari ve klinik izolatlar dahil olmak üzere altı farklı probiyotik arka planda her geni ayrı ayrı sildiler. Sonuçlar özellikle bir gen için çarpıcı derecede netti: ENA1 kaldırıldığında, test edilen her suş farelerde çok daha az zarar veriyordu. Tüm hayvanlar kısa süreli kan dolaşımı enfeksiyonunda sağ kaldı ve böbreklerdeki mantar seviyeleri nispeten düşük kaldı; başlangıçta oldukça virülent olan suşlarda bile bu gözlendi. Buna karşın NHA1'in silinmesi tutarlı bir güvenlik faydası sağlamadı ve bazen suşları daha zararlı hale getirdi; bu da genetik bir değişikliğin etkisinin geniş genetik arka plana güçlü biçimde bağlı olabileceğini vurguluyor.
Faydaları Koruyup Ekstra Bir Silah Eklemek
Daha güvenli bir probiyotik yalnızca bağırsaktaki amacını yerine getirebiliyorsa kullanışlıdır. Bu nedenle ekip, ENA1 eksik suşların standart besiyerlerinde ve bağırsak benzeri koşullar altında—orta dereceli asidite, safra tuzları ve ince ile kalın bağırsakta bulunan pH seviyeleri dahil—iyi büyüyüp büyümediğini kontrol etti. ENA1 yokluğu, özgün probiyotikle büyük ölçüde benzer davrandı; yalnızca sağlıklı bağırsakta tipik olmayan olağanüstü yüksek alkalin veya tuzlu koşullarda zorlandı. Ağız yoluyla günlük doz verilen canlı farelerde, modifiye maya ticari suşla benzer düzeylerde bağırsakları kolonize etti ve doz kesildikten sonra benzer hızda temizlendi. Değiştirilmiş suş ayrıca bağırsak bakteri topluluğunun bileşimini ve çeşitliliğini özgün probiyotiğin yaptığı şekilde benzer biçimde değiştirdi; bu, genel bağırsak etkisinin korunduğunu gösteriyor.
Gelecek Tedaviler İçin Daha Güvenli Bir Platform İnşa Etmek
Güvenliğin ötesinde, yazarlar bir “tasarımcı” probiyotiğin neler yapabileceğini de gösterdi. Kavram kanıtı niteliğindeki bir adımda, ENA1 geninin yerine Listeria gibi ciddi gıda kaynaklı patojenlere karşı hedefli kısa bir antibakteriyel peptid olan Leucocin C’yi kodlayan DNA yerleştirildi. Genetiği değiştirilmiş maya farelerde hâlâ kan dolaşımı enfeksiyonu yapma yeteneğinde büyük azalma gösterdi, laboratuvar testlerinde iyi büyüdü, ticari üretimde kullanılan dondurarak kurutma işlemlerine dayanabildi ve kültürde Listeria’yı inhibe eden aktif bir peptid salgıladı. Bir arada değerlendirildiğinde, bu sonuçlar ENA1’in yok edilmesinin umut verici bir platform suşu yarattığını öne sürüyor: kırılgan hastalarda yaşamı tehdit eden fungemiye yol açma olasılığı çok daha düşük olan, ancak probiyotik davranışını koruyan ve zararlı bakterilerle savaşmak üzere daha da donatılabilecek bir maya. Basitçe söylemek gerekirse, çalışma bazen riskli olabilen bir yardımcının gelecekte bağırsak temelli terapiler için daha güvenli, programlanabilir bir müttefike dönüştürülebileceğini gösteriyor.
Atıf: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
Anahtar kelimeler: probiyotik maya, fungemi, gen düzenleme, mikrobiyom, tasarımcı probiyotikler