Clear Sky Science · ru
Дефицит ENA1 ослабляет вирулентность пробиотического дрожжа Saccharomyces ‘boulardii’ в модели фунгемии у иммуносупрессированных мышей
Почему полезные дрожжи иногда становятся вредными
Многие принимают таблетки с пробиотическими дрожжами, чтобы успокоить расстройство желудка или предотвратить диарею во время антибиотикотерапии. Один из самых популярных вариантов продаётся под именем Saccharomyces boulardii. Хотя он помогает многим пациентам, врачи замечают тревожную тенденцию: у некоторых тяжёлобольных или иммуносупрессированных людей эти «дружелюбные» дрожжи могут покинуть кишечник, попасть в кровь и вызвать серьёзные, иногда смертельные, инфекции. В этом исследовании поставлен насущный вопрос для современной медицины: можно ли переработать этот пробиотик так, чтобы он сохранил кишечные преимущества, но значительно утратил способность вызывать опасные инфекции крови?
Растущая обеспокоенность среди уязвимых пациентов
Больницы по всему миру всё чаще сообщают о случаях, когда этот пробиотический дрожжевой штамм обнаруживают в крови пациентов в отделениях интенсивной терапии, после операций или при тяжёлом заболевании. У таких людей обычно ослаблен иммунитет и установлены инвазивные устройства, например катетеры, которые открывают микробам новые пути в организм. В некоторых учреждениях инфекции, связанные с этим пробиотиком, встречаются почти так же часто, как и инфекции классических патогенных грибов. Тем не менее до сих пор большинство исследований сосредотачивалось либо на полезных эффектах дрожжей, либо на их инженерии для производства лекарств, в то время как факторам, делающим их рискованными для уязвимых пациентов, уделялось мало внимания. Авторы попытались заполнить этот пробел, изучив как полезные, так и вредоносные стороны продукта в рамках одного проекта.
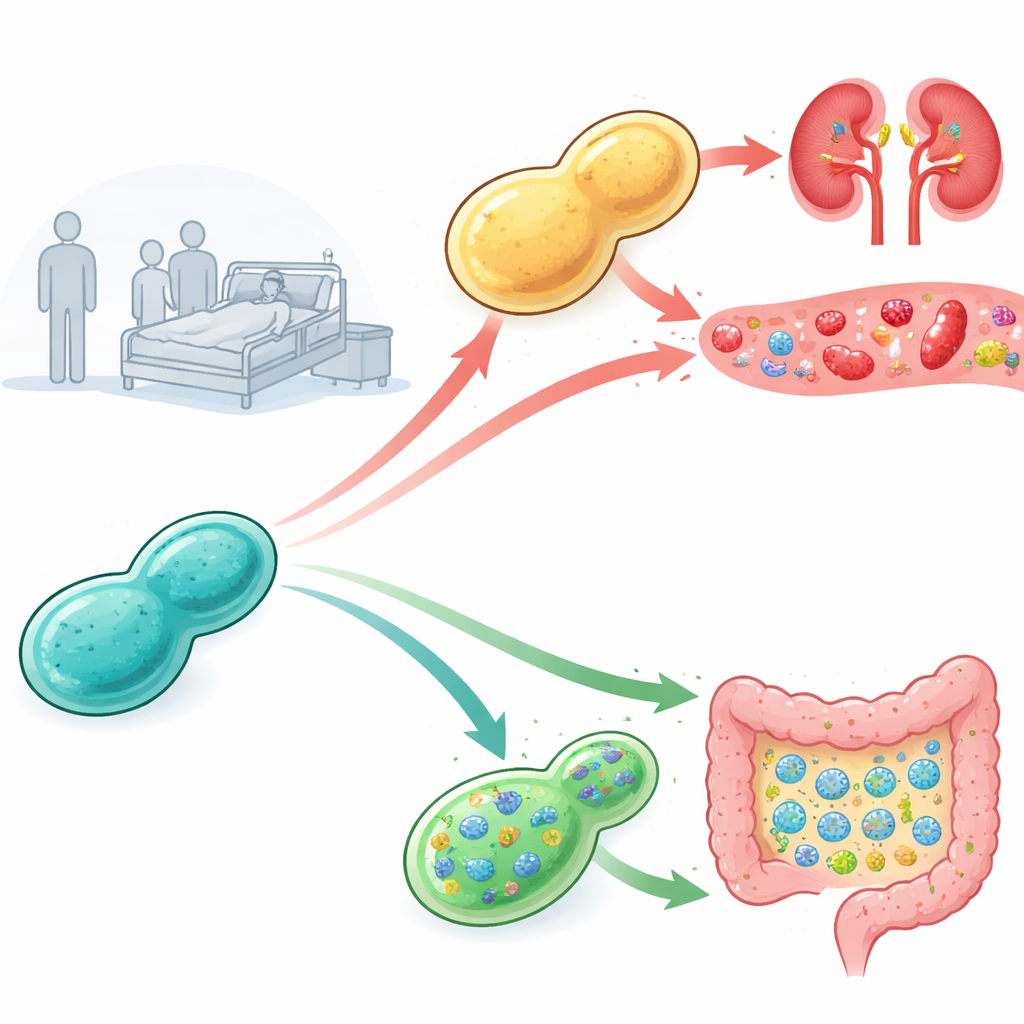
Отслеживание вирулентности в организме мышей
Исследователи собрали пробиотические дрожжи из коммерческих продуктов и образцов из больниц и проверили, насколько опасен каждый из них в мышах с ослабленным иммунитетом. Все мыши, которым вводили дрожжи из коммерческих препаратов, выжили, но некоторые клинические изоляты вызвали высокий процент смертности и сильное разрастание грибка в почках — признак тяжёлой фунгемии. Чтобы понять причину, команда выделила множество сублиний дрожжей до и после инфекции и подвергла их различным стрессам на лабораторных планшетах. Они заметили, что более вирулентные пациентские изоляты, особенно варианты, прошедшие через мышей, были необычно устойчивы к солевым условиям с натрием или литиевыми солями, что намекало на связь между способностью выживать в жёсткой внутренней среде и потенциалом вызывать болезнь.
Выведение ключевого насоса выживания из строя
Солевую устойчивость у дрожжей обеспечивают мембранные транспортеры, выкачивающие ионы внутрь и наружу клетки. Авторы сосредоточились на двух таких генах, ENA1 и NHA1, которые помогают клеткам переживать солевой и щелочной стресс. С помощью редактирования генома CRISPR они удалили каждый ген отдельно в шести различных пробиотических фондах, включая коммерческие и клинические изоляты. Результаты для одного гена были поразительно однозначны: при удалении ENA1 все исследованные штаммы вызывали значительно меньше вреда у мышей. Все животные переживали кратковременную фунгемию, а уровни грибка в почках оставались относительно низкими, даже когда исходный штамм был изначально весьма вирулентен. Напротив, удаление NHA1 не давало последовательного эффекта безопасности и иногда даже делало штаммы более вредными, подчёркивая, что влияние генетической модификации сильно зависит от общего генетического фона.
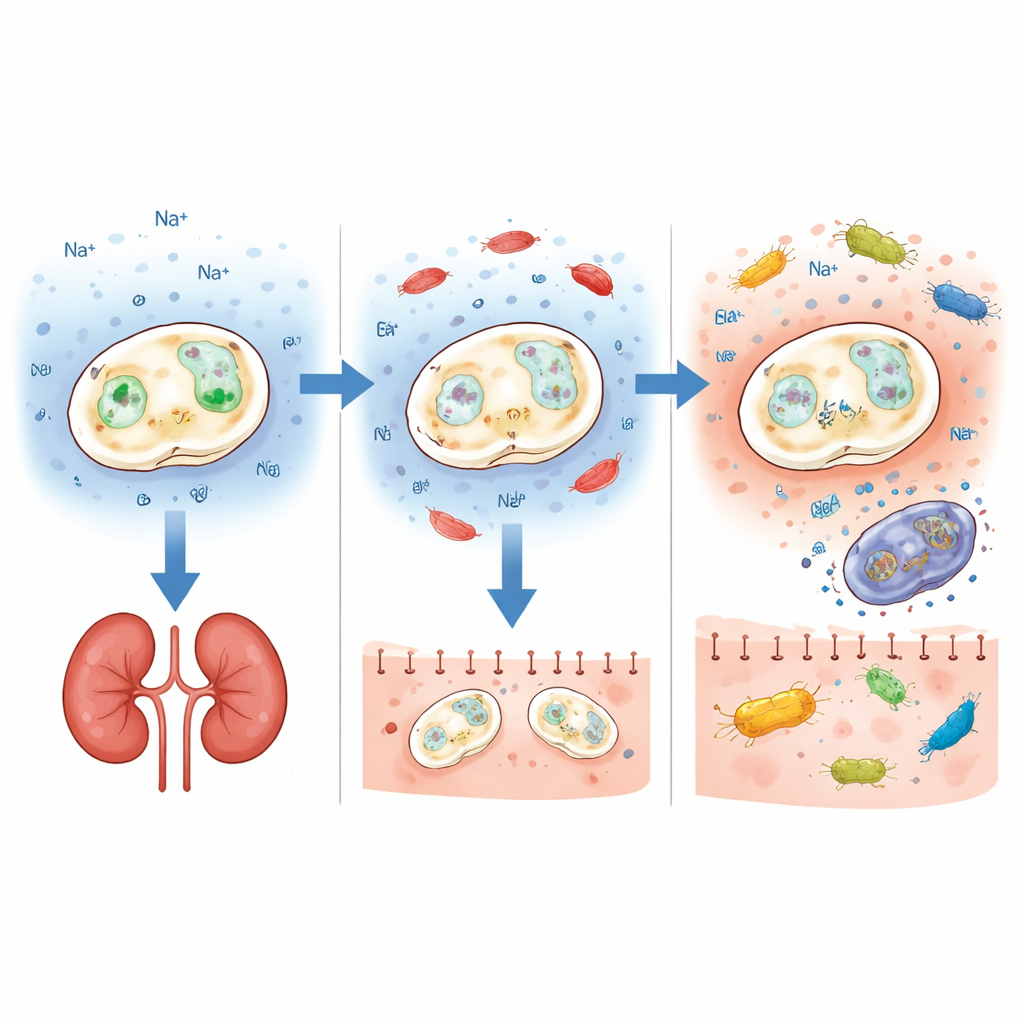
Сохранение преимуществ и добавление дополнительного оружия
Безопасный пробиотик полезен только если он по‑прежнему выполняет свою роль в кишечнике. Поэтому команда проверила, могут ли штаммы с дефицитом ENA1 по‑прежнему хорошо расти в стандартных питательных средах и в условиях, приближённых к кишечным: при умеренной кислотности, наличии жёлчных солей и pH, характерных для тонкой и толстой кишки. Нокаут ENA1 вел себя очень похоже на исходный пробиотик, за исключением затруднений только при необычно высокой щёлочной среде или высоком содержании соли, что нетипично для здорового кишечника. В живых мышах, получавших ежедневные пероральные дозы, модифицированные дрожжи колонизировали кишечник на сопоставимом уровне с коммерческим штаммом и выводились с похожей скоростью после прекращения приёма. Изменённый штамм также изменял состав и разнообразие бактериального сообщества кишечника примерно так же, как и исходный пробиотик, что говорит о сохранении его общего воздействия на кишечник.
Создание более безопасной платформы для будущих терапий
Помимо безопасности, авторы продемонстрировали потенциал «дизайнерского» пробиотика. В демонстрационном эксперименте они заменили ген ENA1 на ДНК, кодирующую Leucocin C — короткий антибактериальный пептид, направленный против Listeria, серьёзного пищевого патогена. Инженерный дрожжевой штамм по‑прежнему характеризовался резко сниженной способностью вызывать фунгемию у мышей, хорошо рос в лабораторных тестах, выдерживал лиофилизацию, используемую в коммерческом производстве, и секретировал активный пептид, который ингибировал Listeria в культуре. В совокупности эти результаты указывают, что удаление ENA1 создаёт перспективную платформенную линию: дрожжи, которые значительно менее склонны вызывать опасную для жизни фунгемию у уязвимых пациентов, но сохраняют пробиотическое поведение и могут дополнительно оснащаться для борьбы с вредными бактериями. Проще говоря, исследование показывает, что можно превратить иногда рискованного помощника в более безопасного, программируемого союзника для будущих кишечных терапий.
Цитирование: Imre, A., Kovács, R., Jakab, Á. et al. ENA1 deficiency attenuates Saccharomyces ‘boulardii’ probiotic yeast virulence in immunosuppressed mouse fungaemia model. Commun Biol 9, 542 (2026). https://doi.org/10.1038/s42003-026-09763-z
Ключевые слова: пробиотические дрожжи, фунгемия, редактирование генов, микробиом, дизайнерские пробиотики