Clear Sky Science · zh
在表达帕尔瓦布明的神经元中缺失 Cacna1c 会促进焦虑与被动应激应对行为
为何微小的脑内开关对压力与焦虑至关重要
焦虑以及我们应对压力的方式常被认为仅由个性或生活经历决定。然而在大脑深处,专门的细胞充当微观开关,帮助决定我们是僵住、放弃,还是积极应对挑战。本研究探讨了其中一种开关:由 CACNA1C 基因编码的电压门控钙通道蛋白 Cav1.2,位于一类特定的抑制性神经元中。研究者仅在小鼠的这些细胞中关闭该蛋白,揭示了大脑连线的微小变化如何将行为倾向推向焦虑与被动应对,为未来更有针对性的精神疾病治疗提供线索。
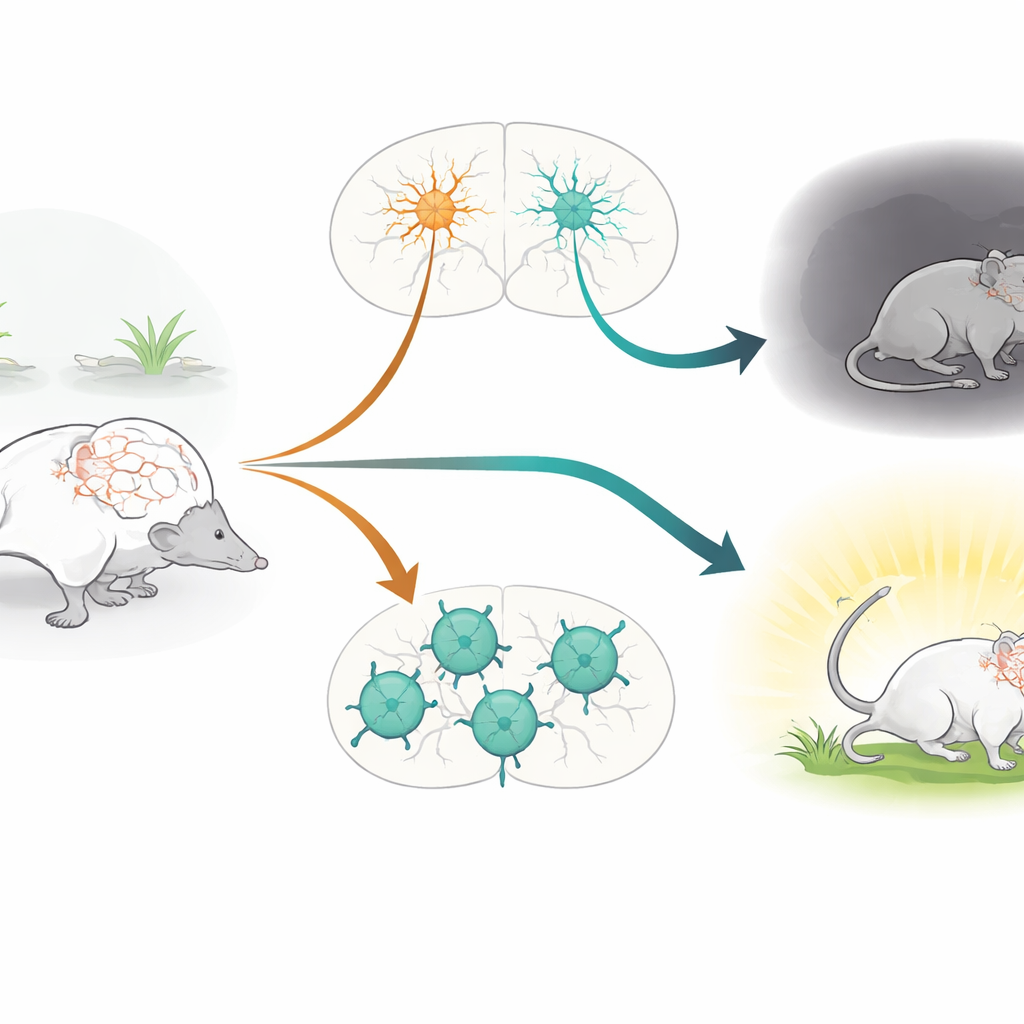
大脑的节律守护者
研究聚焦于帕尔瓦布明阳性(PV+)神经元,这类高速放电的抑制性细胞在大脑中充当节律守护者。它们帮助维持兴奋与抑制之间的微妙平衡,塑造支撑注意力、记忆与情绪的脑节律。PV+ 神经元长期以来与精神分裂症、抑郁、自闭症和癫痫等疾病有关。同时,编码 Cav1.2 钙通道的 CACNA1C 基因是多个精神疾病中一致发现的遗传风险因子之一。Cav1.2 通道在细胞活跃时允许钙离子流入,影响细胞的发育、连接以及随时间调整其突触强度。尽管如此,Cav1.2 在 PV+ 神经元中的特定作用尚未在活体动物中被直接检验。
构建具有靶向改变的小鼠模型
为了解答这个问题,研究者构建了只在 PV+ 神经元中选择性去除 Cav1.2 的小鼠模型,而保持其他细胞类型不受影响。他们使用一种遗传系统,在 PV+ 细胞中特异性地激活“切除”酶(Cre),从而删除 Cacna1c 基因。研究团队在核糖体上添加了分子标记以验证重组发生的位置,确认皮层、海马、杏仁核和小脑等富含 PV 的区域被有效靶向。随后,这些小鼠接受了广泛的行为学测试电池,评估基本运动、类似焦虑的行为、社交互动、学习与记忆以及它们对无法逃避的应激源的反应。
焦虑增加但认知完整
在 PV+ 神经元中缺失 Cav1.2 的小鼠表现出明显增加的类焦虑行为。在常规测试中,动物在安全的黑暗或有掩蔽区域与更开放、明亮的空间之间做选择时,这些改造小鼠比同窝的正常小鼠更强烈地回避开阔或明亮区域,尽管它们的总体活动水平并未改变。令人注目的是,这些小鼠在一系列检测社交偏好、新物体识别、空间记忆以及在水迷宫中学习隐藏平台位置的任务上表现正常。这表明,在该模型中,PV+ 神经元中的 Cav1.2 对情绪调节与应激反应尤为重要,而对社交或认知能力的影响较小。
来自不同细胞类型的相反应激风格
在经常用于研究应激应对风格的强迫游泳测试中,PV 特异性 Cav1.2 敲除小鼠采用了更被动的策略:它们主动游动的时间减少,而静止时间增加。同一研究组早期的工作表明,当在兴奋性谷氨酸能神经元中删除 Cav1.2 时则出现相反效果:那些小鼠在应对压力情境中变得更积极主动。对这两种模型的直接比较证实了这种双向模式。为了将行为与脑活动联系起来,团队在游泳测试后测量了 cFos(一种近期被激活神经元的标记)。在 PV+ 神经元中缺失 Cav1.2 导致如伏隔核、外侧缰核和室旁核—这些与负性情绪与压力处理相关的区域—的活动增强;而在兴奋性神经元中删除则反而增强了参与情绪调节与心理韧性的外侧间脑区的活动。
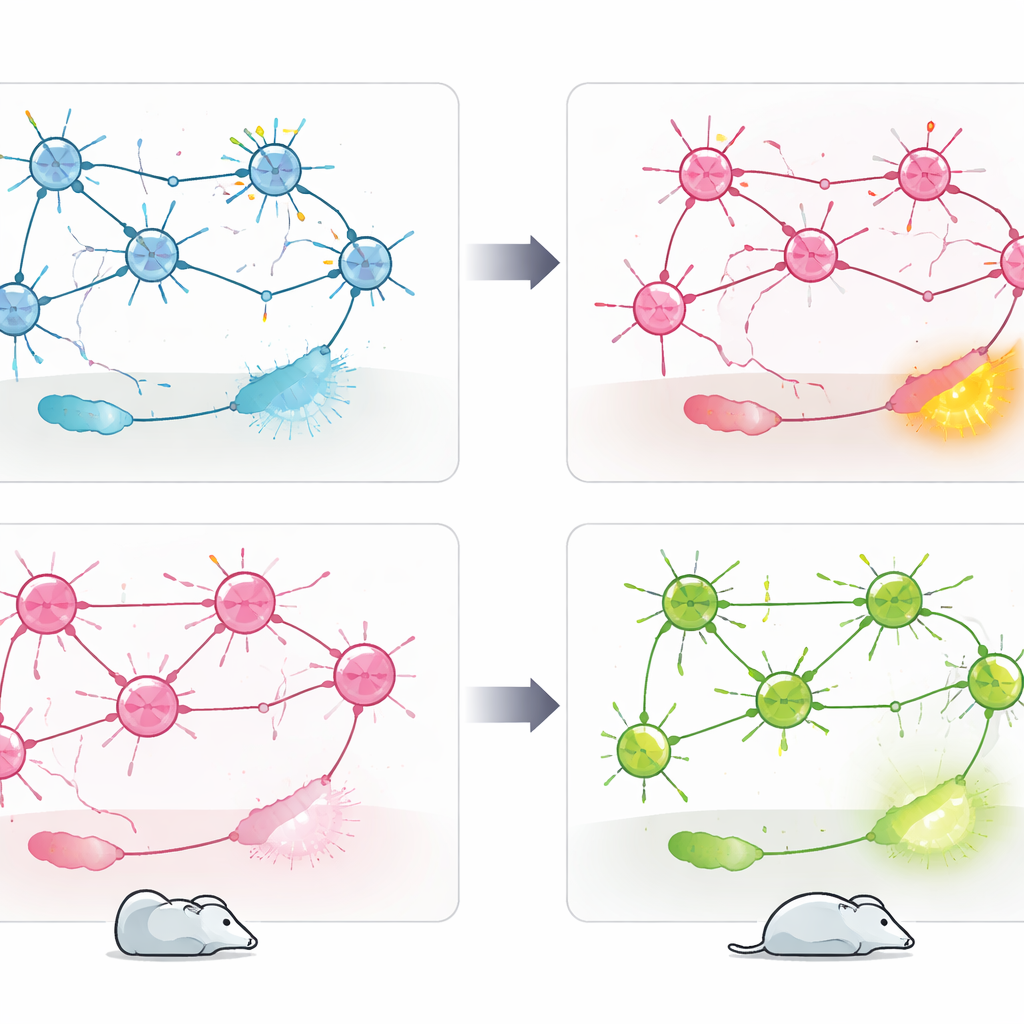
这对未来治疗的意义
综上所述,研究结果表明,相同的风险基因 CACNA1C 可根据受影响的细胞类型将应激行为推向相反方向。PV+ 神经元中的 Cav1.2 似乎对抑制焦虑与被动应对起到刹车作用,而其在兴奋性神经元中的作用则支持另一种更积极的应激应对方式。CACNA1C 并非单一的“好”或“坏”基因,而是作为一种依赖语境的调节因子嵌入不同的脑回路中。对于携带该基因相关精神疾病的人群,这些结果暗示未来的治疗可能需要针对特定的细胞群体或回路节点,而不是在全脑范围内广泛阻断或增强 Cav1.2。
引用: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
关键词: 焦虑, 应对压力, 帕尔瓦布明神经元, CACNA1C, 小鼠行为