Clear Sky Science · nl
Tekort aan Cacna1c in parvalbumine-expressende neuronen bevordert angst en passief stresscopinggedrag
Waarom kleine schakelaarachtige mechanismen in de hersenen ertoe doen voor stress en angst
Angst en hoe we met stress omgaan lijken vaak het resultaat van iemands persoonlijkheid of levenservaring. Toch fungeren gespecialiseerde cellen diep in de hersenen als microscopische schakelaars die mede bepalen of we verstarren, opgeven of actief een uitdaging aangaan. Deze studie onderzoekt één zo’n schakelaar: een calciumkanaaleiwit genaamd Cav1.2, geproduceerd door het CACNA1C-gen, in een specifieke groep remmende hersencellen. Door dit eiwit alleen in die cellen uit te schakelen bij muizen, tonen de onderzoekers aan hoe subtiele verschuivingen in hersenbedrading gedrag richting angst en passief copingsgedrag kunnen kantelen, en bieden ze aanknopingspunten voor toekomstige, meer gerichte behandelingen van psychiatrische aandoeningen.
De ritmewakers van de hersenen
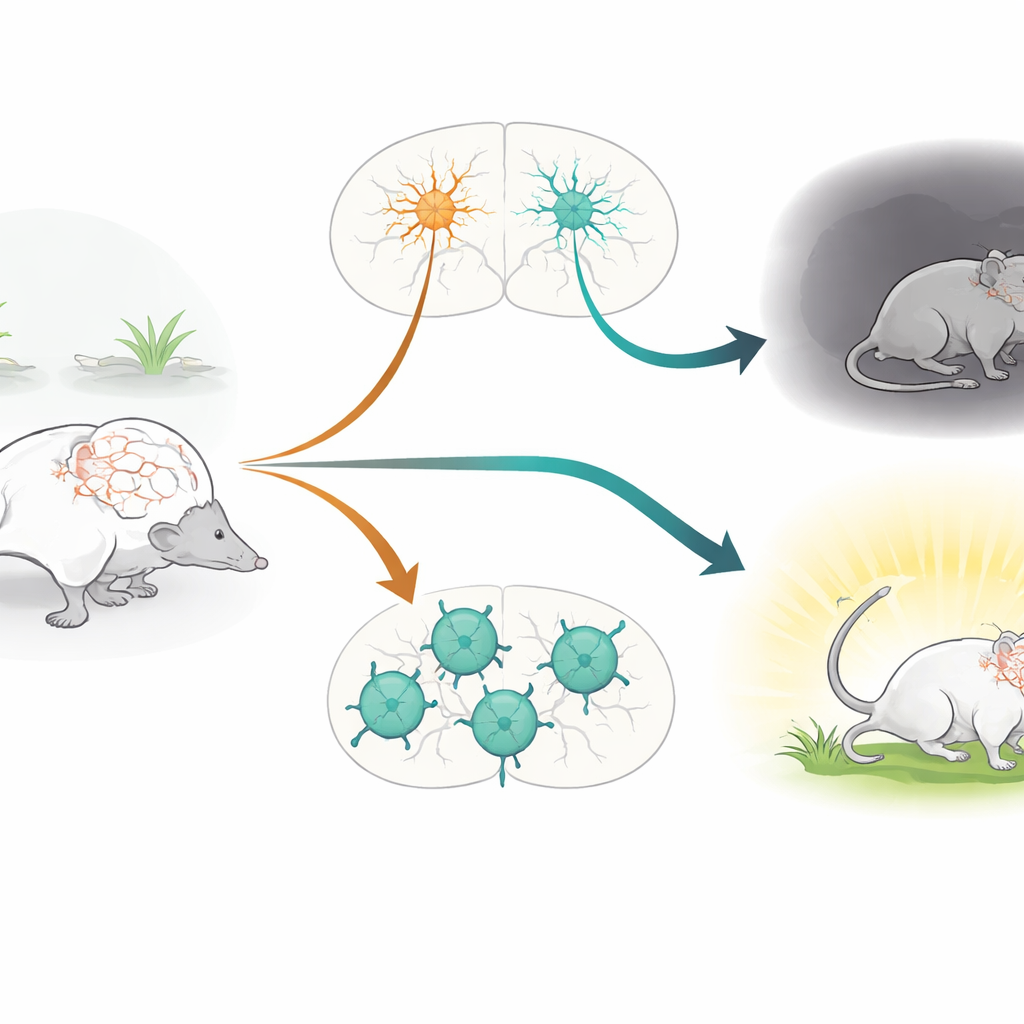
Het onderzoek richt zich op parvalbumine-positieve (PV+) neuronen, een klasse van snel vurende remmende cellen die functioneren als ritmewakers in de hersenen. Deze cellen helpen een delicaat evenwicht tussen excitatie en inhibitie te bewaren en vormen hersenritmes die aandacht, geheugen en emotie ondersteunen. PV+ neuronen worden al lange tijd in verband gebracht met aandoeningen zoals schizofrenie, depressie, autisme en epilepsie. Tegelijkertijd is het CACNA1C-gen, dat het Cav1.2-calciumkanaal codeert, één van de meest consistent aangetroffen genetische risicofactoren bij meerdere psychiatrische aandoeningen. Cav1.2-kanalen laten calciumionen de cel binnenstromen wanneer ze actief zijn, wat invloed heeft op hun ontwikkeling, verbindingen en de aanpassing van synaptische sterkte in de loop van de tijd. Desondanks was de specifieke rol van Cav1.2 in PV+ neuronen nog niet rechtstreeks getest in levende dieren.
Muizen ingegaan op maat gemaakte veranderingen
Om deze vraag te isoleren, maakten de onderzoekers muizen waarin Cav1.2 selectief werd verwijderd alleen in PV+ neuronen, terwijl andere celtypen ongemoeid werden gelaten. Ze gebruikten een genetisch systeem dat een 'knip'-enzym (Cre) specifiek in PV+ cellen activeert, waardoor het Cacna1c-gen daar werd weggehaald. Een moleculaire tag werd toegevoegd aan ribosomen om te verifiëren waar deze recombinatie had plaatsgevonden, wat bevestigde dat PV-rijke gebieden zoals cortex, hippocampus, amygdala en cerebellum effectief werden bereikt. De muizen ondergingen vervolgens een uitgebreid gedragstestpakket dat basisbeweging, angstachtig gedrag, sociale interactie, leren en geheugen en hun reactie op een ontsnappingsloze stressor beoordeelde.
Angstig maar mentaal intact
Muizen zonder Cav1.2 in PV+ neuronen vertoonden een duidelijke toename van angstachtig gedrag. In standaardtests waarin dieren kiezen tussen veilige, donkere of beschutte gebieden en meer blootgestelde, fel verlichte ruimtes, vermeden deze gemodificeerde muizen de open of verlichte zones sterker dan hun normale nestgenoten, hoewel hun algemene bewegingsniveaus ongewijzigd waren. Opvallend genoeg presteerden diezelfde muizen normaal op een breed scala aan taken die sociale voorkeur, herkenning van nieuwe objecten, ruimtelijk geheugen en het leren van de locatie van een verborgen platform in een waterlabyrint onderzochten. Dit suggereert dat, ten minste in dit model, Cav1.2 in PV+ neuronen met name belangrijk is voor emotionele regulatie en stressreacties, eerder dan voor sociale of cognitieve vaardigheden.
Tegenovergestelde stressstijlen vanuit verschillende celtypen
Wanneer ze werden geplaatst in een geforceerde-zwemtest, die vaak wordt gebruikt om stresscopingstijlen te bestuderen, namen PV-specifieke Cav1.2-knockoutmuizen een meer passieve strategie aan: ze besteedden minder tijd aan actief zwemmen en meer tijd aan bewegingsloosheid. Eerder werk van dezelfde groep had het tegenovergestelde effect getoond toen Cav1.2 werd verwijderd in excitatoire glutamaterge neuronen: die muizen gingen actiever om met de stressvolle situatie. Directe vergelijking van de twee modellen bevestigde dit tweerichtingspatroon. Om gedrag met hersenactiviteit te verbinden, mat het team cFos, een merker voor recent geactiveerde neuronen, na de zwemtest. Verlies van Cav1.2 in PV+ neuronen leidde tot verhoogde activiteit in gebieden zoals de nucleus accumbens, laterale habenula en paraventriculaire thalamus—regio’s die gelinkt zijn aan een negatieve stemming en stressverwerking—terwijl deletie in excitatoire neuronen in plaats daarvan de activiteit in de laterale septum versterkte, een gebied betrokken bij emotionele regulatie en veerkracht.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk laten de bevindingen zien dat hetzelfde risicogen, CACNA1C, stressgedrag in tegengestelde richtingen kan duwen, afhankelijk van welk celtype wordt beïnvloed. Cav1.2 in PV+ neuronen lijkt te fungeren als een rem op angst en passief copingsgedrag, terwijl zijn rol in excitatoire neuronen een andere, meer actieve responsstijl op stress ondersteunt. In plaats van één enkel "goed" of "slecht" gen, komt CACNA1C naar voren als een contextafhankelijke regulator ingebed in verschillende hersencircuits. Voor mensen met psychiatrische aandoeningen die aan dit gen gelinkt zijn, suggereren deze resultaten dat toekomstige therapieën mogelijk specifieke celpopulaties of circuitknopen moeten richten, in plaats van het Cav1.2-kanaal in de hele hersenen breed te blokkeren of te versterken.
Bronvermelding: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
Trefwoorden: angst, stresscoping, parvalbumine-neuronen, CACNA1C, muizengedrag