Clear Sky Science · fr
La déficience en Cacna1c dans les neurones exprimant la parvalbumine favorise l’anxiété et les comportements d’évitement passif au stress
Pourquoi de minuscules interrupteurs cérébraux comptent pour le stress et l’anxiété
L’anxiété et notre manière de faire face au stress peuvent donner l’impression d’être uniquement le fruit de la personnalité ou de l’expérience. Pourtant, au cœur du cerveau, des cellules spécialisées font office d’interrupteurs microscopiques qui contribuent à décider si l’on se fige, si l’on abandonne ou si l’on affronte activement une difficulté. Cette étude explore l’un de ces interrupteurs : une protéine canal calcique appelée Cav1.2, codée par le gène CACNA1C, dans un sous-ensemble particulier de cellules inhibitrices. En éteignant cette protéine uniquement dans ces cellules chez la souris, les chercheurs montrent comment de subtils changements dans le câblage cérébral peuvent orienter le comportement vers l’anxiété et des stratégies d’évitement passif, fournissant des indices pour de futurs traitements plus ciblés des troubles psychiatriques.
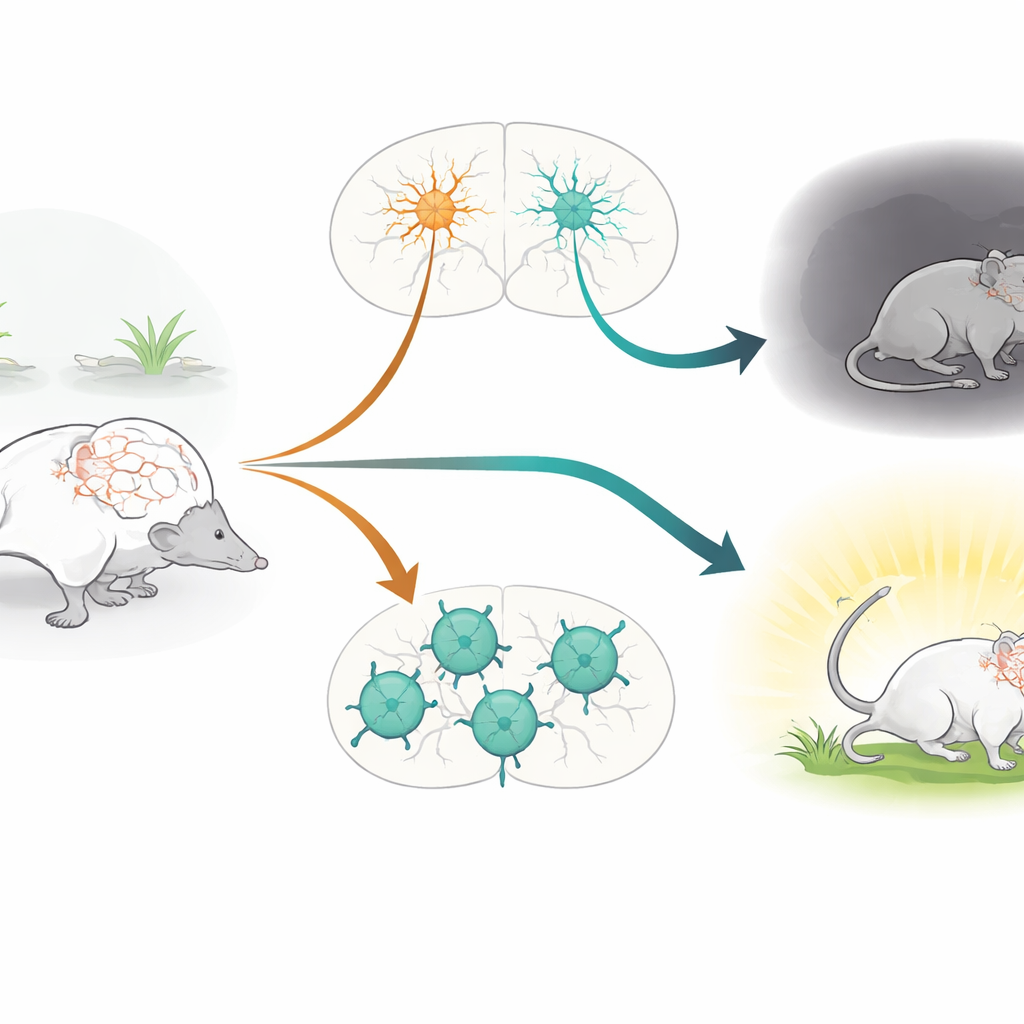
Les gardiens du rythme cérébral
Le travail se concentre sur les neurones positifs pour la parvalbumine (PV+), une classe de cellules inhibitrices à décharge rapide qui jouent le rôle de gardiens du rythme dans le cerveau. Ces cellules contribuent à maintenir un équilibre délicat entre excitation et inhibition, façonnant les rythmes cérébraux qui sous-tendent l’attention, la mémoire et les émotions. Les neurones PV+ ont longtemps été impliqués dans des pathologies telles que la schizophrénie, la dépression, l’autisme et l’épilepsie. Parallèlement, le gène CACNA1C, qui code pour le canal calcique Cav1.2, est l’un des facteurs génétiques de risque les plus régulièrement identifiés dans plusieurs troubles psychiatriques. Les canaux Cav1.2 laissent entrer des ions calcium dans les cellules lorsqu’elles sont actives, influençant leur développement, leurs connexions et la façon dont elles ajustent leur force au fil du temps. Malgré cela, le rôle spécifique de Cav1.2 au sein des neurones PV+ n’avait pas été testé directement chez des animaux vivants.
Des souris génétiquement modifiées de façon ciblée
Pour isoler cette question, les chercheurs ont conçu des souris dans lesquelles Cav1.2 a été retiré sélectivement uniquement des neurones PV+, laissant les autres types cellulaires intacts. Ils ont utilisé un système génétique qui active une enzyme de découpe (Cre) spécifiquement dans les cellules PV+, supprimant ainsi le gène Cacna1c à ces endroits. Une étiquette moléculaire a été ajoutée aux ribosomes pour vérifier où cette recombinaison avait lieu, confirmant que des régions riches en PV telles que le cortex, l’hippocampe, l’amygdale et le cervelet étaient effectivement ciblées. Les souris ont ensuite été soumises à une batterie étendue de tests comportementaux évaluant la locomotion de base, les comportements de type anxieux, l’interaction sociale, l’apprentissage et la mémoire, ainsi que leur réponse à un stresseur inévitable.
Anxieux mais mentalement préservés
Les souris dépourvues de Cav1.2 dans les neurones PV+ ont montré une augmentation nette des comportements de type anxieux. Dans des tests standards où les animaux choisissent entre des zones sûres, sombres ou abritées et des espaces plus exposés et éclairés, ces souris modifiées ont évité les zones ouvertes ou éclairées plus fortement que leurs congénères normaux, bien que leur niveau global de mouvement soit inchangé. Fait remarquable, ces mêmes souris ont néanmoins obtenu des performances normales sur une large gamme de tâches évaluant la préférence sociale, la reconnaissance d’objets nouveaux, la mémoire spatiale et l’apprentissage de l’emplacement d’une plateforme cachée dans un test de type labyrinthe d’eau. Cela suggère que, au moins dans ce modèle, Cav1.2 dans les neurones PV+ est particulièrement important pour la régulation émotionnelle et les réponses au stress, plutôt que pour les capacités sociales ou cognitives.
Styles de réaction opposés selon le type cellulaire
Lorsqu’elles ont été placées dans un test de nage forcée, souvent utilisé pour étudier les styles de coping au stress, les souris avec suppression de Cav1.2 spécifique aux PV ont adopté une stratégie plus passive : elles ont passé moins de temps à nager activement et plus de temps immobiles. Des travaux antérieurs du même groupe avaient montré l’effet inverse lorsque Cav1.2 était supprimé dans les neurones excitateurs glutamatergiques : ces souris devenaient plus actives dans leur façon de faire face à la situation stressante. La comparaison directe des deux modèles a confirmé ce schéma bidirectionnel. Pour relier le comportement à l’activité cérébrale, l’équipe a mesuré la cFos, un marqueur des neurones récemment activés, après le test de nage. La perte de Cav1.2 dans les neurones PV+ a conduit à une activité accrue dans des régions telles que le noyau accumbens, l’habénula latérale et le thalamus paraventriculaire — des zones liées à l’humeur négative et au traitement du stress — tandis que la suppression dans les neurones excitateurs augmentait plutôt l’activité dans le septum latéral, une région impliquée dans la régulation émotionnelle et la résilience.
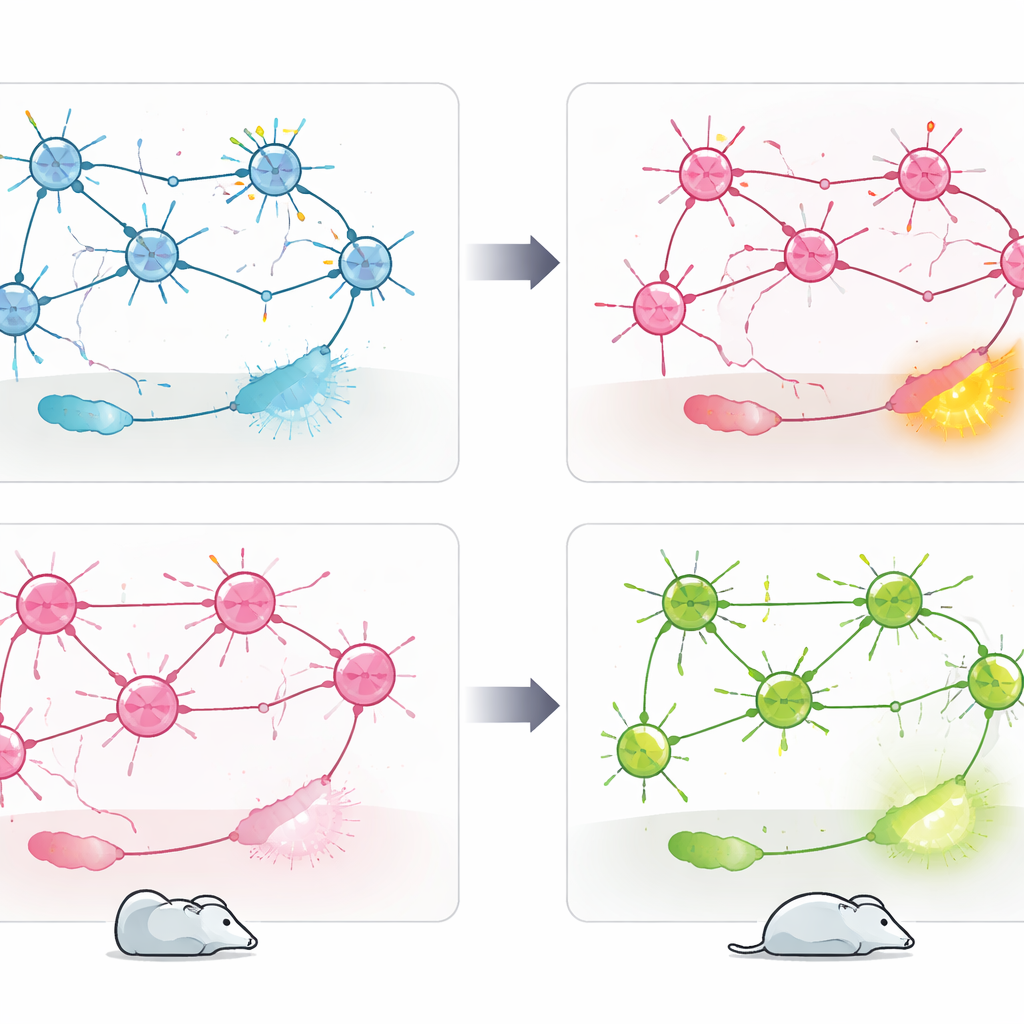
Ce que cela implique pour les traitements futurs
En somme, ces résultats montrent que le même gène de risque, CACNA1C, peut orienter le comportement face au stress dans des directions opposées selon le type cellulaire affecté. Cav1.2 dans les neurones PV+ semble jouer le rôle d’un frein sur l’anxiété et le coping passif, tandis que son rôle dans les neurones excitateurs soutient un style de réponse au stress plus actif. Plutôt que d’être un gène « bon » ou « mauvais », CACNA1C apparaît comme un régulateur dépendant du contexte, intégré dans des circuits cérébraux distincts. Pour les personnes vivant avec des troubles psychiatriques liés à ce gène, ces résultats suggèrent que les thérapies futures pourraient devoir cibler des populations cellulaires ou des nœuds de circuit spécifiques, plutôt que de bloquer ou d’amplifier de manière générale Cav1.2 dans tout le cerveau.
Citation: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
Mots-clés: anxiété, coping au stress, neurones à parvalbumine, CACNA1C, comportement des souris