Clear Sky Science · de
Cacna1c-Mangel in parvalbumin-exprimierenden Neuronen fördert Angst und passives Stressbewältigungsverhalten
Warum winzige Schaltstellen im Gehirn für Stress und Angst wichtig sind
Angst und unsere Art, mit Stress umzugehen, erscheinen oft als Ergebnisse von Persönlichkeit oder Lebenserfahrung. Tief im Gehirn agieren jedoch spezialisierte Zellen als mikroskopische Schalter, die mitentscheiden, ob wir erstarren, aufgeben oder aktiv gegen eine Herausforderung ankämpfen. Diese Studie untersucht einen solchen Schalter: ein Calciumkanalprotein namens Cav1.2, codiert vom Gen CACNA1C, in einer bestimmten Klasse inhibitorischer Gehirnzellen. Indem die Forschenden dieses Protein nur in genau diesen Zellen bei Mäusen ausschalten, zeigen sie, wie subtile Veränderungen in der neuronalen Verschaltung das Verhalten zugunsten von Angst und passiver Bewältigung verschieben können — ein Hinweis für künftig gezieltere Behandlungsansätze bei psychiatrischen Erkrankungen.
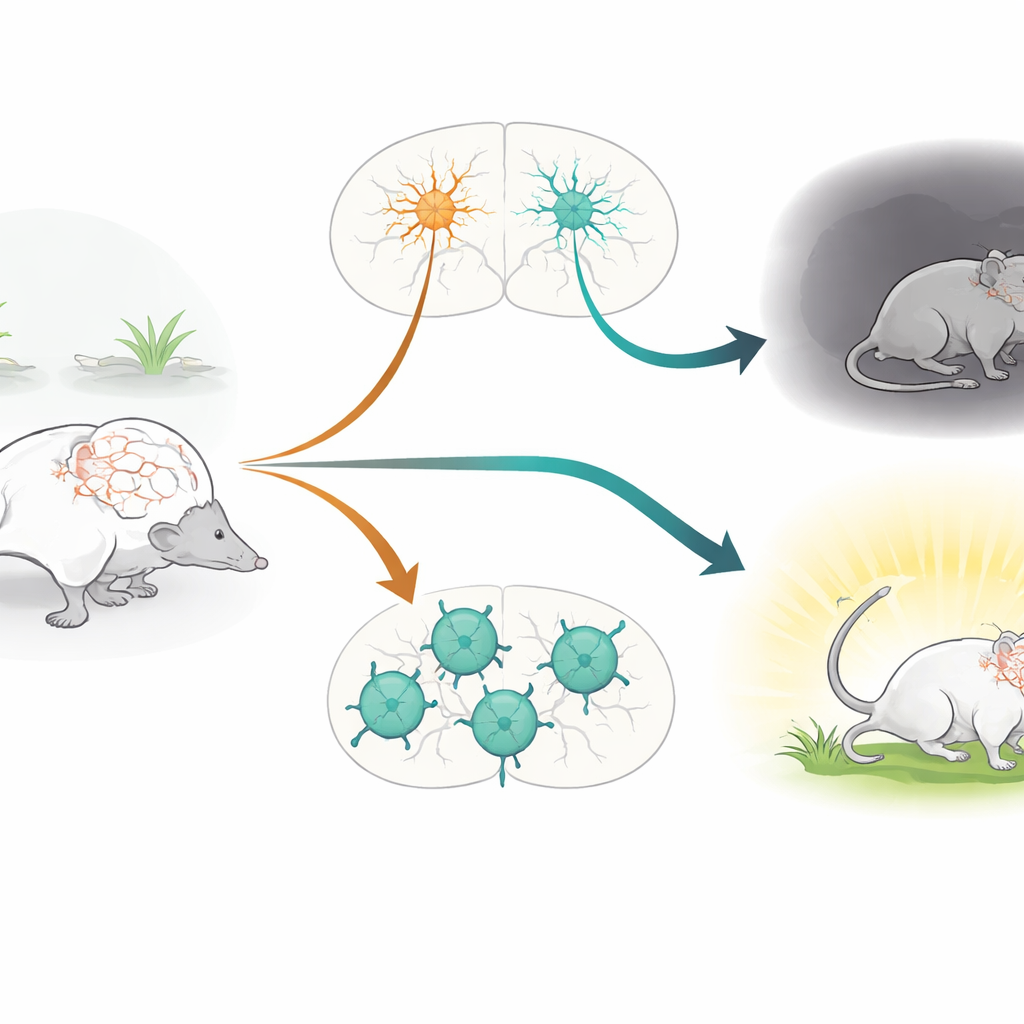
Die Rhythmusgeber des Gehirns
Die Arbeit konzentriert sich auf parvalbumin-positive (PV+) Neuronen, eine Klasse schnell feuender inhibitorischer Zellen, die als Rhythmusgeber im Gehirn fungieren. Diese Zellen helfen, ein empfindliches Gleichgewicht zwischen Erregung und Hemmung zu erhalten und formen Hirnrhythmen, die Aufmerksamkeit, Gedächtnis und Emotionen zugrunde liegen. PV+-Neuronen werden seit Langem mit Erkrankungen wie Schizophrenie, Depression, Autismus und Epilepsie in Verbindung gebracht. Gleichzeitig ist das Gen CACNA1C, das den Cav1.2-Calciumkanal codiert, einer der beständigsten genetischen Risikofaktoren über verschiedene psychiatrische Störungen hinweg. Cav1.2-Kanäle erlauben Calciumionen, in aktive Zellen einzuströmen, und beeinflussen so deren Entwicklung, Vernetzung und langfristige Anpassungsfähigkeit. Dennoch war die spezifische Rolle von Cav1.2 in PV+-Neuronen in lebenden Tieren bislang nicht direkt untersucht worden.
Mäuse mit gezielten Veränderungen erzeugen
Um diese Frage zu isolieren, erzeugten die Forschenden Mäuse, bei denen Cav1.2 selektiv nur in PV+-Neuronen entfernt wurde, während andere Zelltypen unberührt blieben. Sie nutzten ein genetisches System, das ein in PV+-Zellen aktiviertes „Schneide“-Enzym (Cre) aktiviert und dort das Cacna1c-Gen löscht. Ein molekulares Tag wurde den Ribosomen hinzugefügt, um zu verifizieren, wo diese Rekombination stattgefunden hatte, und bestätigte, dass PV-reiche Regionen wie Kortex, Hippocampus, Amygdala und Kleinhirn effektiv getroffen wurden. Die Mäuse unterzogen sich anschließend einer umfangreichen Verhaltensbatterie, die Grundbewegung, angstähnliches Verhalten, soziale Interaktion, Lernen und Gedächtnis sowie Reaktionen auf einen unausweichlichen Stressor bewertete.
Ängstlich, aber geistig intakt
Mäuse ohne Cav1.2 in PV+-Neuronen zeigten eine deutliche Zunahme von angstähnlichem Verhalten. In Standardtests, in denen Tiere zwischen sicheren, dunklen oder geschützten Bereichen und offeneren, helleren Zonen wählen, mieden diese veränderten Mäuse die offenen oder beleuchteten Bereiche stärker als ihre normalen Wurfgeschwister, obwohl sich ihr generelles Bewegungsniveau nicht verändert hatte. Auffällig ist jedoch, dass dieselben Mäuse in einer Vielzahl von Aufgaben zur sozialen Präferenz, Wiedererkennung neuer Objekte, räumlichem Gedächtnis und dem Erlernen der Lage einer verborgenen Plattform im Wasserlabyrinth normal abschnitten. Das deutet darauf hin, dass Cav1.2 in PV+-Neuronen in diesem Modell vor allem für die emotionale Regulation und Stressantworten wichtig ist, weniger für soziale oder kognitive Fähigkeiten.
Entgegengesetzte Stressstile durch verschiedene Zelltypen
Wurden die Mäuse in einem erzwungenen Schwimmtest platziert, der oft zur Untersuchung von Stressbewältigungsstilen verwendet wird, zeigten die PV-spezifischen Cav1.2-Knockout-Mäuse eine eher passive Strategie: Sie verbrachten weniger Zeit mit aktivem Schwimmen und mehr Zeit unbeweglich. Frühere Arbeiten derselben Gruppe hatten den entgegengesetzten Effekt gezeigt, wenn Cav1.2 in exzitatorischen glutamatergen Neuronen gelöscht wurde: Diese Mäuse zeigten ein aktiveres Bewältigungsverhalten. Der direkte Vergleich der beiden Modelle bestätigte dieses bidirektionale Muster. Um Verhalten mit Gehirnaktivität zu verknüpfen, maßen die Forschenden cFos, einen Marker kürzlich aktivierter Neuronen, nach dem Schwimmtest. Der Verlust von Cav1.2 in PV+-Neuronen führte zu erhöhter Aktivität in Bereichen wie dem Nucleus accumbens, der lateralen Habenula und dem paraventrikulären Thalamus — Regionen, die mit negativer Stimmung und Stressverarbeitung verbunden sind — während die Deletion in exzitatorischen Neuronen stattdessen die Aktivität in der lateralen Septumregion steigerte, die an emotionaler Regulation und Resilienz beteiligt ist.
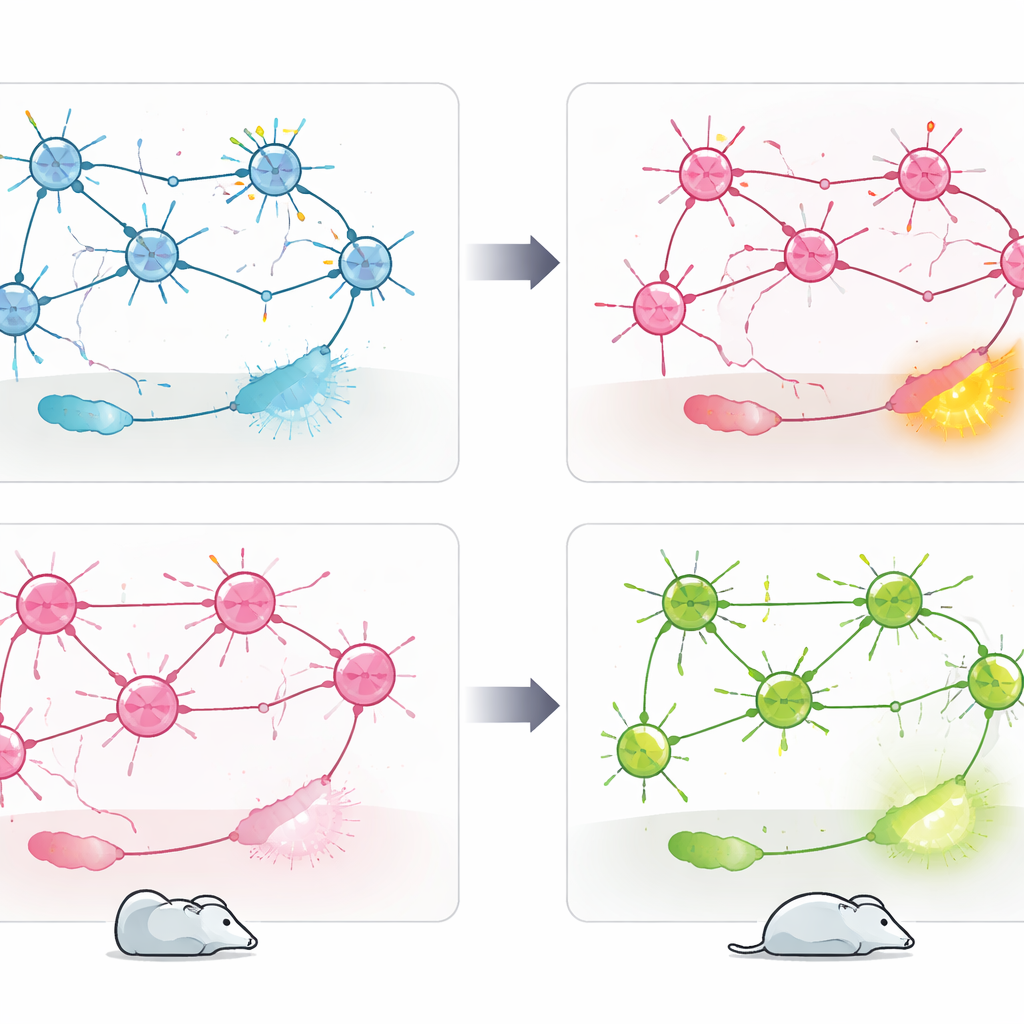
Was das für künftige Behandlungen bedeutet
In der Summe zeigen die Befunde, dass dasselbe Risikogen, CACNA1C, das Stressverhalten in unterschiedliche Richtungen treiben kann, abhängig davon, welcher Zelltyp betroffen ist. Cav1.2 in PV+-Neuronen scheint als Bremse für Angst und passives Bewältigen zu wirken, während seine Rolle in exzitatorischen Neuronen einen anderen, aktiveren Bewältigungsstil unterstützt. Statt eines einfachen „guten“ oder „schlechten“ Gens tritt CACNA1C als kontextabhängiger Regulator in unterschiedlichen Schaltkreisen des Gehirns hervor. Für Menschen mit psychiatrischen Erkrankungen, die mit diesem Gen zusammenhängen, deuten diese Ergebnisse darauf hin, dass künftige Therapien bestimmte Zellpopulationen oder Schaltkreispunkte ins Visier nehmen könnten, statt Cav1.2 breit im ganzen Gehirn zu hemmen oder zu verstärken.
Zitation: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
Schlüsselwörter: Angst, Stressbewältigung, Parvalbumin-Neuronen, CACNA1C, Mausverhalten