Clear Sky Science · ru
Дефицит Cacna1c в нейронах, экспрессирующих парвальбумин, усиливает тревожность и пассивное поведение при стрессе
Почему маленькие «переключатели» мозга имеют значение для стресса и тревоги
Тревога и наши стратегии совладания со стрессом кажутся чем-то, что определяется только личностью или жизненным опытом. Однако глубоко в мозге специализированные клетки выступают в роли микроскопических переключателей, которые помогают решить, замереть, сдаться или активно преодолевать трудности. В этом исследовании изучается один такой переключатель: кальциевый канал Cav1.2, кодируемый геном CACNA1C, в конкретном подтипе ингибирующих клеток. Отключив этот белок только в этих клетках у мышей, исследователи показали, как тонкие изменения в проводке мозга могут смещать поведение в сторону тревожности и пассивного совладания, что даёт подсказки для будущих более целевых подходов к лечению психиатрических расстройств.
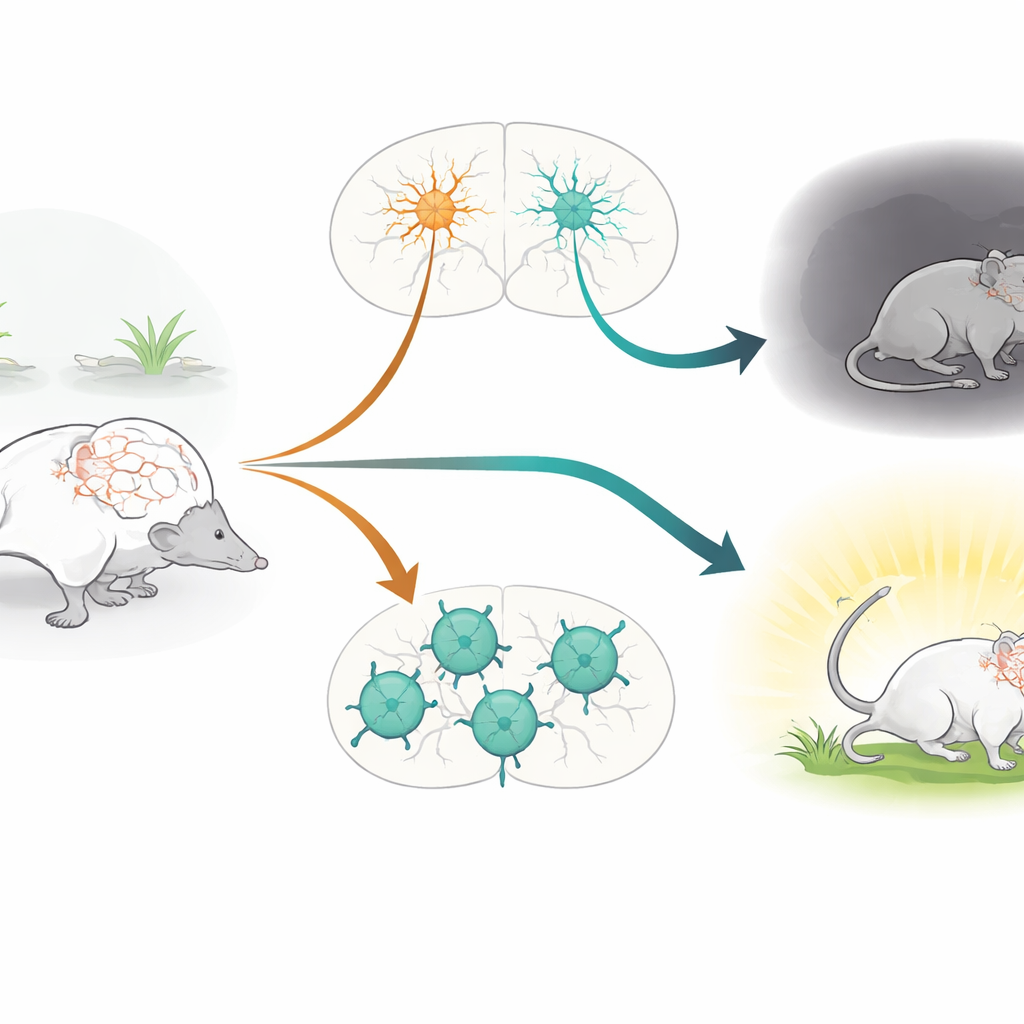
Хранители ритма мозга
Работа сосредоточена на парвальбумин-положительных (PV+) нейронах — классе быстро стреляющих ингибирующих клеток, которые выступают хранителями ритма в мозге. Эти клетки помогают поддерживать тонкое равновесие между возбуждением и торможением, формируя мозговые ритмы, лежащие в основе внимания, памяти и эмоций. PV+ нейроны давно связывают с такими состояниями, как шизофрения, депрессия, аутизм и эпилепсия. В то же время ген CACNA1C, кодирующий кальциевый канал Cav1.2, является одним из наиболее последовательно выявляемых генетических факторов риска при различных психиатрических расстройствах. Каналы Cav1.2 позволяют ионам кальция входить в клетки при их активации, влияя на развитие, установление связей и пластичность со временем. Несмотря на это, конкретную роль Cav1.2 в PV+ нейронах ранее не проверяли непосредственно на живых животных.
Создание мышей с целенаправленными изменениями
Чтобы изолировать этот вопрос, исследователи создали мышей, у которых Cav1.2 селективно удалён только из PV+ нейронов, не затрагивая другие типы клеток. Они использовали генетическую систему, активирующую «режущий» фермент (Cre) именно в PV+ клетках, что приводит к удалению гена Cacna1c там. К рибосомам был добавлен молекулярный маркер, чтобы проверить, где произошла рекомбинация, подтвердив, что районы, богатые PV-нейронами, такие как кора, гиппокамп, амигдала и мозжечок, были эффективно нацелены. Затем мыши прошли обширный набор поведенческих тестов, оценивавших базовую подвижность, поведение, похожее на тревожное, социальное взаимодействие, обучение и память, а также реакцию на неизбежный стрессовый фактор.
Тревожные, но с сохранёнными умственными способностями
Мыши без Cav1.2 в PV+ нейронах демонстрировали явное усиление тревожноподобного поведения. В стандартных тестах, где животные выбирают между безопасными тёмными или укрытыми местами и более открытыми, ярко освещёнными зонами, модифицированные мыши сильнее избегали открытых или освещённых участков по сравнению с нормальными сибсами, хотя общая активность движения не изменилась. Удивительно, однако, что те же мыши нормально справлялись с широким спектром задач, проверяющих социальные предпочтения, распознавание новых объектов, пространственную память и обучение местоположению скрытой платформы в водном лабиринте. Это указывает на то, что, по крайней мере в этой модели, Cav1.2 в PV+ нейронах особенно важен для эмоциональной регуляции и реакций на стресс, а не для социальных или когнитивных способностей.
Противоположные стили совладания в зависимости от типа клетки
При помещении в тест вынужденного плавания, который часто используют для изучения стилей совладания со стрессом, мыши с нокаутом Cav1.2 в PV+ нейронах перешли к более пассивной стратегии: они проводили меньше времени в активном плавании и больше — в неподвижности. Ранее та же группа показала противоположный эффект при удалении Cav1.2 в возбуждающих глутаматергических нейронах: такие мыши становились более активно вовлечёнными в преодоление стрессовой ситуации. Прямое сравнение двух моделей подтвердило этот двунаправленный паттерн. Чтобы связать поведение с активностью мозга, команда измерила cFos — маркер недавно активированных нейронов — после теста плавания. Потеря Cav1.2 в PV+ нейронах привела к повышенной активности в областях, таких как ядро аккумбенс, латеральная габенула и паравентрикулярное ядро таламуса — регионах, связанных с негативным настроением и обработкой стресса — тогда как удаление в возбуждающих нейронах, напротив, усиливало активность в латеральном септуме, области, вовлечённой в эмоциональную регуляцию и устойчивость.
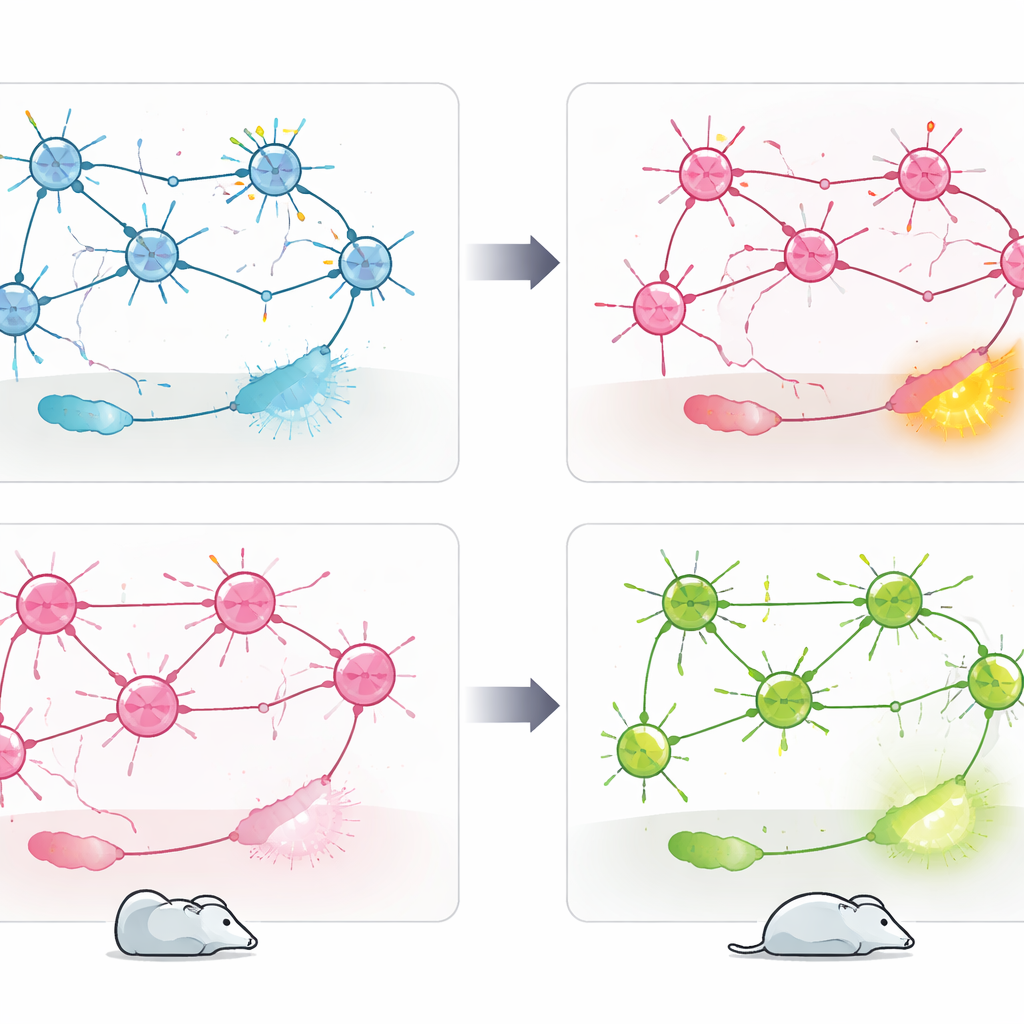
Что это значит для будущих терапий
В совокупности результаты показывают, что один и тот же ген риска, CACNA1C, может сдвигать поведение при стрессе в противоположные стороны в зависимости от того, какой тип клетки затронут. Cav1.2 в PV+ нейронах, по-видимому, действует как тормоз для тревоги и пассивного совладания, тогда как его роль в возбуждающих нейронах поддерживает другой, более активный стиль реакции на стресс. Вместо того чтобы рассматривать CACNA1C как однозначно «хороший» или «плохой» ген, он предстает как контекст-зависимый регулятор, встроенный в разные мозговые цепи. Для людей с психиатрическими расстройствами, связанными с этим геном, эти результаты намекают, что будущие терапии могут потребовать нацеливания на конкретные популяции клеток или узлы схем, а не на широкое блокирование или усиление Cav1.2 по всему мозгу.
Цитирование: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
Ключевые слова: тревожность, совладание со стрессом, нейроны парвальбумин-положительные, CACNA1C, поведение мышей