Clear Sky Science · pt
Deficiência de Cacna1c em neurônios que exprimem parvalbumina promove ansiedade e comportamento passivo de enfrentamento ao estresse
Por que pequenos interruptores cerebrais importam para estresse e ansiedade
A ansiedade e a maneira como enfrentamos o estresse podem parecer frutos apenas da personalidade ou da experiência de vida. Ainda assim, lá no interior do cérebro, células especializadas atuam como interruptores microscópicos que ajudam a decidir se congelamos, desistimos ou enfrentamos ativamente um desafio. Este estudo explora um desses interruptores: uma proteína de canal de cálcio chamada Cav1.2, produzida pelo gene CACNA1C, em um conjunto particular de células inibitórias do cérebro. Ao desligar essa proteína apenas nessas células em camundongos, os pesquisadores revelam como mudanças sutis na conectividade cerebral podem inclinar o comportamento em direção à ansiedade e ao enfrentamento passivo, oferecendo pistas para tratamentos futuros mais direcionados de transtornos psiquiátricos.
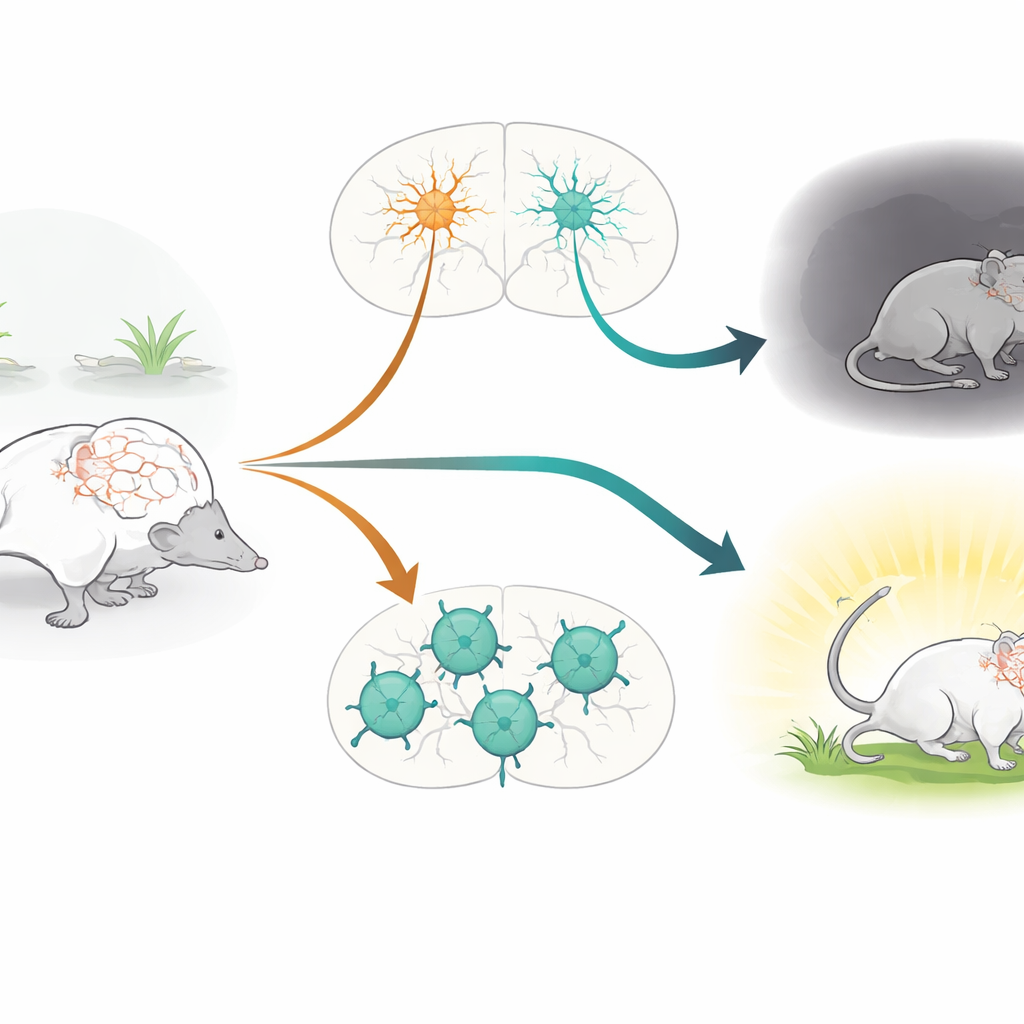
Os reguladores de ritmo do cérebro
O trabalho focaliza os neurônios positivos para parvalbumina (PV+), uma classe de células inibitórias de disparo rápido que atuam como reguladoras de ritmo no cérebro. Essas células ajudam a manter um equilíbrio delicado entre excitação e inibição, moldando ritmos cerebrais que sustentam atenção, memória e emoção. Neurônios PV+ há muito estão implicados em condições como esquizofrenia, depressão, autismo e epilepsia. Ao mesmo tempo, o gene CACNA1C, que codifica o canal de cálcio Cav1.2, é um dos fatores de risco genético mais consistentemente identificados em múltiplos transtornos psiquiátricos. Canais Cav1.2 permitem a entrada de íons cálcio nas células quando estão ativos, influenciando como elas se desenvolvem, se conectam e ajustam sua força ao longo do tempo. Apesar disso, o papel específico de Cav1.2 dentro dos neurônios PV+ não havia sido testado diretamente em animais vivos.
Gerando camundongos com alterações direcionadas
Para isolar essa questão, os pesquisadores criaram camundongos nos quais Cav1.2 foi removido seletivamente apenas dos neurônios PV+, deixando outros tipos celulares intactos. Eles usaram um sistema genético que ativa uma enzima “cortadora” (Cre) especificamente nas células PV+, deletando aí o gene Cacna1c. Uma etiqueta molecular foi adicionada aos ribossomos para verificar onde essa recombinação ocorreu, confirmando que regiões ricas em PV, como córtex, hipocampo, amígdala e cerebelo, foram efetivamente alvo. Os camundongos então passaram por uma extensa bateria de testes comportamentais que avaliaram movimento básico, comportamento semelhante à ansiedade, interação social, aprendizagem e memória, e como responderam a um estressor inescapável.
Ansiosos, mas mentalmente preservados
Camundongos sem Cav1.2 em neurônios PV+ mostraram um claro aumento em comportamentos semelhantes à ansiedade. Em testes padrão em que os animais escolhem entre áreas seguras, escuras ou abrigadas e espaços mais expostos e iluminados, esses camundongos modificados evitaram mais fortemente as zonas abertas ou iluminadas do que seus irmãos normais, embora seus níveis gerais de movimento não tenham mudado. Notavelmente, porém, esses mesmos animais desempenharam-se normalmente em uma ampla gama de tarefas que investigam preferência social, reconhecimento de novos objetos, memória espacial e aprendizado da localização de uma plataforma escondida em um labirinto aquático. Isso sugere que, ao menos nesse modelo, Cav1.2 em neurônios PV+ é particularmente importante para a regulação emocional e respostas ao estresse, em vez de habilidades sociais ou cognitivas.
Estilos de estresse opostos vindos de tipos celulares diferentes
Quando colocados em um teste de natação forçada, frequentemente usado para estudar estilos de enfrentamento do estresse, os camundongos com knockout de Cav1.2 específico em PV adotaram uma estratégia mais passiva: passaram menos tempo nadando ativamente e mais tempo imóveis. Trabalhos anteriores do mesmo grupo mostraram o efeito oposto quando Cav1.2 foi deletado em neurônios excitatórios glutamatérgicos: esses camundongos tornaram-se mais engajados ativamente ao lidar com a situação estressante. A comparação direta dos dois modelos confirmou esse padrão bidirecional. Para conectar comportamento à atividade cerebral, a equipe mediu cFos, um marcador de neurônios recentemente ativados, após o teste de natação. A perda de Cav1.2 em neurônios PV+ levou a aumento de atividade em áreas como núcleo accumbens, habenula lateral e tálamo paraventricular—regiões ligadas ao humor negativo e ao processamento do estresse—enquanto a deleção em neurônios excitatórios, por sua vez, aumentou a atividade no septo lateral, uma região envolvida na regulação emocional e resiliência.
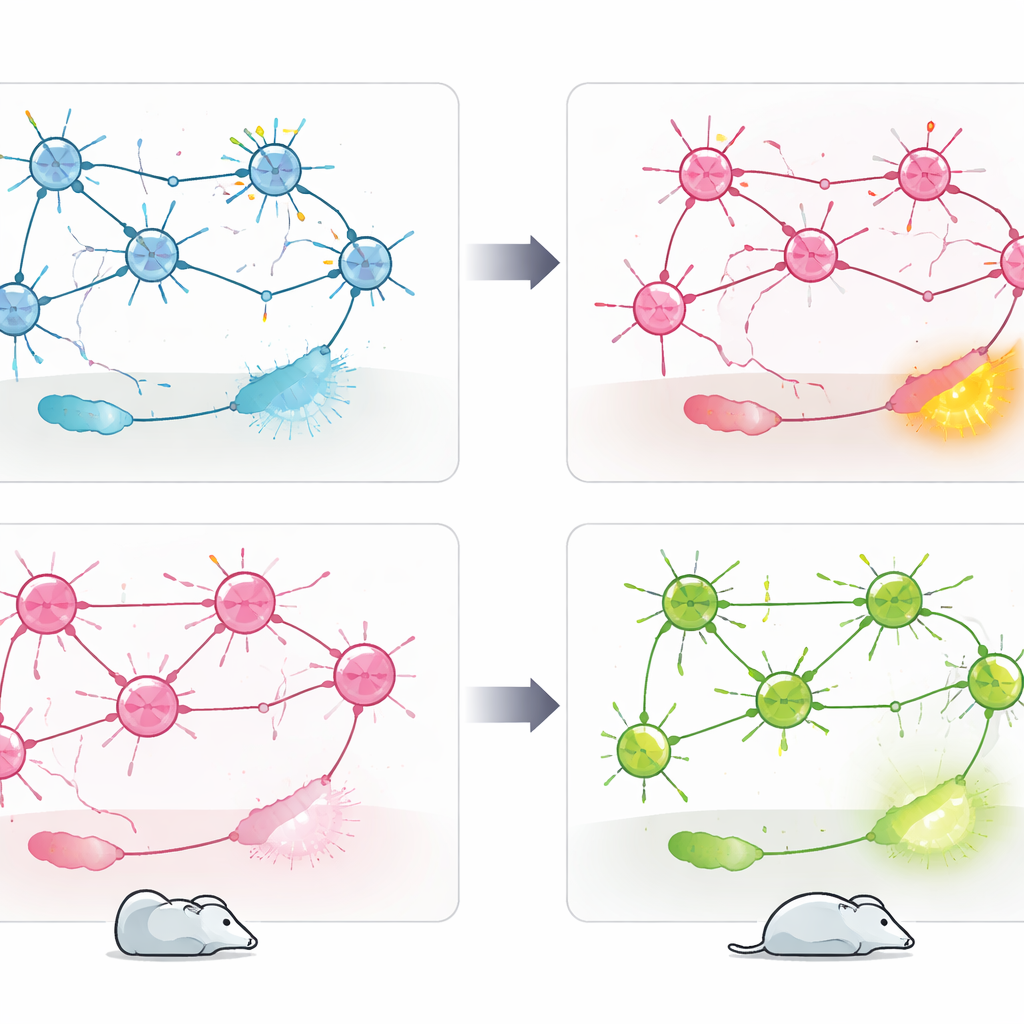
O que isso significa para tratamentos futuros
Em conjunto, os achados mostram que o mesmo gene de risco, CACNA1C, pode empurrar o comportamento em relação ao estresse em direções opostas dependendo de qual tipo celular é afetado. Cav1.2 em neurônios PV+ parece atuar como um freio sobre a ansiedade e o enfrentamento passivo, enquanto seu papel em neurônios excitatórios sustenta um estilo diferente, mais ativo, de resposta ao estresse. Em vez de um gene “bom” ou “ruim”, CACNA1C surge como um regulador dependente do contexto, incorporado em circuitos cerebrais distintos. Para pessoas com transtornos psiquiátricos relacionados a esse gene, esses resultados sugerem que terapias futuras podem precisar direcionar populações celulares ou nós de circuito específicos, em vez de bloquear ou potencializar Cav1.2 de forma difusa por todo o cérebro.
Citação: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
Palavras-chave: ansiedade, enfrentamento do estresse, neurônios de parvalbumina, CACNA1C, comportamento de camundongo