Clear Sky Science · pl
Deficyt Cacna1c w neuronach ekspresjonujących parwalbuminę sprzyja lękowi i biernemu radzeniu sobie ze stresem
Dlaczego drobne przełączniki mózgowe mają znaczenie dla stresu i lęku
Lęk i sposób, w jaki radzimy sobie ze stresem, mogą wydawać się wyłącznie efektem osobowości lub doświadczeń życiowych. Tymczasem głęboko w mózgu wyspecjalizowane komórki działają jak mikroskopijne przełączniki, które pomagają zdecydować, czy zastygnąć, poddać się, czy aktywnie stawić czoła wyzwaniu. W tym badaniu zbadano jeden z takich przełączników: białkowy kanał wapniowy Cav1.2, kodowany przez gen CACNA1C, w szczególnej grupie komórek hamujących. Wyłączając to białko wyłącznie w tych komórkach u myszy, badacze pokazują, jak subtelne zmiany w połączeniach mózgowych mogą przesunąć zachowanie w stronę lęku i biernego radzenia sobie, dostarczając wskazówek dla przyszłych, bardziej celowanych terapii zaburzeń psychiatrycznych.
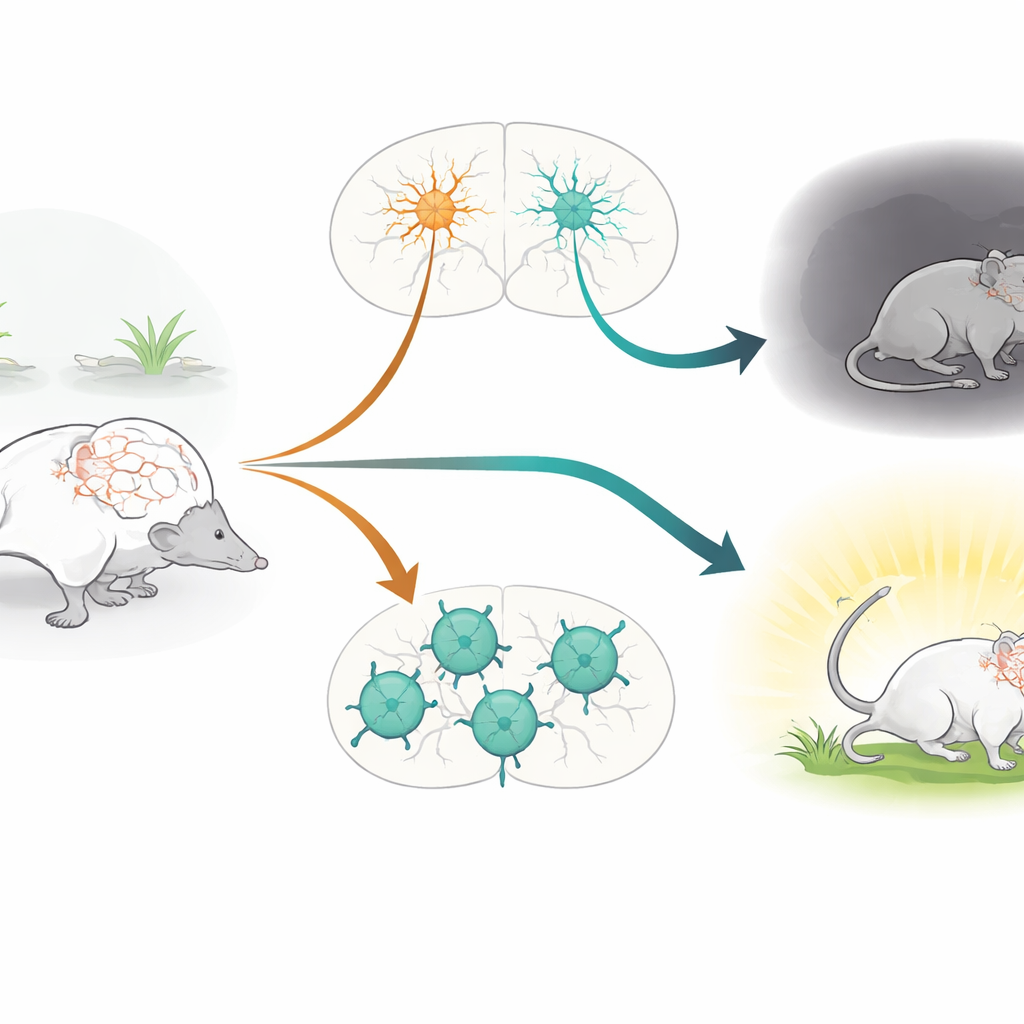
Stróżowie rytmu mózgu
Praca koncentruje się na neuronach pozytywnych na parwalbuminę (PV+), klasie szybko wyładowujących się komórek hamujących, które pełnią rolę stróżów rytmu w mózgu. Te komórki pomagają utrzymać delikatną równowagę między pobudzeniem a hamowaniem, kształtując rytmy mózgowe leżące u podstaw uwagi, pamięci i emocji. Neurony PV+ od dawna wiązane są ze schorzeniami takimi jak schizofrenia, depresja, autyzm i padaczka. Równocześnie gen CACNA1C, kodujący kanał wapniowy Cav1.2, jest jednym z najbardziej konsekwentnie identyfikowanych czynników ryzyka genetycznego w różnych zaburzeniach psychiatrycznych. Kanały Cav1.2 umożliwiają przepływ jonów wapnia do komórek podczas ich aktywności, wpływając na to, jak się rozwijają, łączą i dostosowują swoją siłę w czasie. Mimo to specyficzna rola Cav1.2 w neuronach PV+ nie została dotąd bezpośrednio przetestowana u żywych zwierząt.
Tworzenie myszy z celowanymi zmianami
Aby wydzielić to pytanie, badacze zmodyfikowali myszy tak, by Cav1.2 był selektywnie usunięty tylko z neuronów PV+, pozostawiając inne typy komórek nietknięte. Użyli systemu genetycznego, który aktywuje enzym tnący (Cre) specyficznie w komórkach PV+, usuwając tam gen Cacna1c. Do rybosomów dodano znacznik molekularny, by potwierdzić, gdzie zaszła rekombinacja, co potwierdziło skuteczne skierowanie na regiony bogate w PV, takie jak kora, hipokamp, ciało migdałowate i móżdżek. Myszy poddano następnie obszernej baterii testów behawioralnych oceniających podstawowe poruszanie się, zachowania lękowe, interakcje społeczne, uczenie się i pamięć oraz reakcję na nieunikniony stresor.
Zaniepokojone, ale poznawczo nienaruszone
Myszy pozbawione Cav1.2 w neuronach PV+ wykazywały wyraźny wzrost zachowań przypominających lęk. W standardowych testach, w których zwierzęta wybierają między bezpiecznymi, ciemnymi lub osłoniętymi obszarami a bardziej odsłoniętymi, jasno oświetlonymi przestrzeniami, zmodyfikowane myszy silniej unikały otwartych lub oświetlonych stref niż ich normalne rodzeństwo, choć ich ogólny poziom aktywności ruchowej nie uległ zmianie. Co ciekawe, te same myszy radziły sobie normalnie w szerokim zakresie zadań badających preferencje społeczne, rozpoznawanie nowych obiektów, pamięć przestrzenną oraz naukę lokalizacji ukrytej platformy w labiryncie wodnym. Sugeruje to, że przynajmniej w tym modelu Cav1.2 w neuronach PV+ jest szczególnie istotny dla regulacji emocji i reakcji na stres, a niekoniecznie dla zdolności społecznych czy poznawczych.
Przeciwstawne style radzenia sobie ze stresem wynikające z różnych typów komórek
Poddane testowi przymusowego pływania, który często służy do badania stylów radzenia sobie ze stresem, myszy z usuniętym Cav1.2 w PV przyjęły bardziej bierną strategię: spędzały mniej czasu na aktywnym pływaniu, a więcej na bezruchu. Wcześniejsze prace tej samej grupy pokazały odwrotny efekt, gdy Cav1.2 usunięto w neuronach pobudzających glutamatergicznych: te myszy angażowały się bardziej aktywnie w radzenie sobie ze stresującą sytuacją. Bezpośrednie porównanie obu modeli potwierdziło ten dwukierunkowy wzorzec. Aby powiązać zachowanie z aktywnością mózgu, zespół zmierzył poziom cFos, markera niedawno aktywowanych neuronów, po teście pływania. Utrata Cav1.2 w neuronach PV+ doprowadziła do zwiększonej aktywności w obszarach takich jak jądro półleżące (nucleus accumbens), boczne habenula i jądro przykomorowe wzgórza (paraventricular thalamus) — regionach związanych z negatywnym nastrojem i przetwarzaniem stresu — podczas gdy usunięcie w neuronach pobudzających zamiast tego zwiększyło aktywność w przegrodzie bocznej, obszarze zaangażowanym w regulację emocji i odporność.
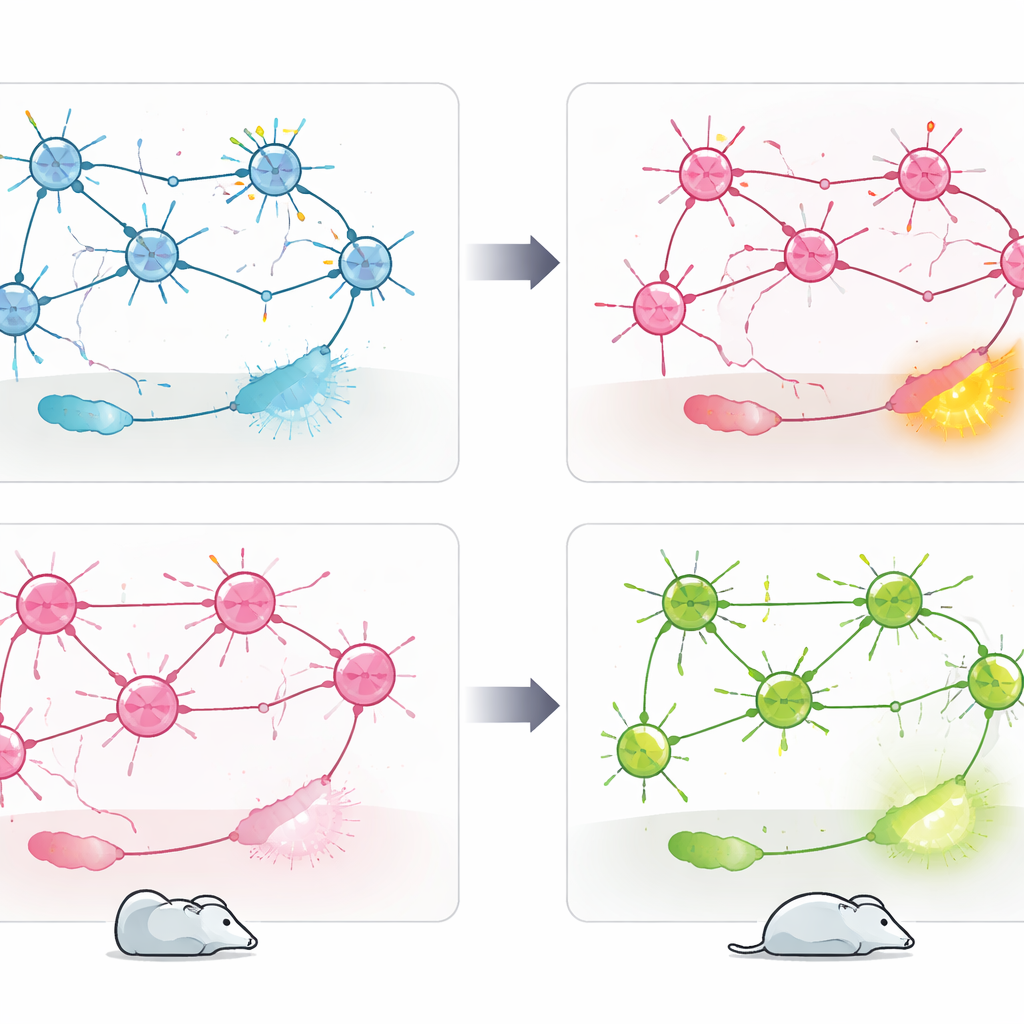
Co to oznacza dla przyszłych terapii
Łącznie wyniki pokazują, że ten sam gen ryzyka, CACNA1C, może przesuwać zachowania związane ze stresem w przeciwne strony w zależności od tego, który typ komórek zostanie dotknięty. Cav1.2 w neuronach PV+ wydaje się pełnić rolę hamulca dla lęku i biernego radzenia sobie, podczas gdy jego rola w neuronach pobudzających sprzyja innemu, bardziej aktywnemu stylowi reagowania na stres. Zamiast jednego „dobrego” lub „złego” genu, CACNA1C wyłania się jako regulator zależny od kontekstu, osadzony w odrębnych obwodach mózgowych. Dla osób żyjących z zaburzeniami psychiatrycznymi powiązanymi z tym genem wyniki sugerują, że przyszłe terapie mogą wymagać ukierunkowania na konkretne populacje komórek lub węzły obwodów, zamiast szerokiego blokowania lub wzmacniania Cav1.2 w całym mózgu.
Cytowanie: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
Słowa kluczowe: lęk, radzenie sobie ze stresem, neurony parwalbuminowe, CACNA1C, zachowanie myszy