Clear Sky Science · ar
نقص Cacna1c في الخلايا المعبرة عن بارفالبومين يعزز القلق وسلوك التكيف السلبي مع الإجهاد
لماذا تهم مفاتيح الدماغ الصغيرة في الإجهاد والقلق
قد يبدو القلق وطريقة تعاملنا مع الإجهاد نتاج شخصية أو تجارب الحياة وحدها. ومع ذلك، داخل الدماغ توجد خلايا متخصصة تعمل كمفاتيح مجهرية تساعد في تقرير ما إذا كنا نتجمد، نستسلم، أم نقاتل بنشاط لمواجهة تحدٍ ما. تستعرض هذه الدراسة أحد هذه المفاتيح: بروتين قناة كالسيوم يُدعى Cav1.2، المُنتَج بواسطة جين CACNA1C، في مجموعة معينة من الخلايا المثبطة في الدماغ. من خلال إيقاف عمل هذا البروتين فقط في تلك الخلايا لدى الفئران، يكشف الباحثون كيف أن تغييرات دقيقة في توصيلات الدماغ قد تزيح السلوك نحو القلق والتكيف السلبي، ما يقدّم دلائل لعلاجات مستقبلية أكثر استهدافًا للاضطرابات النفسية.
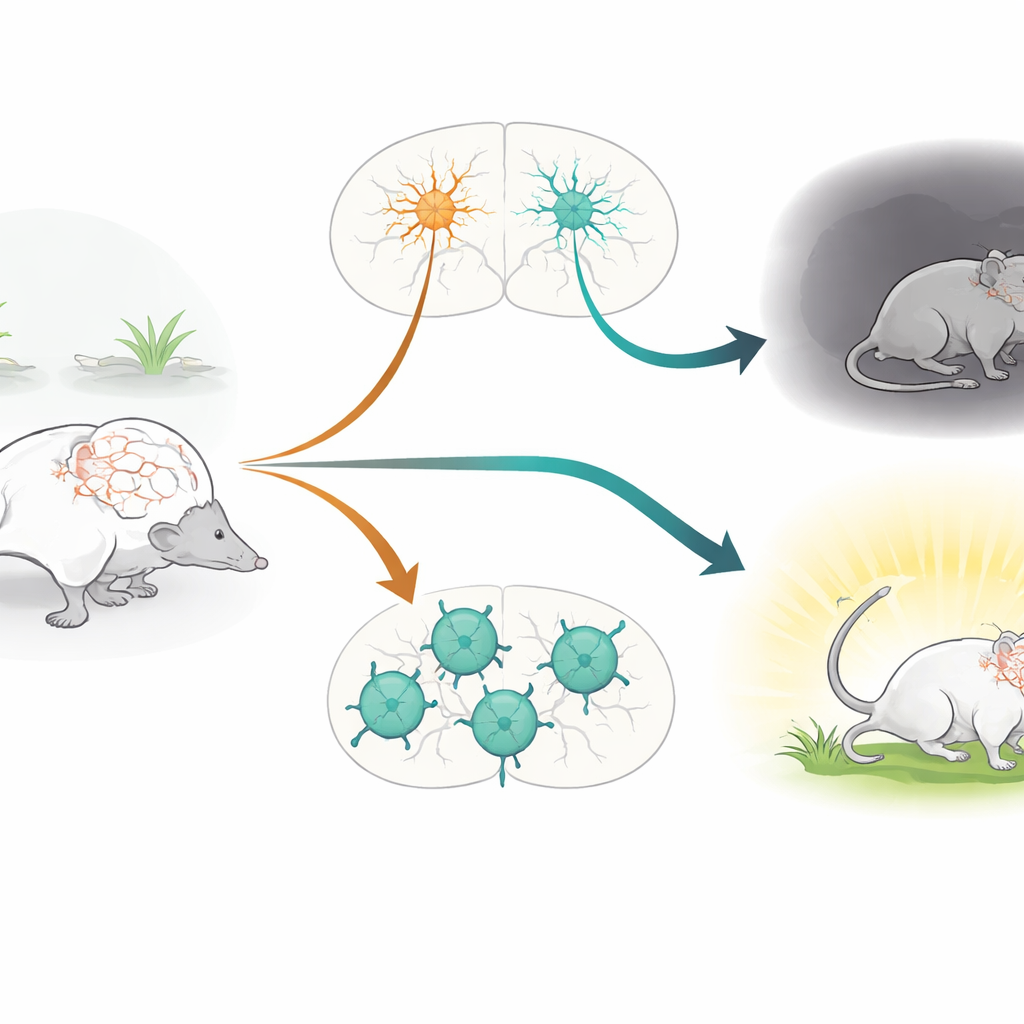
حافظو إيقاع الدماغ
تركز الدراسة على الخلايا الإيجابية لبارفالبومين (PV+)، وهي فئة من الخلايا المثبطة سريعة الإطلاق التي تعمل كحافظات للإيقاع في الدماغ. تساعد هذه الخلايا على الحفاظ على توازن دقيق بين التحفيز والتثبيط، وتشكل إيقاعات دماغية تدعم الانتباه والذاكرة والعاطفة. ارتبطت خلايا PV+ منذ زمن بحالات مثل الفصام والاكتئاب والتوحد والصرع. وفي الوقت نفسه، يعد جين CACNA1C، الذي يشفر قناة الكالسيوم Cav1.2، واحدًا من عوامل الخطر الوراثية التي تكررت عبر عدة اضطرابات نفسية. تسمح قنوات Cav1.2 لأيونات الكالسيوم بالدخول إلى الخلايا عند نشاطها، مما يؤثر في كيفية تطورها واتصالها وتعديل قوتها على مدى الزمن. ومع ذلك، لم يتم اختبار الدور المحدد لـ Cav1.2 داخل خلايا PV+ مباشرة في حيوانات حية من قبل.
هندسة فئران بتعديلات مستهدفة
لعزل هذا السؤال، هندس الباحثون فئرانًا أُزيلت فيها قناة Cav1.2 انتقائيًا من خلايا PV+ فقط، تاركين أنواع الخلايا الأخرى دون تغيير. استخدموا نظامًا جينيًا ينشط إنزيم "القص" (Cre) خصيصًا في خلايا PV+، ليحذف جين Cacna1c هناك. أضيف وسم جزيئي إلى الريبوسومات للتحقق من مكان حدوث إعادة التركيب هذه، مؤكّدين استهداف مناطق غنية بـ PV مثل القشرة، والحُصين، والمِهاد اللوزي، والمخيخ بشكل فعّال. ثم خضعت الفئران لسلسلة واسعة من اختبارات السلوك التي قيّمت الحركة الأساسية، والسلوك الشبيه بالقلق، والتفاعل الاجتماعي، والتعلّم والذاكرة، وكيف استجابوا لمُسبّب إجهاد لا مفر منه.
قلق لكن سليم ذهنيًا
أظهرت الفئران التي تفتقر إلى Cav1.2 في خلايا PV+ زيادة واضحة في السلوك الشبيه بالقلق. في الاختبارات القياسية التي يختار فيها الحيوان بين مناطق آمنة ومظلمة أو محمية وبين مساحات مكشوفة ومضاءة، تجنبت الفئران المعدّلة المناطق المفتوحة أو المضيئة بقوة أكبر من نظرائها الطبيعيين، رغم أن مستويات حركتها العامة لم تتغير. ولافت أن هذه الفئران نفسها أدت بشكل طبيعي في مجموعة واسعة من المهمات التي تفحص التفضيل الاجتماعي، والتعرّف على أشياء جديدة، والذاكرة المكانية، وتعلّم موقع منصة مخفية في متاهة مائية. يشير ذلك إلى أن Cav1.2 في خلايا PV+ مهم بالخصوص لتنظيم العاطفة والاستجابات للإجهاد، أكثر منه للقدرات الاجتماعية أو الإدراكية.
أساليب إجهاد متعاكسة من أنواع خلوية مختلفة
عند وضعها في اختبار السباحة القسري، الذي يستخدم غالبًا لدراسة أنماط التكيف مع الإجهاد، تبنّت فئران حذف Cav1.2 المحدد في PV استراتيجية أكثر سلبية: قضت وقتًا أقل في السباحة النشطة ووقتًا أكثر في عدم الحركة. أظهرت أعمال سابقة من نفس المجموعة التأثير المعاكس عند حذف Cav1.2 في الخلايا التحفيزية غلوتاماتية: أصبحت تلك الفئران أكثر انخراطًا بنشاط في مواجهة الموقف المجهد. وأكدت المقارنة المباشرة بين النموذجين هذا النمط ذي الاتجاهين. لربط السلوك بنشاط الدماغ، قاس الفريق تعبير cFos، وهو علامة للخلايا المنشطة مؤخرًا، بعد اختبار السباحة. أدى فقدان Cav1.2 في خلايا PV+ إلى زيادة نشاط في مناطق مثل النواة المتكئة، والهابلولة الجانبية، والمهاد الظنبوبي—مناطق مرتبطة بالمزاج السلبي ومعالجة الإجهاد—بينما أدى الحذف في الخلايا التحفيزية إلى تعزيز النشاط في الحزيمة الجانبية، وهي منطقة تشارك في تنظيم العاطفة والمرونة.
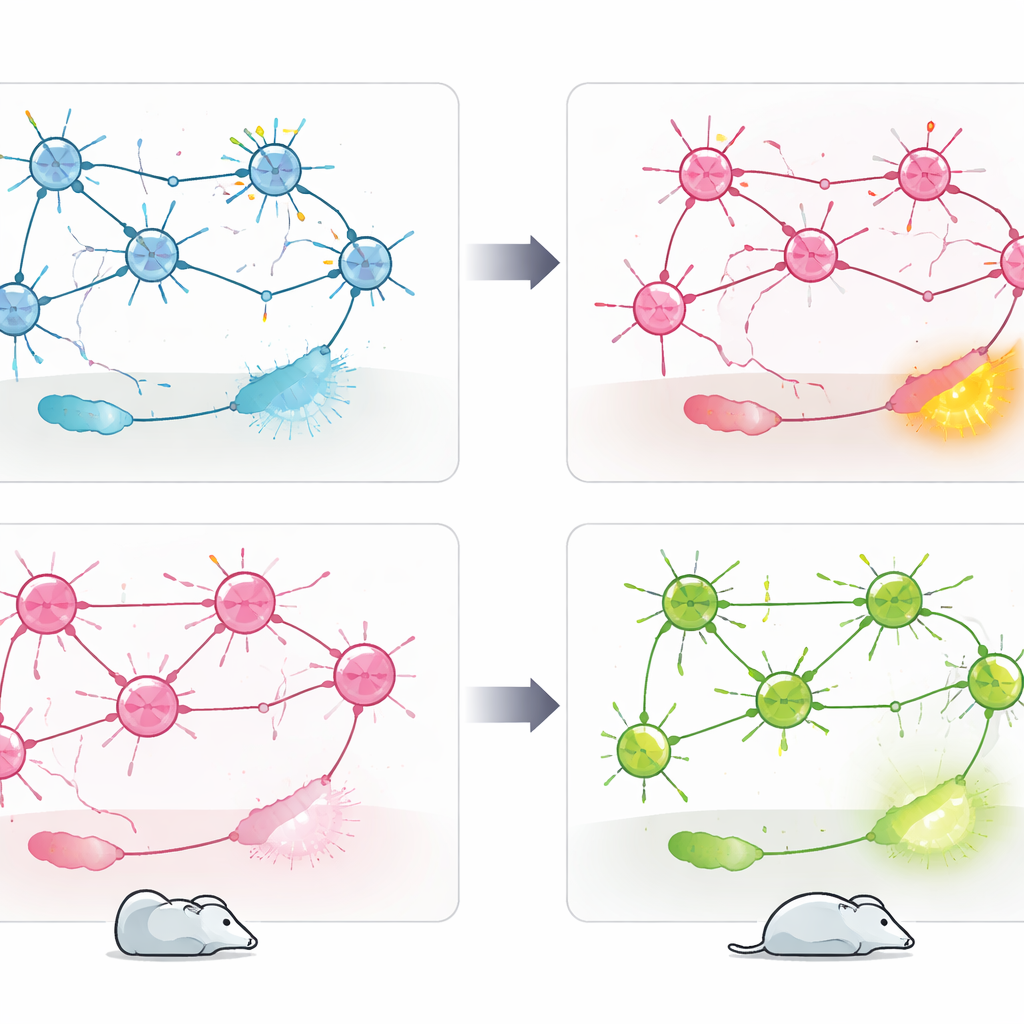
ماذا يعني هذا للعلاجات المستقبلية
بالمجمل، تُظهر النتائج أن نفس جين الخطر، CACNA1C، يمكن أن يدفع سلوك الإجهاد في اتجاهات متعارضة اعتمادًا على نوع الخلايا المتأثرة. يبدو أن Cav1.2 في خلايا PV+ يعمل كفرامل ضد القلق والتكيف السلبي، بينما يدعم دوره في الخلايا التحفيزية أسلوب استجابة مختلفًا وأكثر نشاطًا تجاه الإجهاد. بدلاً من أن يكون جينًا "جيدًا" أو "سيئًا" واحدًا، يظهر CACNA1C كمنظم يعتمد على السياق ومندمج في دوائر دماغية مميزة. للأشخاص الذين يعيشون مع اضطرابات نفسية مرتبطة بهذا الجين، تلمّح هذه النتائج إلى أن العلاجات المستقبلية قد تحتاج إلى استهداف مجموعات خلوية أو عقد دائرية محددة، بدلًا من حجب أو تعزيز Cav1.2 على نطاق واسع في كامل الدماغ.
الاستشهاد: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
الكلمات المفتاحية: القلق, التكيف مع الإجهاد, خلايا بارفالبومين, CACNA1C, سلوك الفأر