Clear Sky Science · it
La carenza di Cacna1c nei neuroni che esprimono parvalbumina favorisce ansia e comportamenti passivi di coping allo stress
Perché i piccoli interruttori cerebrali contano per stress e ansia
L’ansia e il modo in cui affrontiamo lo stress possono sembrare prodotti unicamente della personalità o delle esperienze di vita. Eppure, nelle profondità del cervello, cellule specializzate funzionano come interruttori microscopici che aiutano a decidere se congeliamo, ci arrendiamo o affrontiamo attivamente una sfida. Questo studio esplora uno di questi interruttori: una proteina canale del calcio chiamata Cav1.2, codificata dal gene CACNA1C, in un particolare insieme di cellule inibitorie cerebrali. Disattivando questa proteina solo in quelle cellule nei topi, i ricercatori mostrano come spostamenti sottili nel cablaggio cerebrale possano inclinare il comportamento verso l’ansia e il coping passivo, offrendo indizi per futuri trattamenti più mirati per i disturbi psichiatrici.
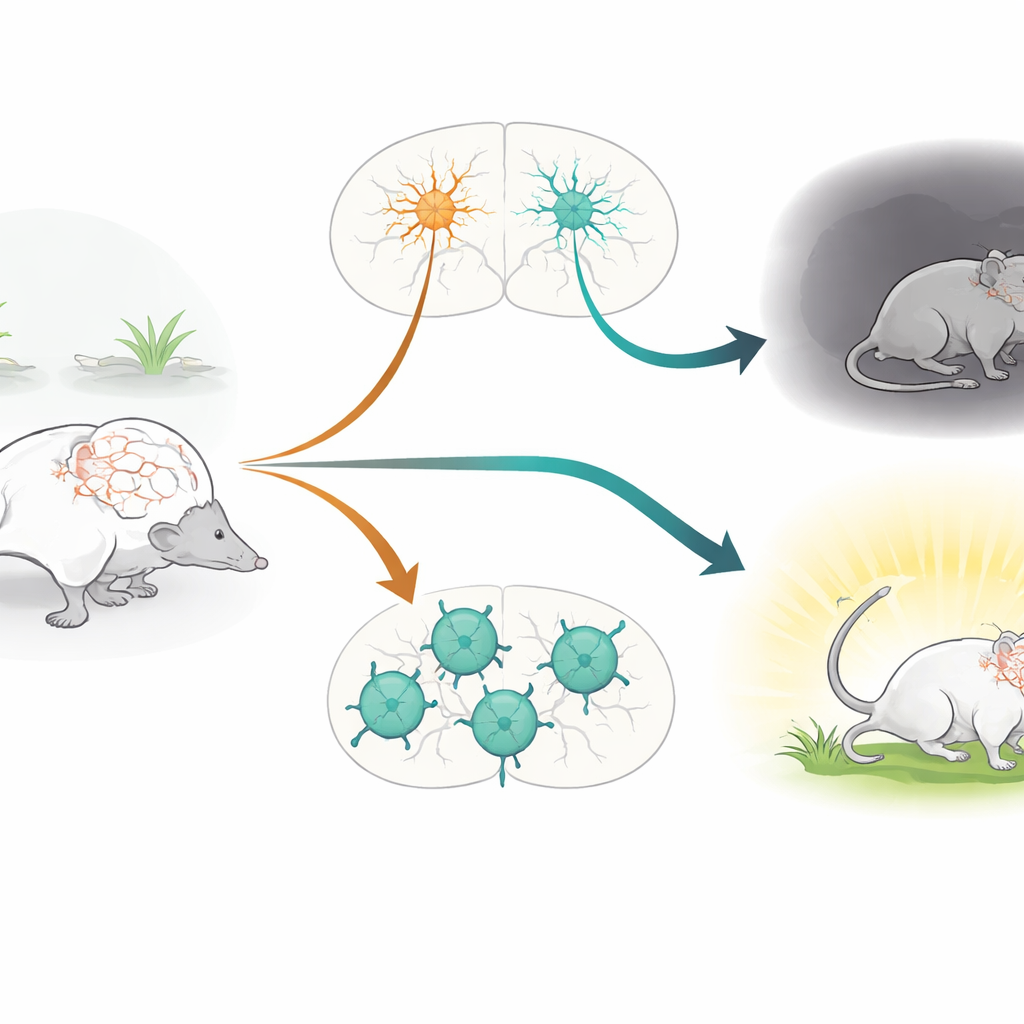
I guardiani del ritmo cerebrale
Il lavoro si concentra sui neuroni positivi per la parvalbumina (PV+), una classe di cellule inibitorie a scarica rapida che agiscono come guardiani del ritmo nel cervello. Queste cellule aiutano a mantenere un delicato equilibrio tra eccitazione e inibizione, modulando i ritmi cerebrali che sottendono attenzione, memoria ed emozione. I neuroni PV+ sono stati implicati a lungo in condizioni quali schizofrenia, depressione, autismo ed epilessia. Allo stesso tempo, il gene CACNA1C, che codifica il canale del calcio Cav1.2, è uno dei fattori di rischio genetico più costantemente identificati in diversi disturbi psichiatrici. I canali Cav1.2 permettono il passaggio di ioni calcio nelle cellule quando queste sono attive, influenzando come si sviluppano, si connettono e modulano la loro forza nel tempo. Nonostante ciò, il ruolo specifico di Cav1.2 all’interno dei neuroni PV+ non era stato testato direttamente in animali viventi.
Creare topi con modifiche mirate
Per isolare questa domanda, i ricercatori hanno ingegnerizzato topi in cui Cav1.2 è stato rimosso selettivamente solo dai neuroni PV+, lasciando intatti gli altri tipi cellulari. Hanno utilizzato un sistema genetico che attiva un enzima «taglia» (Cre) specificamente nelle cellule PV+, cancellando il gene Cacna1c in quelle cellule. È stato aggiunto un marcatore molecolare ai ribosomi per verificare dove si fosse verificata questa ricombinazione, confermando che regioni ricche di PV come corteccia, ippocampo, amigdala e cervelletto sono state efficacemente prese di mira. I topi sono poi stati sottoposti a un ampio batteria di test comportamentali che valutavano il movimento di base, i comportamenti simili all’ansia, l’interazione sociale, l’apprendimento e la memoria, e la loro risposta a uno stress ineludibile.
Ansiosi ma mentalmente intatti
I topi privi di Cav1.2 nei neuroni PV+ hanno mostrato un chiaro aumento dei comportamenti simili all’ansia. Nei test standard in cui gli animali scelgono tra aree sicure, scure o riparate e spazi più esposti, illuminati, questi topi modificati hanno evitato le zone aperte o illuminate più intensamente rispetto ai loro consanguinei normali, pur mantenendo gli stessi livelli complessivi di movimento. In modo sorprendente, tuttavia, gli stessi topi hanno ottenuto punteggi normali in un’ampia gamma di compiti che sondano la preferenza sociale, il riconoscimento di oggetti nuovi, la memoria spaziale e l’apprendimento della posizione di una piattaforma nascosta in un labirinto d’acqua. Ciò suggerisce che, almeno in questo modello, Cav1.2 nei neuroni PV+ è particolarmente importante per la regolazione emotiva e le risposte allo stress, piuttosto che per le capacità sociali o cognitive.
Stili di coping opposti da diversi tipi cellulari
Quando posti nel test dell’immersione forzata, spesso usato per studiare gli stili di coping allo stress, i topi con knockout specifico di Cav1.2 nei PV+ hanno adottato una strategia più passiva: hanno trascorso meno tempo nuotando attivamente e più tempo immobili. Lavori precedenti dello stesso gruppo avevano mostrato l’effetto opposto quando Cav1.2 era stata eliminata nei neuroni eccitatori glutamatergici: quei topi diventavano più attivamente impegnati nell’affrontare la situazione stressante. Il confronto diretto tra i due modelli ha confermato questo schema bidirezionale. Per collegare il comportamento all’attività cerebrale, il team ha misurato cFos, un marcatore di neuroni recentemente attivati, dopo il test di immersione. La perdita di Cav1.2 nei neuroni PV+ ha portato a un aumento dell’attività in aree quali il nucleo accumbens, l’habenula laterale e il talamo paraventricolare—regioni collegate all’umore negativo e all’elaborazione dello stress—mentre la delezione nei neuroni eccitatori ha invece incrementato l’attività nella sezione laterale, una regione coinvolta nella regolazione emotiva e nella resilienza.
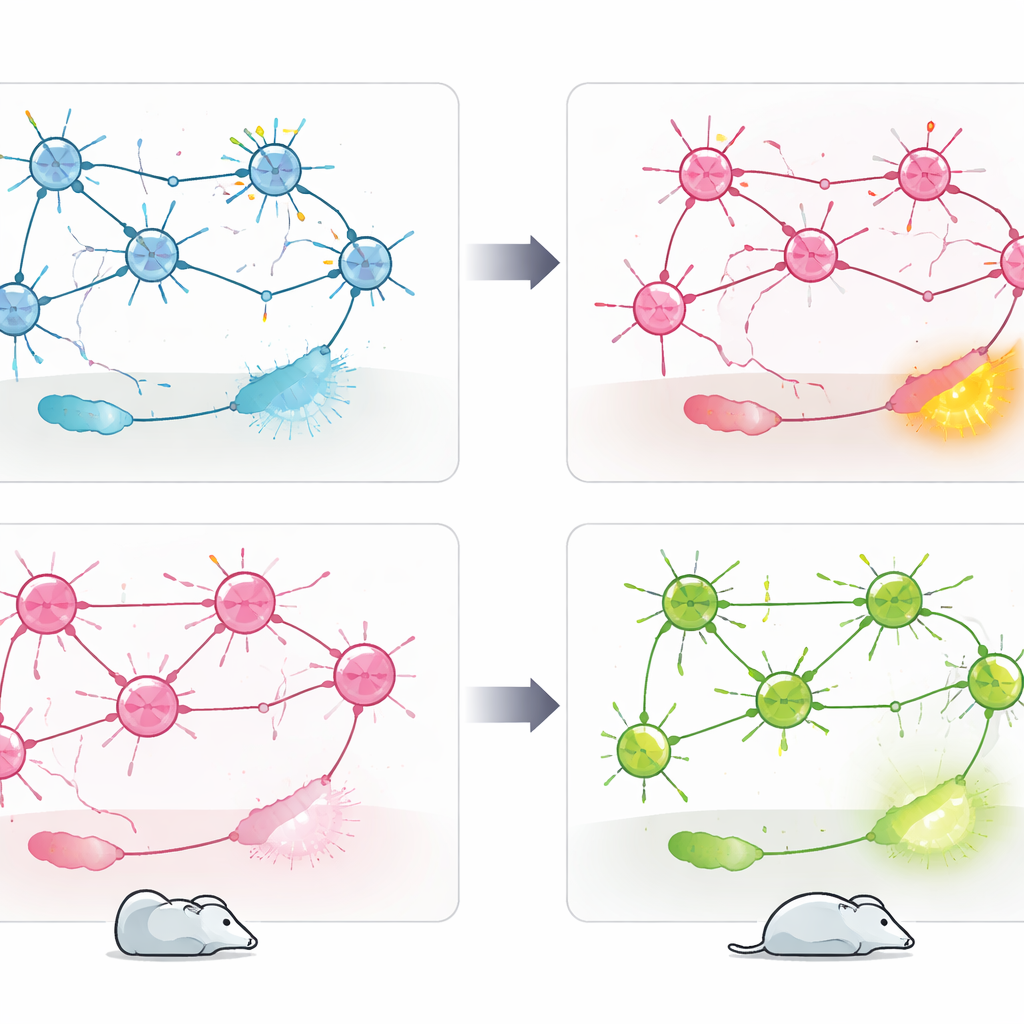
Cosa significa per i trattamenti futuri
Nel complesso, i risultati mostrano che lo stesso gene di rischio, CACNA1C, può spingere il comportamento di fronte allo stress in direzioni opposte a seconda del tipo cellulare coinvolto. Cav1.2 nei neuroni PV+ sembra agire come freno sull’ansia e sul coping passivo, mentre il suo ruolo nei neuroni eccitatori sostiene uno stile di risposta allo stress differente e più attivo. Piuttosto che un singolo gene «buono» o «cattivo», CACNA1C emerge come un regolatore dipendente dal contesto, inserito in circuiti cerebrali distinti. Per le persone che convivono con disturbi psichiatrici legati a questo gene, questi risultati suggeriscono che le terapie future potrebbero dover mirare a popolazioni cellulari o nodi di circuito specifici, invece di bloccare o potenziare in modo generalizzato Cav1.2 in tutto il cervello.
Citazione: Loganathan, S., Zhao, C. & Deussing, J.M. Cacna1c deficiency in parvalbumin-expressing neurons promotes anxiety and passive stress-coping behavior. Sci Rep 16, 12870 (2026). https://doi.org/10.1038/s41598-026-48841-4
Parole chiave: ansia, affrontare lo stress, neuroni parvalbumina, CACNA1C, comportamento dei topi