Clear Sky Science · zh
PLS1基因变体在听力丧失中的致病机制及斑马鱼模型中的功能验证
为何微小的耳内结构重要
听觉依赖于内耳深处成行的显微级毛状突起。当声波使这些毛发生弯曲时,会打开允许带电粒子进入细胞的通道,从而产生大脑解读为声音的信号。本研究考察了塑形这些毛束的蛋白中一个单一基因变化如何扰乱该过程并导致遗传性听力丧失,研究中使用了人类细胞和斑马鱼模型。
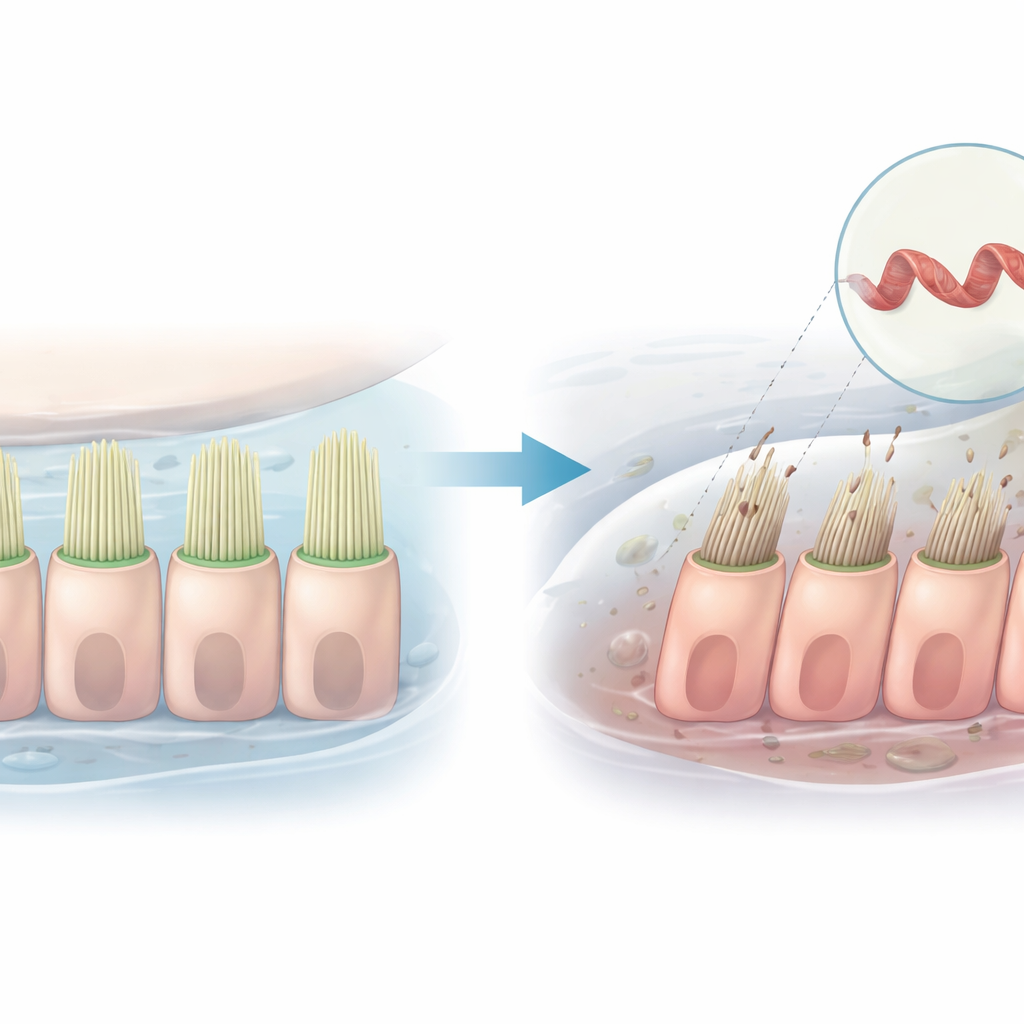
导致声音减弱的基因
该研究聚焦于名为PLS1的基因,它编码plastin 1,这是一种将内耳毛状突起内的细丝捆束在一起的蛋白。携带特定PLS1变体的家族被发现患有进行性、非综合征性听力丧失。在一户中国家庭中,基因中的一个变异导致丢失一小段序列,称为外显子8。受影响的家庭成员在儿童期即开始出现高频听力下降,且随年龄加重,但这一听力衰退的细胞学机制此前尚不清楚。
结构变化如何在细胞内产生连锁反应
Plastin 1具有两个主要的结合内丝区域,在正常情况下,一个区域对另一个区域有调节作用,使捆束保持灵活且有序。团队构建了含或不含外显子8的plastin 1变体并在培养细胞中表达。研究发现,外显子8缺失破坏了这两个区域之间的正常自我相互作用。因此,突变蛋白与内丝及调节运动与张力的伴侣蛋白的结合方式发生改变。对内部支架的三维成像显示,含有突变蛋白的细胞其捆束数量更少、长度更短、直径更细,且整体形态更趋圆润,表明内部结构被扰乱。
对稳定性和互作的影响
科学家还发现,突变的plastin 1更容易被细胞的降解系统标记,这意味着它被更快分解,无法积累到正常水平。与此同时,突变形式对某些关键伴侣的结合更为紧密,包括一种常见的成丝蛋白和一种名为MYO1C的电动蛋白,后者帮助调整毛状突起顶端的张力。实际上,改变后的plastin 1既丧失了一部分常规功能,又干扰了打开和关闭声音感受通道的机械系统的微调。
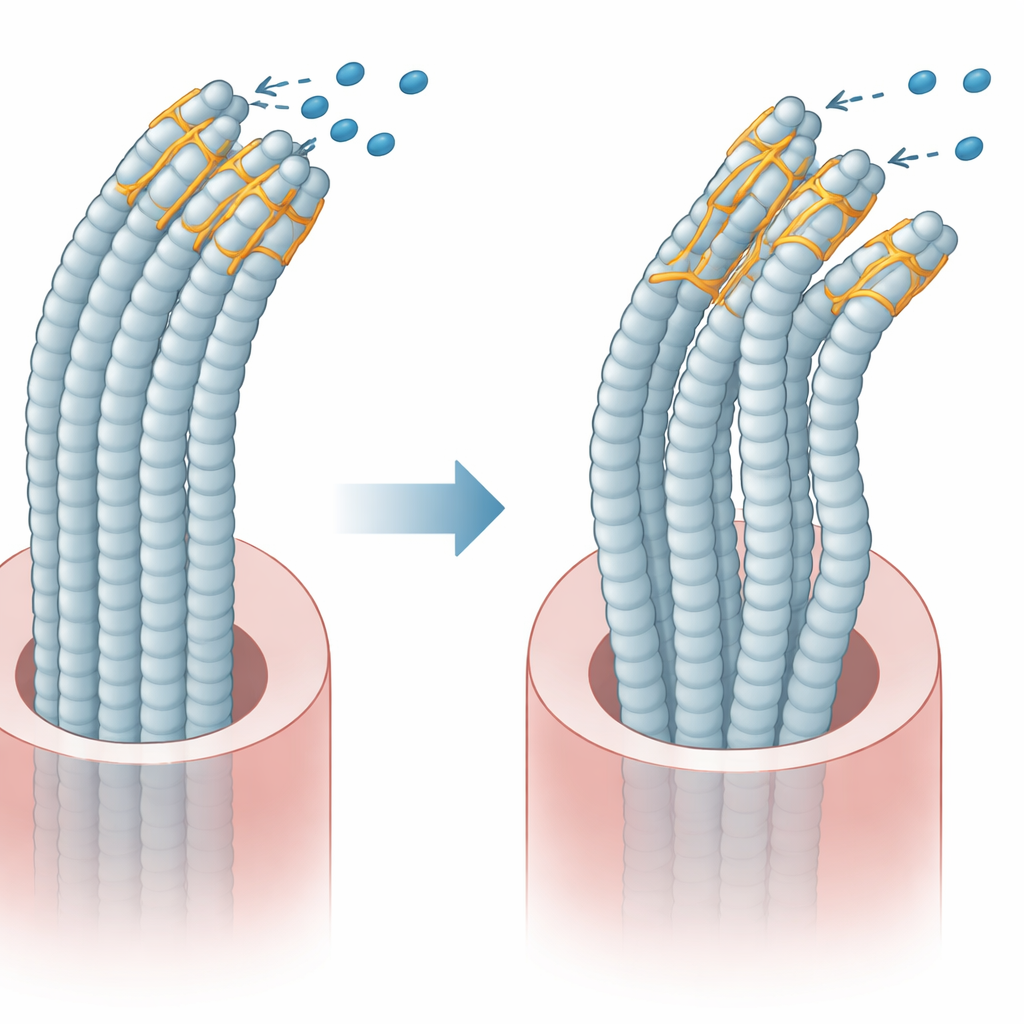
来自斑马鱼耳朵与行为的教训
为了观察这些细胞变化在活体耳朵中的表现,研究者转向斑马鱼,因为其内耳结构和基因与人类非常相似。他们通过基因编辑构建了完全缺失斑马鱼PLS1的个体,并尝试通过补入正常的人类PLS1或缺失外显子8的变体来恢复功能。缺乏PLS1的鱼在内耳囊体和感应运动的微小耳石的大小与形状上出现轻度变化,这些缺陷在补入正常人类基因后大多得到纠正。然而,注入突变人类基因的鱼仍显示结构异常,并且对声音的游动反应不如常人,提示听觉样反应减弱。
通道不再正常打开
随后团队探查了毛细胞表面的关键通道是否正常工作。他们使用一种荧光染料,该染料仅能通过打开的通道进入毛细胞,并测量进入量。表达突变基因的鱼染料摄取明显减少,意味着这些通道较少开启。相比之下,仅缺失PLS1而无突变形式存在的鱼,染料进入量实际上略有增加,仿佛其通道比平常更易打开。这一对比表明,突变蛋白在主动干扰正常通道行为,而不只是简单失去有益功能。
对遗传性听力丧失的意义
综上,细胞和斑马鱼实验表明外显子8的PLS1变体具有双重影响。突变的plastin 1稳定性降低,不能完全履行其在塑造和支撑毛细胞内部框架中的常规作用,但它也异常结合关键伴侣,使控制通道开启的结构变得僵硬或错位。这种复合作用很可能是受影响家族中听力丧失的根源。对于未来治疗,这项工作表明单纯添加更多正常PLS1可能不足以奏效;治疗可能还需要沉默或绕过有害的突变版本以恢复正常的声音感知。
引用: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
关键词: 遗传性听力丧失, PLS1基因, 毛细胞, 斑马鱼模型, 机械传导