Clear Sky Science · nl
Pathogeen mechanisme van de PLS1-genvariant bij gehoorverlies en functionele validatie in een zebravismodel
Waarom kleine structuren in het oor ertoe doen
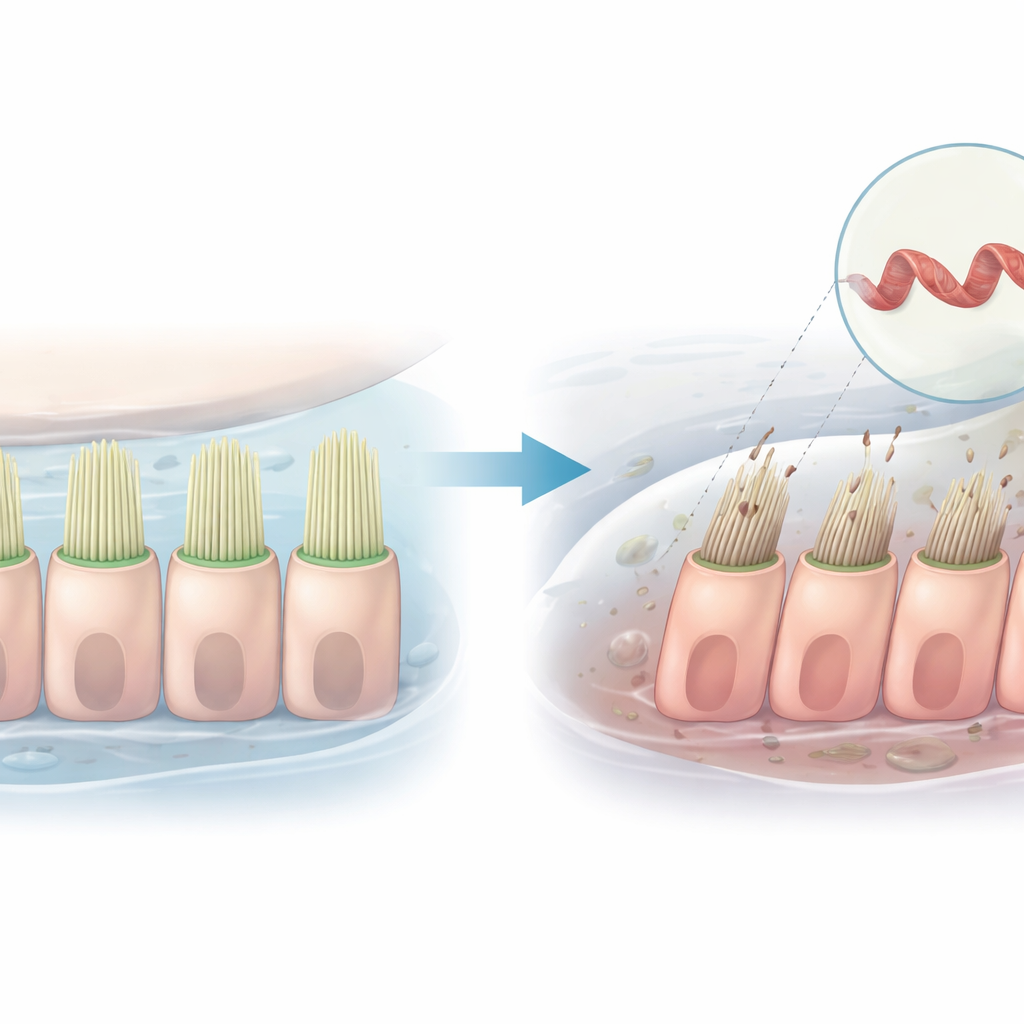
Gehoor berust op rijen microscopisch kleine haarachtige projecties diep in het binnenoor. Wanneer geluidstrillingen deze haren buigen, openen kanalen die geladen deeltjes in de cellen laten stromen en daarmee signalen creëren die de hersenen als geluid interpreteren. Deze studie onderzoekt hoe één genetische verandering in een eiwit dat helpt deze haarbundels te vormen dat proces kan verstoren en tot erfelijk gehoorverlies kan leiden, met zowel menselijke cellen als zebravissen als model.
Een gen achter verzwakt geluid
Het onderzoek richt zich op een gen genaamd PLS1, dat instructies geeft voor het maken van plastine 1, een eiwit dat dunne strengen in de haarachtige projecties van binnenoorschelpen bundelt. Families met een vorm van progressief, niet-syndromisch gehoorverlies bleken specifieke PLS1-varianten te dragen. In één Chinese familie veroorzaakt een wijziging in het gen het verlies van een klein segment, bekend als exon 8. Getroffenen verliezen al in de kinderjaren het gehoor voor hoge tonen en hun gehoor verslechtert met de leeftijd, maar de cellulaire verklaring voor deze achteruitgang was onduidelijk.
Hoe een structurele wijziging doorwerkt in de cel
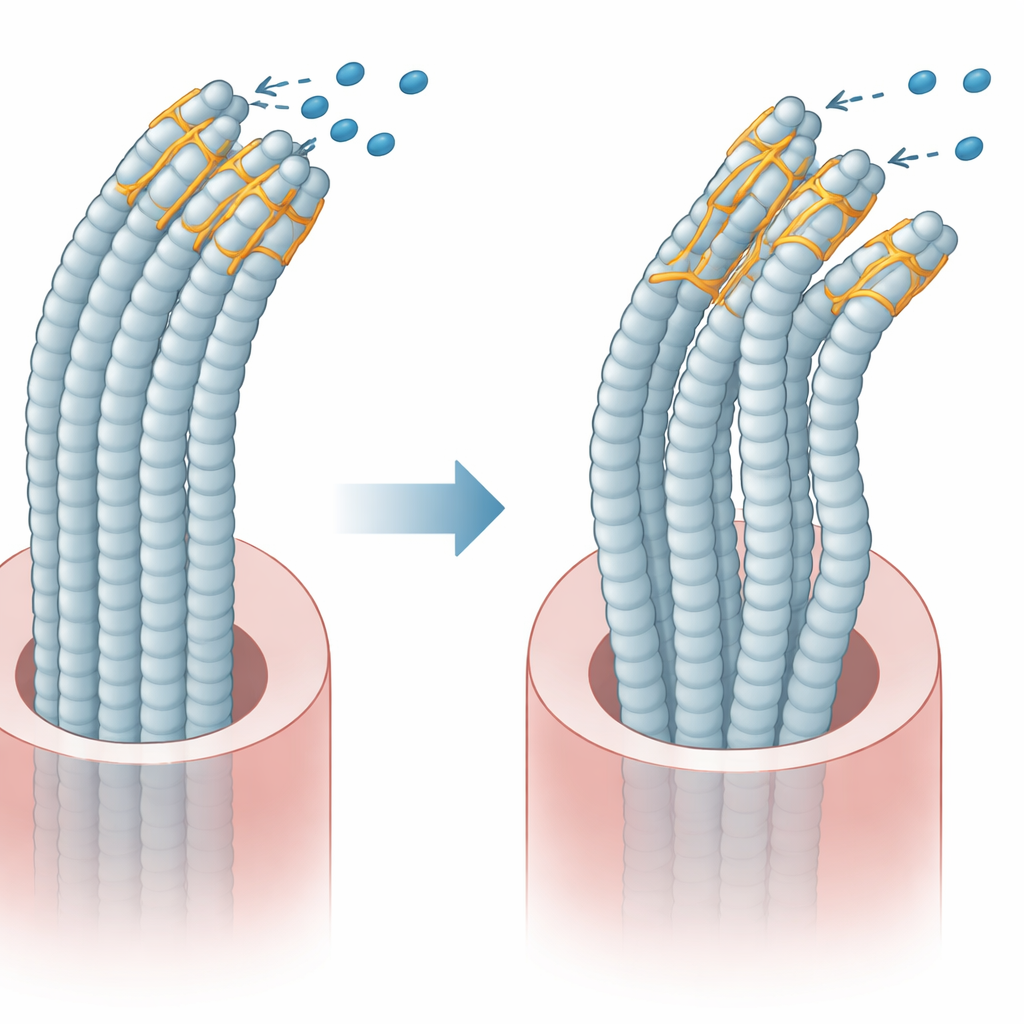
Plastine 1 heeft twee hoofdgebieden die interne strengen vastgrijpen, en onder normale omstandigheden houdt het ene gebied het andere in toom zodat de bundels flexibel en geordend blijven. Het team maakte versies van plastine 1 met en zonder exon 8 en bracht die tot expressie in gekweekte cellen. Ze ontdekten dat de deletie van exon 8 de normale zelfinteractie tussen deze twee gebieden verstoort. Daardoor bindt het gemuteerde eiwit anders aan de interne strengen en aan partner-eiwitten die beweging en spanning helpen regelen. 3D-beelden van het interne skelet toonden aan dat cellen met het gemuteerde eiwit minder, kortere en dunnere bundels hadden en dat hun algemene vorm ronder werd, wat wijst op een verstoorde interne architectuur.
Gevolgen voor stabiliteit en partnerschappen
De wetenschappers vonden ook dat het gemuteerde plastine 1 sterker gemarkeerd wordt voor afbraak door het afvalsysteem van de cel, wat betekent dat het sneller wordt afgebroken en niet tot normale niveaus ophoopt. Tegelijkertijd kleeft de gemuteerde vorm steviger aan bepaalde sleutelpartners, waaronder een veelvoorkomend strengvormend eiwit en een motorproteïne genaamd MYO1C die helpt de spanning aan de toppen van de haarachtige projecties aan te passen. In feite verliest het gewijzigde plastine 1 deels zijn normale functie en verstoort het tegelijkertijd de fijnregeling van het mechanische systeem dat de kanalen voor geluidssensing opent en sluit.
Lessen uit zebravishoorn en gedrag
Om te zien hoe deze cellulaire veranderingen zich in een levend oor uitwerken, richtten de onderzoekers zich op zebravissen, waarvan de binnenoorstructuren en genen opvallend op die van mensen lijken. Ze gebruikten genetische bewerking om vissen te maken die volledig het vis-PLS1 misten en probeerden dat verlies te herstellen door ofwel normaal humaan PLS1 toe te voegen of de exon 8-verwijderde versie. Vissen zonder PLS1 vertoonden milde veranderingen in de grootte en vorm van hun binnenoorsakken en de kleine otolieten die beweging helpen waarnemen, en deze defecten werden grotendeels gecorrigeerd door het normale menselijke gen. Vissen die het gemuteerde menselijke gen kregen, bleven echter structurele afwijkingen vertonen en zwommen minder krachtig als reactie op geluid, wat wijst op verminderde gehoorachtige reacties.
Kanalen die niet langer correct openen
Het team vroeg zich vervolgens af of de sleutelkanalen op de haarcellen goed functioneerden. Ze gebruikten een fluorescerende kleurstof die alleen via open kanalen in haarcellen kan binnendringen en maten hoeveel kleurstof binnenkwam. Vissen die het gemuteerde gen tot expressie brachten hadden merkbaar minder kleurstofopname, wat betekent dat deze kanalen minder vaak openstonden. Daarentegen lieten vissen die simpelweg PLS1 misten, zonder de aanwezigheid van de gemuteerde vorm, juist een lichte toename van kleurstofingang zien, alsof hun kanalen meer open stonden dan normaal. Dit contrast suggereert dat het gemuteerde eiwit actief de normale kanaalwerking stoort, in plaats van alleen nuttige functie te verwijderen.
Wat dit betekent voor erfelijk gehoorverlies
Gezamenlijk wijzen de cel- en zebravisexperimenten op een dubbel effect van de exon 8-PLS1-variant. Het gemuteerde plastine 1 is minder stabiel en kan zijn gebruikelijke rol in het vormen en ondersteunen van het interne framework van haarcellen niet volledig vervullen, maar het bindt ook abnormaal aan sleutelpartners en verstijft of misaligneert de structuren die de kanaalopening regelen. Deze combinatie ligt waarschijnlijk ten grondslag aan het gehoorverlies dat bij getroffen families wordt gezien. Voor toekomstige therapieën suggereert het werk dat het simpelweg toevoegen van meer normaal PLS1 wellicht niet voldoende is; behandelingen zullen mogelijk ook de schadelijke gemuteerde versie moeten uitschakelen of omzeilen om een gezonde geluidsdetectie te herstellen.
Bronvermelding: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Trefwoorden: erfelijk gehoorverlies, PLS1-gen, haarcellen, zebravismodel, mechanotransductie