Clear Sky Science · es
Mecanismo patógeno de la variante del gen PLS1 en la pérdida auditiva y validación funcional en un modelo de pez cebra
Por qué importan las estructuras diminutas del oído
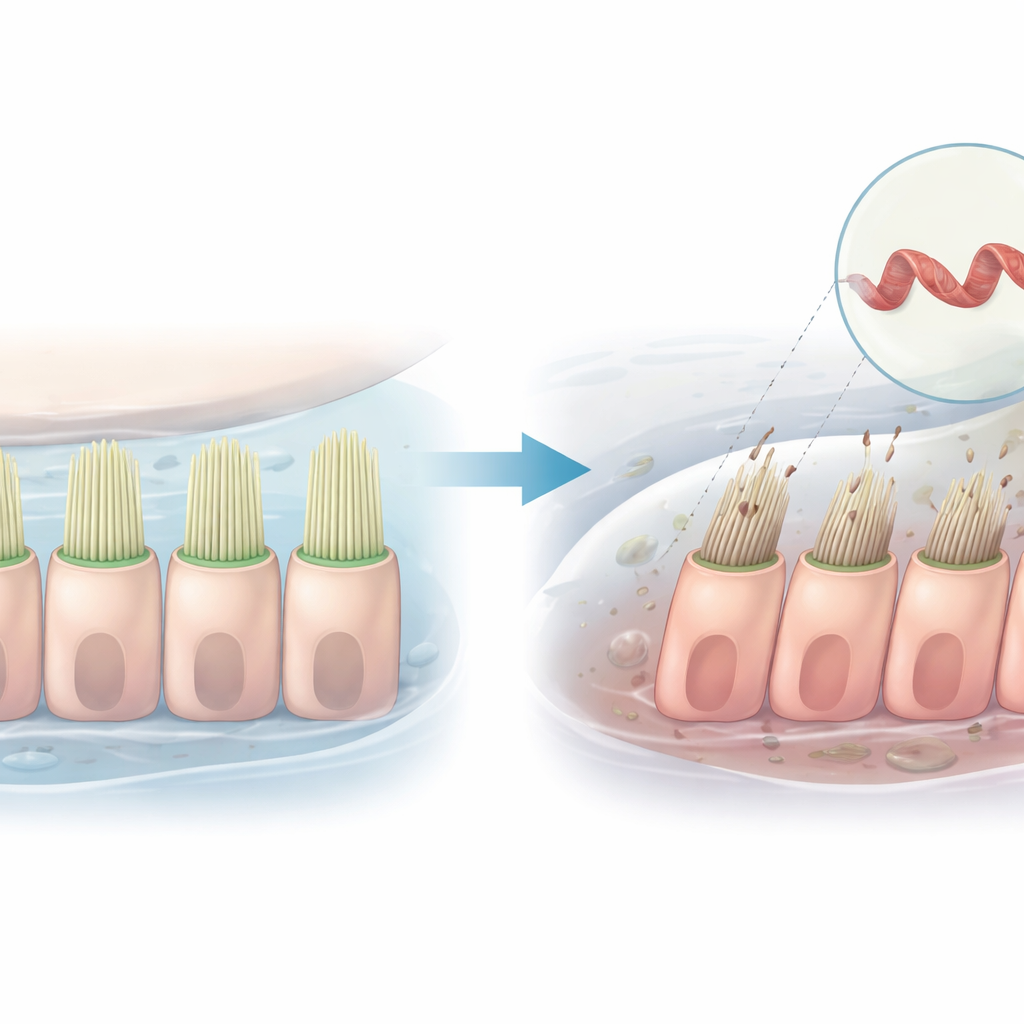
La audición depende de filas de proyecciones microscópicas semejantes a pelos ubicadas en lo profundo del oído interno. Cuando las vibraciones sonoras doblan estos pelos, se abren canales que permiten la entrada de partículas cargadas a las células, generando las señales que nuestro cerebro interpreta como sonido. Este estudio analiza cómo un único cambio genético en una proteína que ayuda a dar forma a estos haces de estereocilios puede perturbar ese proceso y causar pérdida auditiva hereditaria, usando tanto células humanas como el pez cebra como modelos.
Un gen detrás del sonido silenciado
La investigación se centra en un gen llamado PLS1, que codifica plastina 1, una proteína que agrupa filamentos finos dentro de las proyecciones tipo pelo de las células del oído interno. Se han identificado variantes específicas de PLS1 en familias con una forma progresiva y no sindrómica de pérdida auditiva. En una familia china, una alteración del gen causa la pérdida de un pequeño segmento, conocido como exón 8. Los miembros afectados comienzan a perder la audición de tonos agudos en la infancia, y su audición empeora con la edad, pero la razón celular de este deterioro no estaba clara.
Cómo un cambio estructural repercute en la célula
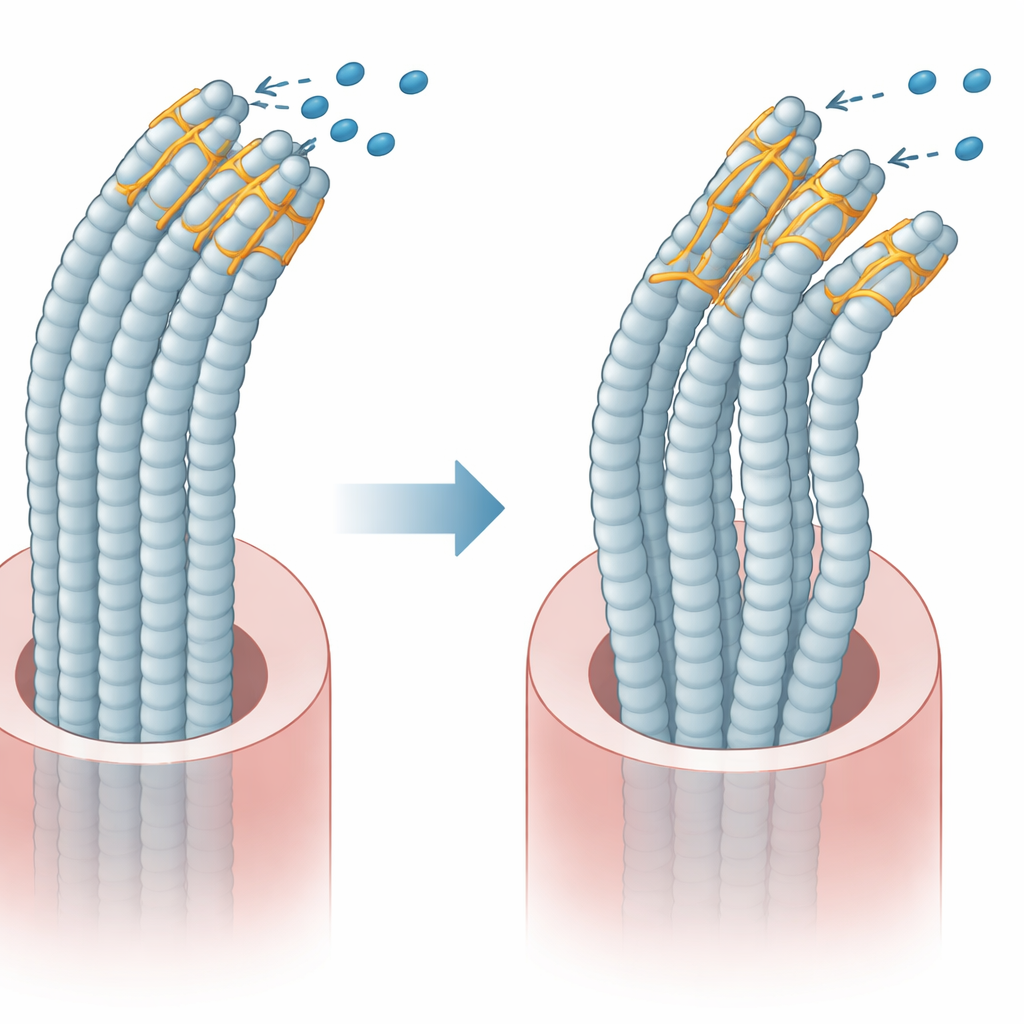
Plastina 1 tiene dos dominios principales que se unen a los filamentos internos, y en condiciones normales un dominio regula al otro para que los haces mantengan flexibilidad y orden. El equipo creó versiones de plastina 1 con y sin el exón 8 y las expresó en células en cultivo. Encontraron que la eliminación del exón 8 altera la interacción normal entre esos dos dominios. Como resultado, la proteína mutante se une de forma diferente a los filamentos internos y a proteínas asociadas que controlan el movimiento y la tensión. Imágenes tridimensionales del andamiaje interno mostraron que las células con la proteína mutante tenían haces más escasos, más cortos y más delgados, y su forma general se volvía más redondeada, lo que indica una arquitectura interna alterada.
Consecuencias para la estabilidad y las interacciones
Los científicos también observaron que la plastina 1 mutante presenta un mayor marcado para su eliminación por el sistema de desecho celular, lo que significa que se degrada más rápido y no alcanza niveles normales. Al mismo tiempo, la forma mutante se une con más fuerza a ciertos socios clave, incluyendo una proteína común formadora de filamentos y una proteína motora llamada MYO1C que ayuda a ajustar la tensión en las puntas de las proyecciones tipo pelo. En efecto, la plastina 1 alterada pierde parte de su función habitual e interfiere con la afinación fina del sistema mecánico que abre y cierra los canales que detectan el sonido.
Lecciones de los oídos y el comportamiento del pez cebra
Para ver cómo se traducen estos cambios celulares en un oído vivo, los investigadores recurrieron al pez cebra, cuyas estructuras y genes del oído interno son notablemente similares a los nuestros. Usaron edición genética para crear peces que carecen por completo de la versión de PLS1 propia del pez y luego intentaron rescatar esta pérdida añadiendo PLS1 humano normal o la versión con la supresión del exón 8. Los peces sin PLS1 mostraron cambios leves en el tamaño y la forma de sus sacos del oído interno y en las pequeñas otolitos que ayudan a detectar el movimiento; estos defectos fueron corregidos en su mayor parte por el gen humano normal. Sin embargo, los peces que recibieron el gen humano mutante continuaron exhibiendo anomalías estructurales y no nadaban con tanta vigorosidad en respuesta al sonido, lo que sugiere respuestas reducidas parecidas a la pérdida auditiva.
Canales que ya no se abren correctamente
El equipo preguntó entonces si los canales clave en las células pilosas funcionaban correctamente. Usaron un tinte fluorescente que solo puede entrar en las células pilosas a través de canales abiertos y midieron cuánto tinte se incorporaba. Los peces que expresaban el gen mutante mostraron una captación de tinte notablemente menor, lo que significa que estos canales eran menos propensos a abrirse. En contraste, los peces que simplemente carecían de PLS1, sin la forma mutante presente, mostraron en realidad un ligero aumento de la entrada de tinte, como si sus canales estuvieran más abiertos de lo normal. Este contraste sugiere que la proteína mutante interfiere activamente con el comportamiento normal de los canales, en lugar de limitarse a eliminar una función beneficiosa.
Qué implica esto para la pérdida auditiva hereditaria
En conjunto, los experimentos en células y en pez cebra apuntan a un doble impacto de la variante en el exón 8 de PLS1. La plastina 1 mutante es menos estable y no puede desempeñar completamente su papel habitual en la conformación y el soporte del andamiaje interno de las células pilosas, pero además se une de forma anómala a socios clave y rigidiza o desalinean las estructuras que controlan la apertura de los canales. Esta combinación probablemente subyace a la pérdida auditiva observada en las familias afectadas. Para terapias futuras, el trabajo sugiere que simplemente aportar más PLS1 normal podría no ser suficiente; los tratamientos podrían necesitar también silenciar o eludir la versión mutante dañina para restaurar una detección sonora saludable.
Cita: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Palabras clave: pérdida auditiva hereditaria, gen PLS1, células pilosas, modelo de pez cebra, mecanotransducción