Clear Sky Science · pl
Mechanizm patogenny wariantu genu PLS1 w utracie słuchu i weryfikacja funkcjonalna w modelu zebraffisha
Dlaczego drobne struktury ucha mają znaczenie
Słyszenie zależy od rzędów mikroskopijnych, włosopodobnych wypustek głęboko w uchu wewnętrznym. Gdy drgania dźwiękowe wyginają te rzęski, otwierają one kanały umożliwiające przepływ naładowanych cząstek do komórek, tworząc sygnały, które mózg interpretuje jako dźwięk. W tym badaniu przyglądamy się, jak pojedyncza zmiana genetyczna w białku kształtującym te pęczki rzęsek może zakłócić ten proces i prowadzić do dziedzicznej utraty słuchu, używając zarówno komórek ludzkich, jak i zebrafishy jako modeli.
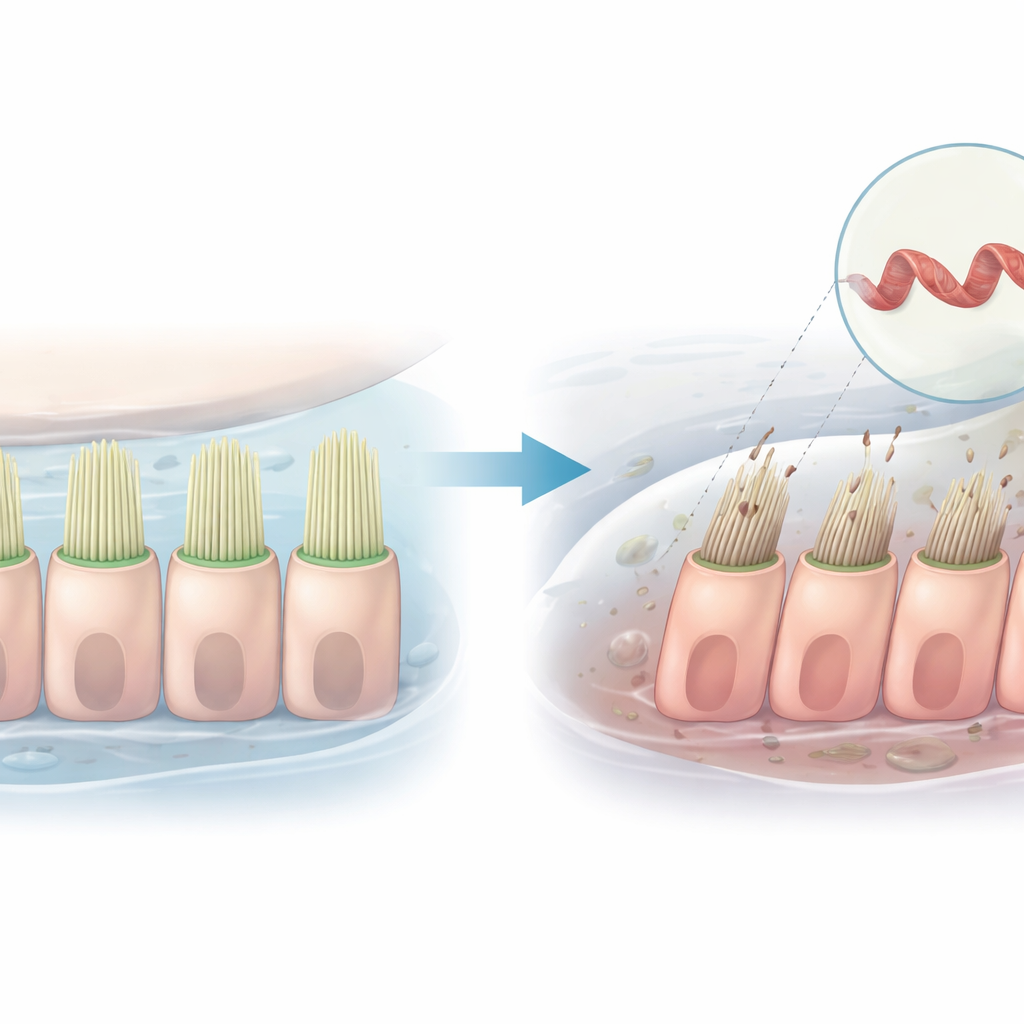
Gen stojący za przyciszonym dźwiękiem
Badania koncentrują się na genie o nazwie PLS1, który zawiera instrukcje do wytwarzania plastyny 1 — białka, które wiąże cienkie włókna wewnątrz włosopodobnych wypustek komórek ucha wewnętrznego. W rodzinach z postępującą, niesyndromową utratą słuchu zidentyfikowano specyficzne warianty PLS1. W jednej chińskiej rodzinie zmiana w genie prowadzi do utraty niewielkiego fragmentu, znanego jako egzon 8. Osoby dotknięte zaczynają tracić słyszenie wysokich częstotliwości w dzieciństwie, a ich słuch pogarsza się z wiekiem, jednak komórkowa przyczyna tego pogorszenia nie była wcześniej jasna.
Jak zmiana strukturalna rozchodzi się w komórce
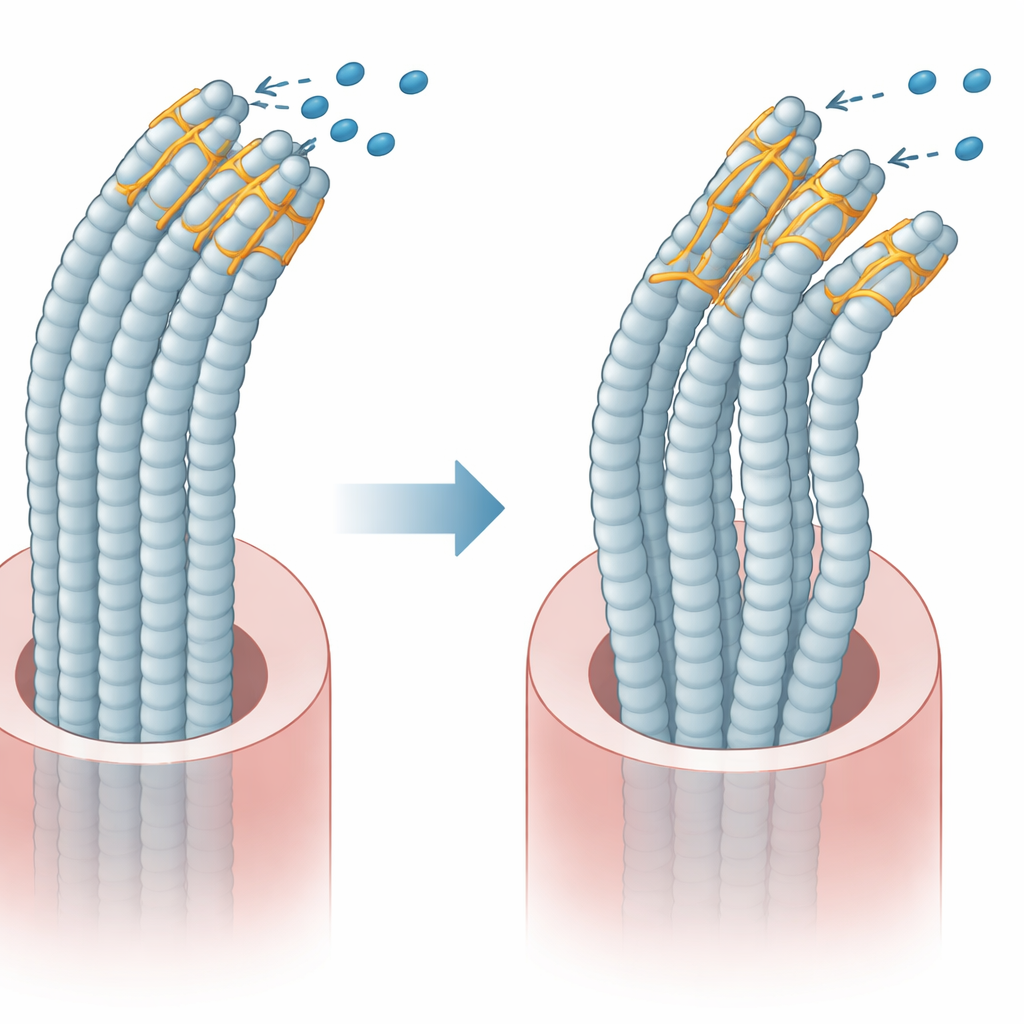
Plastyna 1 ma dwa główne regiony, które wiążą wewnętrzne włókna, a w warunkach normalnych jeden region kontroluje drugi, dzięki czemu pęczki pozostają elastyczne i uporządkowane. Zespół stworzył wersje plastyny 1 z egzonem 8 i bez niego, i wyraził je w hodowanych komórkach. Stwierdzili, że delecja egzonu 8 zaburza normalną wewnętrzną interakcję między tymi regionami. W rezultacie białko z mutacją wiąże się inaczej z włóknami wewnętrznymi oraz z białkami partnerskimi, które pomagają kontrolować ruch i napięcie. Trójwymiarowe obrazowanie wewnętrznego rusztowania wykazało, że komórki z mutantem miały mniej, krótsze i cieńsze pęczki, a ich ogólny kształt stał się bardziej zaokrąglony, co wskazuje na zaburzoną wewnętrzną architekturę.
Konsekwencje dla stabilności i współpracy białek
Naukowcy odkryli także, że mutant plastyny 1 jest silniej oznaczany do usunięcia przez system komórkowego recyklingu, co oznacza, że jest szybciej degradowany i nie gromadzi się na normalnym poziomie. Jednocześnie forma z mutacją silniej przylega do niektórych kluczowych partnerów, w tym powszechnie występującego białka tworzącego włókna oraz motorowego białka MYO1C, które pomaga regulować napięcie na końcach wypustek. W efekcie zmieniona plastyna 1 zarówno traci część swojej zwykłej funkcji, jak i zaburza precyzyjną regulację mechanicznego systemu otwierającego i zamykającego kanały wykrywające dźwięk.
Wnioski z uszu i zachowania zebrafishy
Aby zobaczyć, jak te zmiany komórkowe przekładają się na działanie żywego ucha, badacze sięgnęli po zebrafishy, których struktury ucha wewnętrznego i geny są zaskakująco podobne do naszych. Użyli edycji genów, aby stworzyć ryby, które całkowicie pozbawione są rybiej wersji PLS1, a następnie próbowali odratować ten defekt, dodając albo normalny ludzki PLS1, albo wersję bez egzonu 8. Ryby pozbawione PLS1 wykazały niewielkie zmiany wielkości i kształtu pęcherzyków ucha wewnętrznego oraz drobnych otolitów, które pomagają wyczuwać ruch; defekty te zostały w większości skorygowane przez normalny ludzki gen. Natomiast ryby otrzymujące zmutowany ludzki gen nadal wykazywały nieprawidłowości strukturalne i nie pływały tak energicznie w odpowiedzi na dźwięk, co sugeruje osłabione reakcje przypominające słyszenie.
Kanały, które już się prawidłowo nie otwierają
Zespół sprawdził następnie, czy kluczowe kanały na komórkach rzęsatych działają prawidłowo. Użyli fluorescencyjnego barwnika, który może przeniknąć do komórek rzęsatych tylko przez otwarte kanały, i zmierzyli, ile barwnika weszło. Ryby wyrażające zmutowany gen miały wyraźnie mniejsze wychwycenie barwnika, co oznacza, że kanały były rzadziej otwarte. Dla porównania, ryby jedynie pozbawione PLS1, bez obecności formy zmutowanej, wykazywały w rzeczywistości niewielki wzrost wejścia barwnika, jakby ich kanały były bardziej otwarte niż zwykle. Ten kontrast sugeruje, że zmutowane białko aktywnie zakłóca normalne zachowanie kanałów, zamiast jedynie pozbawiać komórki korzystnej funkcji.
Co to oznacza dla dziedzicznej utraty słuchu
Podsumowując, eksperymenty na komórkach i zebrafishach wskazują na podwójny wpływ wariantu egzonu 8 w PLS1. Zmutowana plastyna 1 jest mniej stabilna i nie może w pełni spełniać swojej zwykłej roli w kształtowaniu i wsparciu wewnętrznego rusztowania komórek rzęsatych, ale jednocześnie wiąże się nieprawidłowo z kluczowymi partnerami i usztywnia bądź przesuwa struktury kontrolujące otwieranie kanałów. To połączenie najpewniej leży u podstaw utraty słuchu obserwowanej w dotkniętych rodzinach. Dla przyszłych terapii wyniki sugerują, że samo dostarczenie większej ilości prawidłowego PLS1 może nie wystarczyć; leczenie może również wymagać wyciszenia lub ominięcia szkodliwej formy zmutowanej, aby przywrócić prawidłowe wykrywanie dźwięku.
Cytowanie: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Słowa kluczowe: dziedziczna utrata słuchu, gen PLS1, komórki rzęsate, model zebrafisha, mechanotransdukcja