Clear Sky Science · sv
Patogen mekanism för PLS1-genvarianten vid hörselnedsättning och funktionell validering i en zebrafiskmodell
Varför små öronstrukturer spelar roll
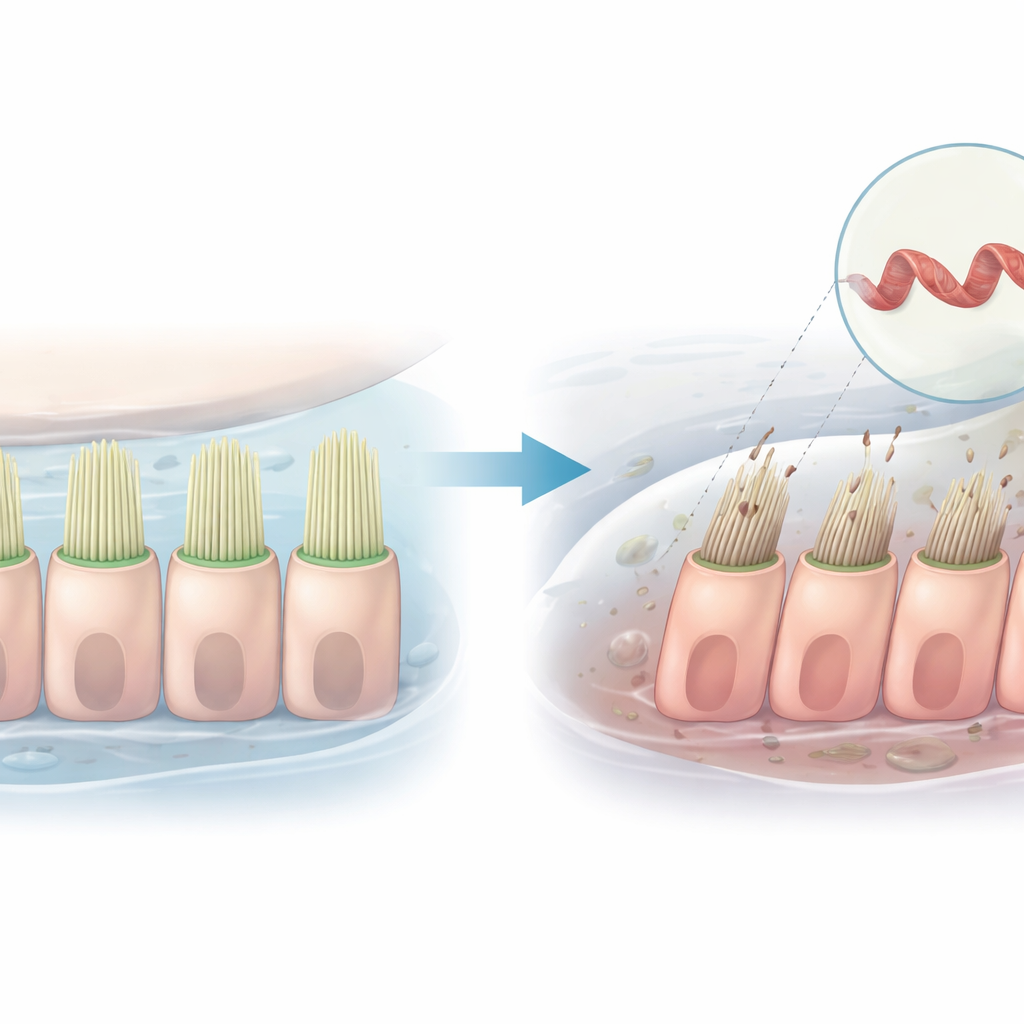
Hörseln beror pr rader av mikroskopiska, hårlika utskott djupt inne i innerörat. När ljudvibrationer böjer dessa hår öppnas kanaler som tillåter laddade partiklar att strömma in i cellerna och skapa de signaler som hjärnan tolkar som ljud. Denna studie undersöker hur en enda genetisk förändring i ett protein som hjälper till att forma dessa hårpenslar kan störa den processen och leda till ärftlig hörselnedsättning, med både mänskliga celler och zebrafisk som modellorganismer.
En gen bakom tystare ljud
Forskningen fokuserar på en gen kallad PLS1, som innehåller instruktioner för att göra plastin 1, ett protein som binder ihop tunna filament i de hårlika utskotten hos innerörats celler. Familjer med en form av progressiv, icke-syndromisk hörselnedsättning har visat sig bära specifika PLS1-varianter. I en kinesisk familj orsakar en förändring i genen förlusten av en liten del, kallad exon 8. Påverkade familjemedlemmar börjar förlora hörseln för höga frekvenser i barndomen, och deras hörsel försämras med åldern, men den cellulära orsaken till denna nedgång hade inte varit klarlagd.
Hur en strukturell förändring sprider sig i cellen
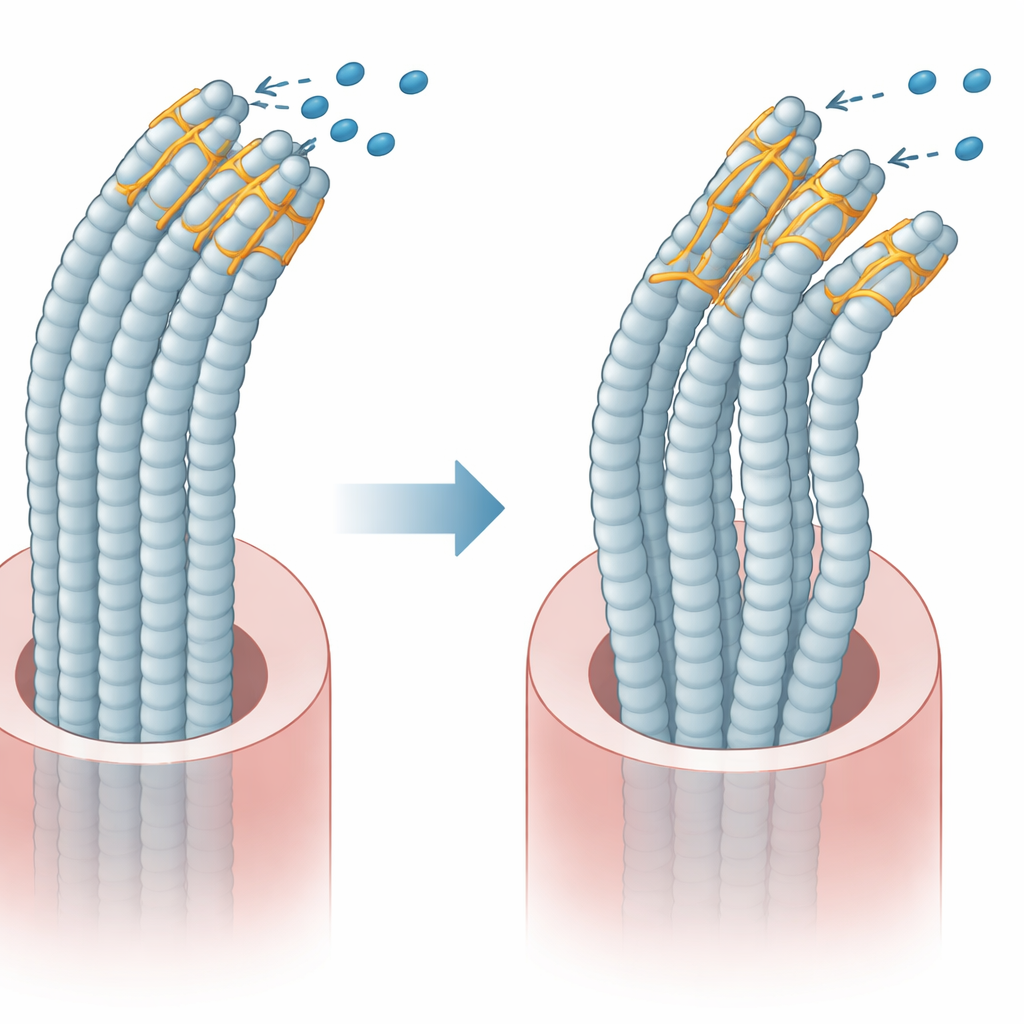
Plastin 1 har två huvudregioner som binder till interna filament, och under normala förhållanden håller en region den andra i schack så att buntarna förblir flexibla och ordnade. Teamet skapade versioner av plastin 1 med och utan exon 8 och uttryckte dem i odlade celler. De fann att exon 8-deletion stör den normala självinteraktionen mellan dessa två regioner. Som ett resultat binder det mutanta proteinet annorlunda till de interna filamenten och till partnerproteiner som hjälper till att kontrollera rörelse och spänning. tredimensionell avbildning av det interna skelettet visade att celler med det mutanta proteinet hade färre, kortare och tunnare buntar, och att deras övergripande form blev mer rundad, vilket pekar på en störd intern arkitektur.
Konsekvenser för stabilitet och partnerskap
Forskarnas analyser visade också att det mutanta plastin 1 i högre grad märkts för nedbrytning av cellens avfallssystem, vilket innebär att det bryts ner snabbare och inte ansamlas till normala nivåer. Samtidigt håller den mutanta formen hårdare i vissa viktiga partners, inklusive ett vanligt filamentbildande protein och ett motorprotein kallat MYO1C som hjälper till att justera spänningen vid spetsarna av de hårlika utskotten. I praktiken förlorar det förändrade plastin 1 både en del av sin vanliga funktion och stör fininställningen av det mekaniska system som öppnar och stänger de ljudkännande kanalerna.
Lärdomar från zebrafisköron och beteende
För att se hur dessa cellulära förändringar yttrar sig i ett levande öra vände forskarna sig till zebrafisk, vars inneröronstrukturer och gener är förvånansvärt lika våra egna. De använde geredigering för att skapa fiskar som helt saknar fiskversionen av PLS1 och försökte sedan rädda denna förlust genom att tillsätta antingen normal mänsklig PLS1 eller exon 8-deletionen. Fiskar utan PLS1 uppvisade milda förändringar i storlek och form på sina inre öronsäckar och de små kalkstenarna (otoliter) som hjälper till att känna rörelse, och dessa defekter korrigerades till stor del av den normala humana genen. Däremot fortsatte fiskar som fick den mutanta humana genen att uppvisa strukturella avvikelser och simmade inte lika livligt som svar på ljud, vilket tyder på nedsatta hörselrelaterade responser.
Kanaler som inte längre öppnar som de ska
Forskarna frågade sedan om de viktiga kanalerna på hårcellerna fungerade korrekt. De använde ett fluorescerande färgämne som bara kan ta sig in i hårceller genom öppna kanaler och mätte hur mycket färg som kom in. Fiskar som uttryckte den mutanta genen hade märkbart lägre upptag av färgämnet, vilket betyder att dessa kanaler öppnades mindre ofta. I kontrast visade fiskar som helt saknade PLS1, utan den mutanta formen närvarande, faktiskt en liten ökning av färgupptaget, som om deras kanaler var mer öppna än vanligt. Denna kontrast tyder på att det mutanta proteinet aktivt stör normal kanalbeteende snarare än bara att ta bort en nyttig funktion.
Vad detta betyder för ärftlig hörselnedsättning
Tillsammans pekar cell- och zebrafiskexperimenten på en dubbel effekt av exon 8-varianten i PLS1. Det mutanta plastin 1 är mindre stabilt och kan inte fullt ut utföra sin vanliga roll i att forma och stödja hårcellernas interna ramverk, men det binder också onormalt till nyckelpartners och gör strukturerna som kontrollerar kanalöppning stelare eller feljusterade. Denna kombination ligger sannolikt bakom hörselnedsättningen som ses i de drabbade familjerna. För framtida terapier antyder arbetet att det kanske inte räcker att bara tillsätta mer normal PLS1; behandlingar kan också behöva tysta eller kringgå den skadliga mutanta versionen för att återställa normal ljuddetektion.
Citering: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Nyckelord: ärftlig hörselnedsättning, PLS1-genen, hårceller, zebrafiskmodell, mekanotransduktion