Clear Sky Science · de
Pathogener Mechanismus der PLS1-Genvariante bei Hörverlust und funktionelle Validierung in einem Zebrafischmodell
Warum winzige Ohrstrukturen wichtig sind
Hören beruht auf Reihen mikroskopischer, haarähnlicher Fortsätze tief im Innenohr. Wenn Schallvibrationen diese Haare biegen, öffnen sich Kanäle, die geladene Teilchen in die Zellen strömen lassen und so die Signale erzeugen, die unser Gehirn als Schall interpretiert. Diese Studie untersucht, wie eine einzelne genetische Veränderung in einem Protein, das diese Haarbündel formt, diesen Prozess stören und zu vererbtem Hörverlust führen kann — unter Verwendung menschlicher Zellen und Zebrafischen als Modelle.
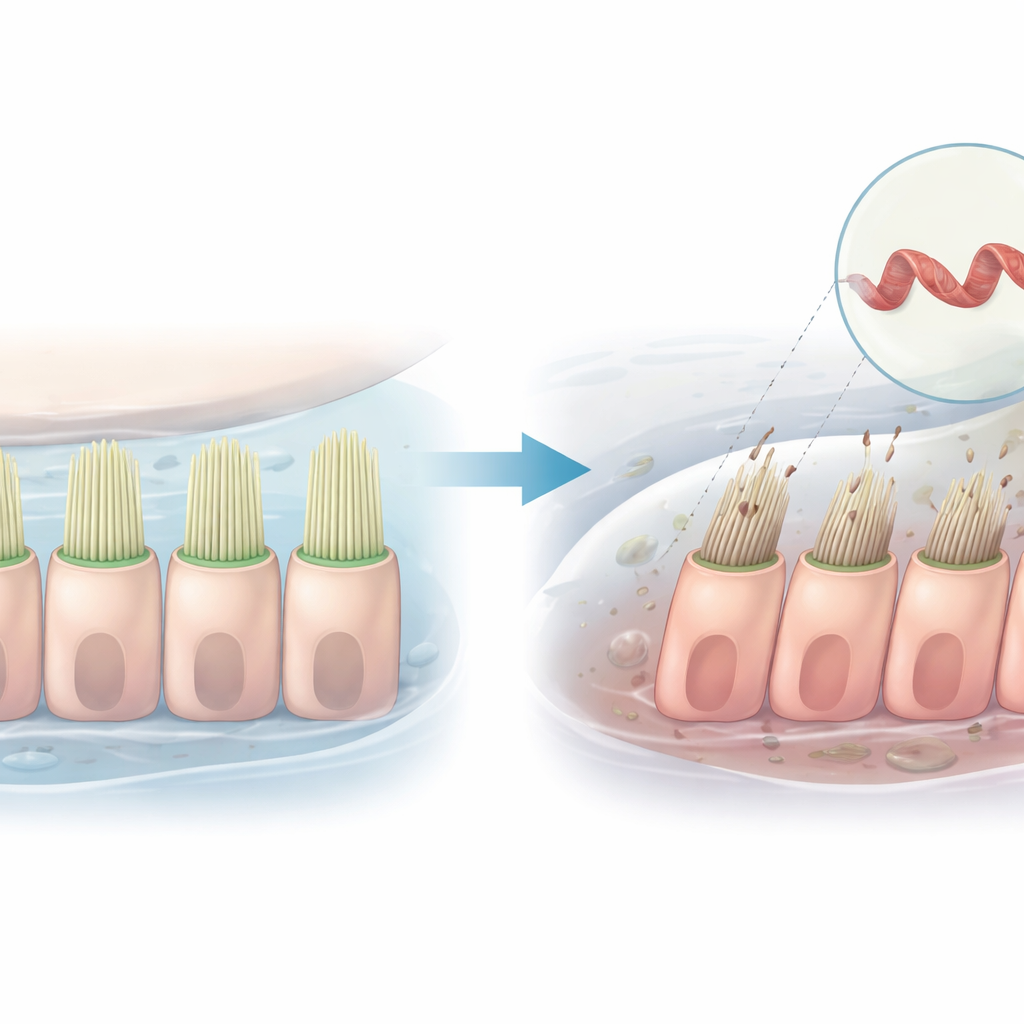
Ein Gen hinter dem Verstummen
Die Untersuchung konzentriert sich auf ein Gen namens PLS1, das die Bauanleitung für Plastin 1 liefert, ein Protein, das schlanke Stränge in den haarähnlichen Fortsätzen der Innenohrzellen zusammenbindet. Familien mit einer Form von fortschreitendem, nicht-syndromalem Hörverlust tragen spezifische PLS1-Varianten. In einer chinesischen Familie führt eine Genveränderung zum Verlust eines kleinen Abschnitts, bekannt als Exon 8. Betroffene Familienmitglieder verlieren in der Kindheit das hochfrequente Hören, und ihr Hörvermögen verschlechtert sich mit dem Alter, doch die zelluläre Ursache dieses Abfalls war nicht klar.
Wie eine strukturelle Änderung die Zelle beeinflusst
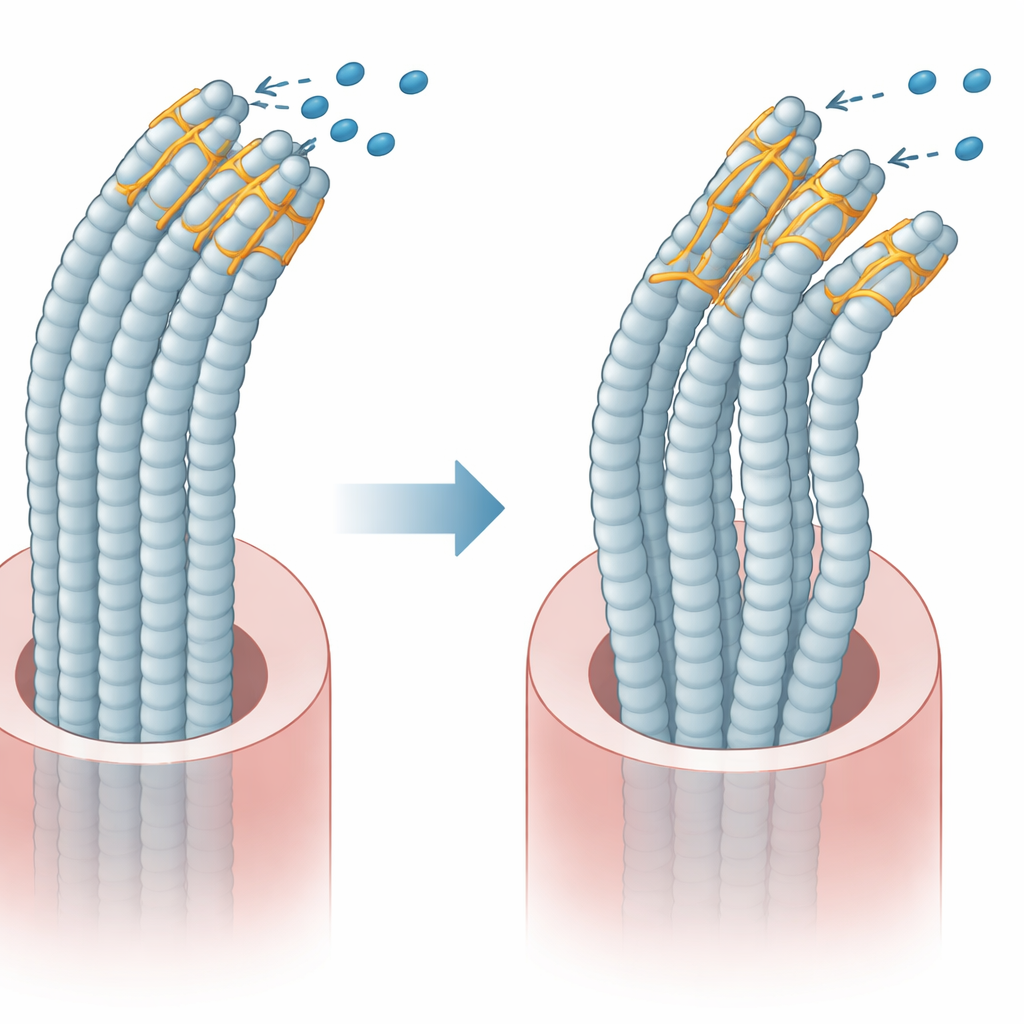
Plastin 1 besitzt zwei Hauptdomänen, die an innere Stränge binden; unter normalen Bedingungen hält eine Domäne die andere in Schach, sodass die Bündel flexibel und geordnet bleiben. Das Team erzeugte Plastin‑1‑Versionen mit und ohne Exon 8 und exprimierte sie in kultivierten Zellen. Sie stellten fest, dass die Exon‑8‑Deletion die normale Wechselwirkung zwischen diesen beiden Domänen stört. Infolgedessen bindet das mutierte Protein anders an die inneren Stränge und an Partnerproteine, die Bewegung und Spannung kontrollieren. Dreidimensionale Aufnahmen des inneren Gerüsts zeigten, dass Zellen mit dem mutierten Protein weniger, kürzere und dünnere Bündel aufwiesen und ihre Gesamtform runder wurde — ein Hinweis auf eine gestörte innere Architektur.
Folgen für Stabilität und Wechselwirkungen
Die Forschenden fanden außerdem heraus, dass das mutierte Plastin 1 stärker für den Abbau durch das zelluläre Entsorgungssystem markiert ist, wodurch es schneller abgebaut wird und nicht in normalen Mengen akkumuliert. Gleichzeitig haftet die mutierte Form enger an bestimmten Schlüsselpartnern, darunter ein häufiges Faserbildendes Protein und ein Motorprotein namens MYO1C, das die Spannung an den Spitzen der haarähnlichen Fortsätze anpasst. Effektiv verliert das veränderte Plastin 1 einen Teil seiner üblichen Funktion und stört zugleich die Feinabstimmung des mechanischen Systems, das die Kanäle zum Schallwahrnehmen öffnet und schließt.
Lehren aus Zebrafischohren und Verhalten
Um zu sehen, wie sich diese zellulären Veränderungen in einem lebenden Ohr auswirken, nutzten die Forschenden Zebrafische, deren Innenohrstrukturen und Gene denen des Menschen bemerkenswert ähneln. Sie erzeugten mittels Geneditierung Fische, die vollständig ohne die Fischversion von PLS1 auskommen, und versuchten dann, diesen Verlust zu retten, indem sie entweder normales humanes PLS1 oder die Exon‑8‑gelöschte Variante einführten. Fische ohne PLS1 zeigten leichte Veränderungen in Größe und Form ihrer Innenohrsäckchen und der winzigen Statolithen, die Bewegung wahrnehmen; diese Defekte wurden größtenteils durch das normale humane Gen korrigiert. Fische, die das mutierte humane Gen erhielten, zeigten jedoch weiterhin strukturelle Auffälligkeiten und reagierten nicht so kräftig auf Schall, was auf eine verringerte hörbezogene Reaktion hindeutet.
Kanäle, die nicht mehr richtig öffnen
Das Team prüfte anschließend, ob die wichtigen Kanäle an den Haarzellen korrekt funktionierten. Sie verwendeten einen fluoreszenten Farbstoff, der nur durch geöffnete Kanäle in Haarzellen eindringen kann, und maßen, wie viel Farbstoff aufgenommen wurde. Fische, die das mutierte Gen exprimierten, hatten deutlich geringere Farbstoffaufnahme, was bedeutet, dass diese Kanäle seltener geöffnet waren. Im Gegensatz dazu zeigten Fische, denen PLS1 schlicht fehlte, ohne dass die mutierte Form vorhanden war, tatsächlich einen leichten Anstieg der Farbstoffaufnahme, als wären ihre Kanäle offener als üblich. Dieser Kontrast deutet darauf hin, dass das mutierte Protein aktiv in das normale Kanalverhalten eingreift, statt nur eine hilfreiche Funktion zu verlieren.
Was das für vererbten Hörverlust bedeutet
Zusammenfassend deuten Zell‑ und Zebrafischexperimente auf eine doppelte Wirkung der Exon‑8‑PLS1‑Variante hin. Das mutierte Plastin 1 ist weniger stabil und kann seine übliche Rolle beim Formen und Stabilisieren des inneren Gerüsts der Haarzellen nicht vollständig erfüllen; zugleich bindet es abnormal an Schlüsselpartner und versteift oder fehlordnet die Strukturen, die das Kanalöffnen steuern. Diese Kombination liegt vermutlich dem in betroffenen Familien beobachteten Hörverlust zugrunde. Für künftige Therapien legt die Arbeit nahe, dass das bloße Hinzufügen von normalem PLS1 möglicherweise nicht ausreicht; Behandlungen müssen möglicherweise auch die schädliche mutierte Version stilllegen oder umgehen, um eine gesunde Schallwahrnehmung wiederherzustellen.
Zitation: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Schlüsselwörter: erblich bedingter Hörverlust, PLS1-Gen, Haarzellen, Zebrafischmodell, Mechanotransduktion