Clear Sky Science · fr
Mécanisme pathogène de la variante du gène PLS1 dans la surdité et validation fonctionnelle chez le modèle du poisson zèbre
Pourquoi de minuscules structures de l’oreille sont importantes
L’audition repose sur des rangées de projections microscopiques en forme de poils, profondément situées dans l’oreille interne. Lorsque les vibrations sonores fléchissent ces cils, elles ouvrent des canaux qui laissent entrer des particules chargées dans les cellules, générant les signaux que notre cerveau interprète comme du son. Cette étude examine comment un seul changement génétique dans une protéine qui façonne ces faisceaux de stéréocils peut perturber ce processus et conduire à une surdité héréditaire, en utilisant à la fois des cellules humaines et le poisson zèbre comme modèles.
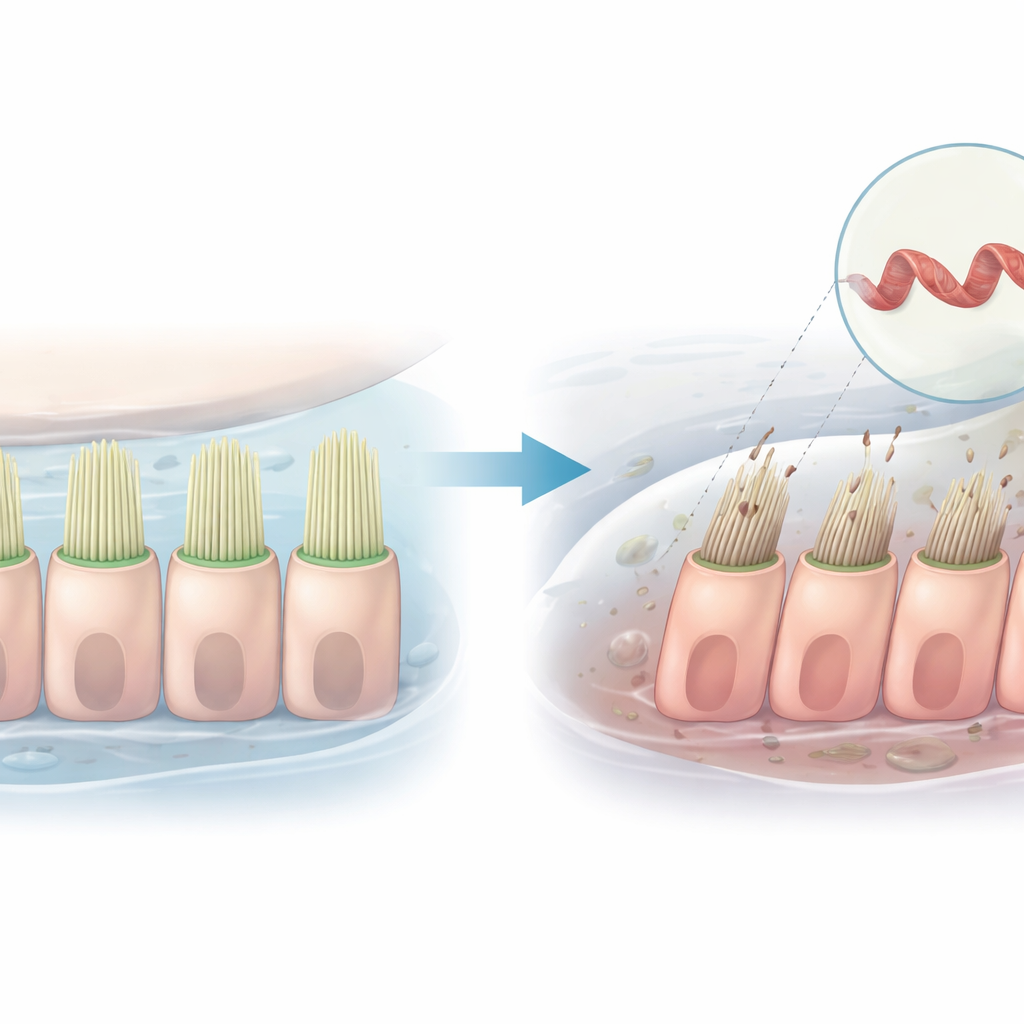
Un gène responsable d’un affaiblissement du son
La recherche se concentre sur un gène appelé PLS1, qui code pour la plastine 1, une protéine qui regroupe des filaments fins au sein des projections en forme de poils des cellules de l’oreille interne. Des familles présentant une forme progressive de surdité non syndromique ont été identifiées avec des variantes spécifiques de PLS1. Dans une famille chinoise, une modification du gène entraîne la perte d’un petit segment, connu sous le nom d’exon 8. Les membres affectés perdent l’audition des hautes fréquences dès l’enfance, et leur audition se détériore avec l’âge, mais la raison cellulaire de ce déclin n’était pas claire.
Comment un changement structural se répercute dans la cellule
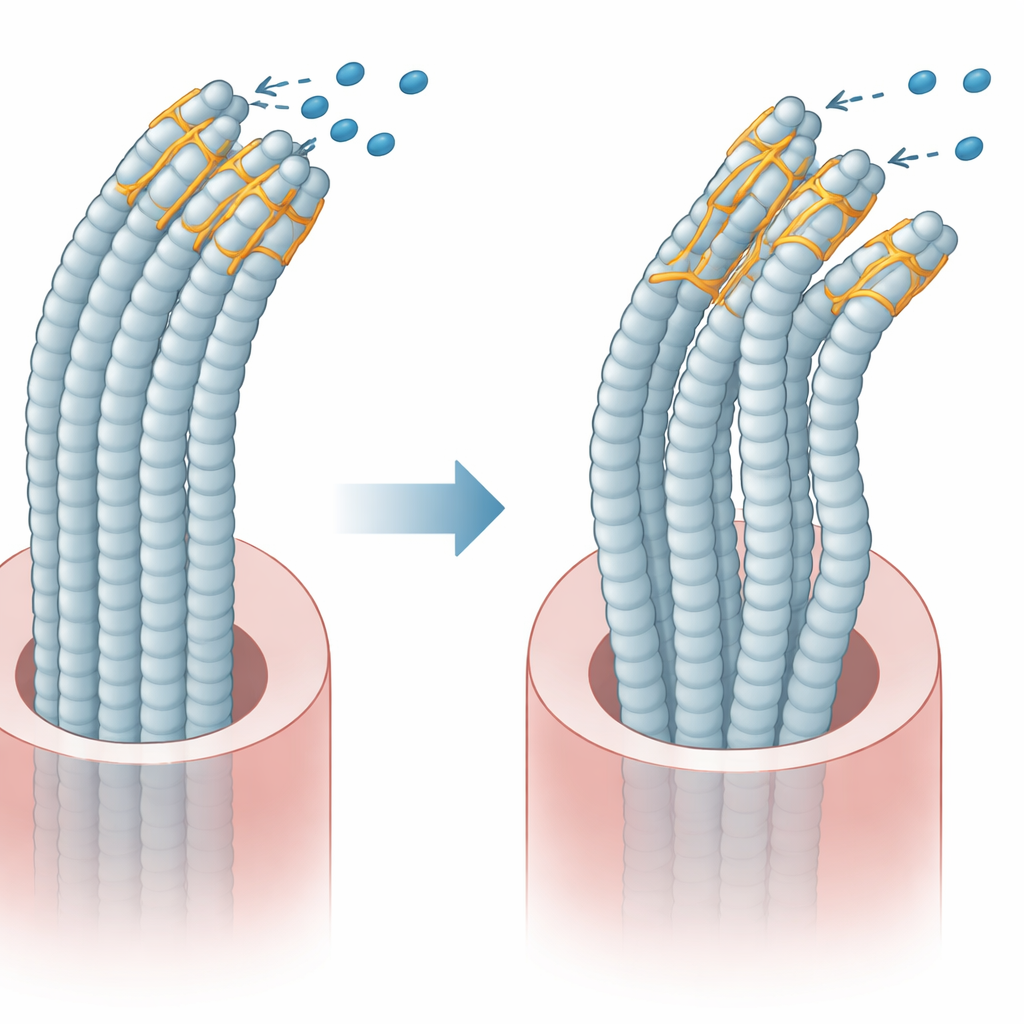
La plastine 1 possède deux domaines principaux qui se lient aux filaments internes, et dans des conditions normales un domaine régule l’autre afin que les faisceaux restent flexibles et ordonnés. L’équipe a créé des versions de la plastine 1 avec et sans l’exon 8 et les a exprimées dans des cellules en culture. Ils ont constaté que la délétion de l’exon 8 perturbe l’interaction normale entre ces deux domaines. En conséquence, la protéine mutante se lie différemment aux filaments internes et aux protéines partenaires qui aident à contrôler le mouvement et la tension. L’imagerie tridimensionnelle du cytosquelette a montré que les cellules portant la protéine mutante avaient des faisceaux moins nombreux, plus courts et plus fins, et leur forme globale devenait plus arrondie, indiquant une architecture interne perturbée.
Conséquences pour la stabilité et les interactions
Les scientifiques ont aussi découvert que la plastine 1 mutante est davantage marquée pour l’élimination par le système de déchet cellulaire, ce qui signifie qu’elle est dégradée plus rapidement et n’atteint pas des niveaux normaux. En parallèle, la forme mutante se lie plus fortement à certains partenaires clés, y compris une protéine commune de formation de filaments et une protéine motrice appelée MYO1C qui aide à ajuster la tension aux extrémités des projections en forme de poils. En pratique, la plastine 1 altérée perd une partie de sa fonction habituelle tout en perturbant le réglage fin du système mécanique qui ouvre et ferme les canaux de détection du son.
Enseignements tirés des oreilles et du comportement du poisson zèbre
Pour observer comment ces changements cellulaires se manifestent dans une oreille vivante, les chercheurs se sont tournés vers le poisson zèbre, dont les structures de l’oreille interne et les gènes sont remarquablement proches des nôtres. Ils ont utilisé l’édition génétique pour créer des poissons dépourvus totalement de la version poisson de PLS1, puis ont tenté de compenser cette perte en introduisant soit le PLS1 humain normal soit la version avec délétion de l’exon 8. Les poissons dépourvus de PLS1 présentaient des modifications légères de la taille et de la forme de leurs vésicules auditives et des otolithes (les petits « cailloux ») qui participent à la détection du mouvement ; ces défauts étaient pour la plupart corrigés par le gène humain normal. En revanche, les poissons recevant le gène humain mutant montraient toujours des anomalies structurelles et ne nageaient pas aussi vigoureusement en réponse aux sons, suggérant des réponses auditives diminuées.
Des canaux qui ne s’ouvrent plus correctement
L’équipe a ensuite vérifié si les canaux clés des cellules ciliées fonctionnaient correctement. Ils ont utilisé un colorant fluorescent qui ne pénètre dans les cellules ciliées que par des canaux ouverts et ont mesuré la quantité de colorant entrée. Les poissons exprimant le gène mutant présentaient une absorption de colorant nettement réduite, ce qui signifie que ces canaux s’ouvraient moins souvent. En contraste, les poissons simplement dépourvus de PLS1, sans la forme mutante présente, montraient en réalité une légère augmentation de l’entrée du colorant, comme si leurs canaux étaient plus ouverts que la normale. Ce contraste suggère que la protéine mutante interfère activement avec le comportement normal des canaux, plutôt que de se contenter d’éliminer une fonction utile.
Ce que cela signifie pour la surdité héréditaire
Pris ensemble, les expériences cellulaires et sur poisson zèbre indiquent un double impact de la variante d’exon 8 de PLS1. La plastine 1 mutante est moins stable et ne peut pas remplir pleinement son rôle habituel de façonnage et de soutien du squelette interne des cellules ciliées, mais elle se lie aussi anormalement à des partenaires clés et rigidifie ou désaligne les structures qui contrôlent l’ouverture des canaux. Cette combinaison est probablement à l’origine de la surdité observée dans les familles affectées. Pour de futures thérapies, le travail suggère que l’apport de PLS1 normal seul pourrait ne pas suffire ; les traitements devront peut‑être aussi supprimer ou contourner la version mutante nuisible pour restaurer une détection sonore saine.
Citation: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Mots-clés: surdité héréditaire, gène PLS1, cellules ciliées, modèle poisson zèbre, mécanotransduction