Clear Sky Science · it
Meccanismo patogenetico della variante del gene PLS1 nella perdita dell'udito e validazione funzionale in un modello di zebrafish
Perché le piccole strutture dell’orecchio contano
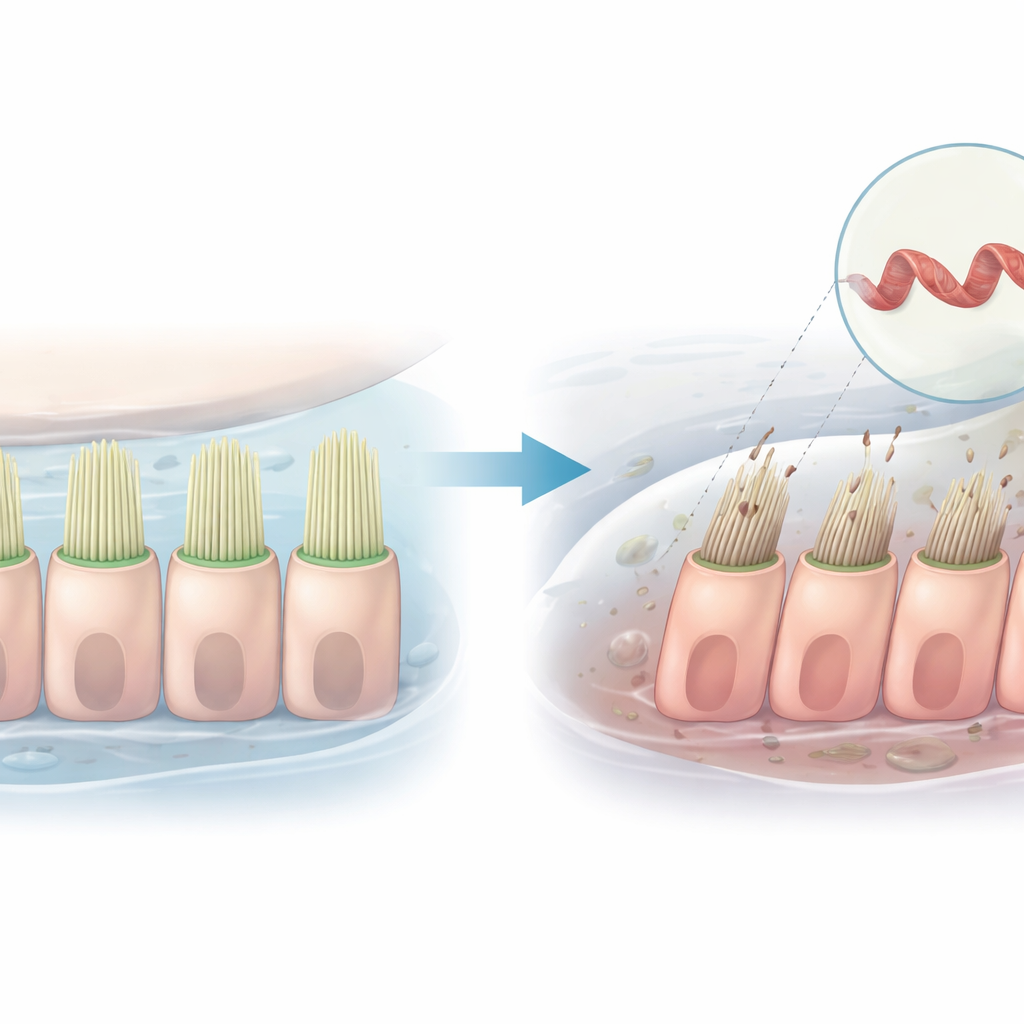
L’udito dipende da file di microscopici prolungamenti simili a peli situati in profondità nell’orecchio interno. Quando le vibrazioni sonore piegano questi peli, si aprono canali che permettono il flusso di particelle cariche nelle cellule, generando i segnali che il cervello interpreta come suono. Questo studio esamina come una singola variazione genetica in una proteina che contribuisce a modellare questi ciuffi possa perturbare quel processo e portare a ipoacusia ereditaria, usando sia cellule umane sia zebrafish come modelli.
Un gene responsabile del suono attenuato
La ricerca si concentra su un gene chiamato PLS1, che codifica per la plastina 1, una proteina che raggruppa filamenti sottili all’interno dei prolungamenti ciliari delle cellule dell’orecchio interno. In famiglie con una forma progressiva e non sindromica di perdita dell’udito sono state identificate varianti specifiche di PLS1. In una famiglia cinese, una modifica del gene provoca la perdita di un piccolo segmento, noto come esone 8. I membri affetti iniziano a perdere l’udito per le frequenze acute durante l’infanzia e la perdita peggiora con l’età, ma la ragione cellulare di questo declino non era chiara.
Come una modifica strutturale riverbera nella cellula
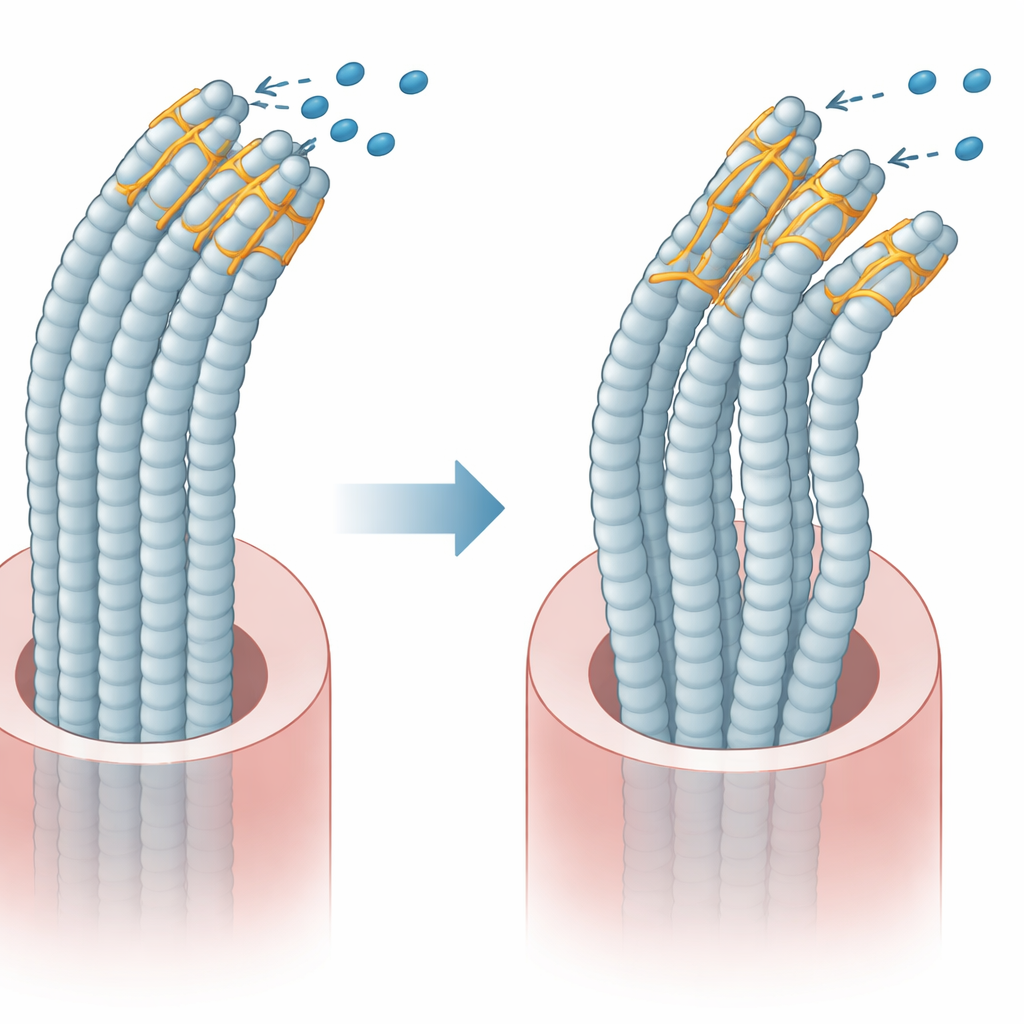
La plastina 1 possiede due regioni principali che si legano ai filamenti interni e, in condizioni normali, una regione regola l’altra in modo che i ciuffi restino flessibili e ordinati. Il gruppo ha creato versioni della plastina 1 con e senza l’esone 8 ed espresso queste proteine in cellule coltivate. Hanno osservato che la delezione dell’esone 8 interrompe la normale interazione tra le due regioni. Di conseguenza, la proteina mutata si lega in modo diverso ai filamenti interni e alle proteine partner che aiutano a controllare movimento e tensione. L’imaging tridimensionale dell’impalcatura interna ha mostrato che le cellule con la proteina mutata avevano ciuffi meno numerosi, più corti e più sottili, e la loro forma complessiva diventava più arrotondata, segnale di un’architettura interna alterata.
Conseguenze per stabilità e interazioni
Gli scienziati hanno anche rilevato che la plastina 1 mutata è maggiormente marcata per lo smaltimento dal sistema di degradazione cellulare, il che significa che viene demolita più rapidamente e non raggiunge livelli normali. Allo stesso tempo, la forma mutata si lega più saldamente ad alcuni partner chiave, inclusa una proteina comune che forma filamenti e una proteina motoria chiamata MYO1C che aiuta a regolare la tensione alle punte dei prolungamenti ciliari. Di fatto, la plastina 1 alterata perde parte della sua funzione abituale e al contempo interferisce con la messa a punto del sistema meccanico che apre e chiude i canali sensori del suono.
Lezioni dalle orecchie e dal comportamento dello zebrafish
Per capire come questi cambiamenti cellulari si manifestano in un orecchio vivente, i ricercatori hanno utilizzato lo zebrafish, le cui strutture dell’orecchio interno e i cui geni sono sorprendentemente simili ai nostri. Hanno impiegato l’editing genetico per creare pesci privi completamente della versione ittica di PLS1 e poi hanno cercato di compensare questa perdita introducendo o il PLS1 umano normale o la versione con la delezione dell’esone 8. I pesci privi di PLS1 mostravano lievi alterazioni nelle dimensioni e nella forma delle sacche dell’orecchio interno e delle piccole pietre (otoliti) che aiutano a percepire il movimento; questi difetti venivano per lo più corretti dal gene umano normale. Tuttavia, i pesci che ricevevano il gene umano mutato mantenevano anomalie strutturali e non nuotavano con la stessa vivacità in risposta ai suoni, suggerendo risposte ridotte alla stimolazione acustica.
Canali che non si aprono correttamente
Il gruppo ha quindi verificato se i canali chiave sulle cellule ciliari funzionassero correttamente. Hanno usato un colorante fluorescente che può entrare nelle cellule ciliate solo attraverso i canali aperti e hanno misurato la quantità di colorante assorbita. I pesci esprimenti il gene mutato avevano un’assunzione di colorante nettamente inferiore, il che indica che questi canali si aprivano meno. Al contrario, i pesci semplicemente privi di PLS1, senza la forma mutata presente, mostravano in realtà un leggero aumento dell’ingresso del colorante, come se i loro canali fossero più aperti del normale. Questo contrasto suggerisce che la proteina mutata interferisca attivamente con il comportamento normale dei canali, più che limitarsi a rimuovere una funzione utile.
Cosa significa per la perdita uditiva ereditaria
Complessivamente, gli esperimenti su cellule e zebrafish indicano un doppio impatto della variante di PLS1 che coinvolge l’esone 8. La plastina 1 mutata è meno stabile e non può svolgere pienamente il suo ruolo nel modellare e sostenere l’impalcatura interna delle cellule ciliari, ma si lega anche in modo anomalo a partner chiave e irrigidisce o disallinea le strutture che regolano l’apertura dei canali. Questa combinazione probabilmente spiega la perdita dell’udito osservata nelle famiglie colpite. Per terapie future, il lavoro suggerisce che limitarsi ad aggiungere PLS1 normale potrebbe non bastare; i trattamenti dovranno anche silenziare o bypassare la versione mutata dannosa per ripristinare una rilevazione del suono sana.
Citazione: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Parole chiave: ipoacusia ereditaria, gene PLS1, cellule ciliate, modello zebrafish, meccanotrasduzione