Clear Sky Science · pt
Mecanismo patogênico da variante do gene PLS1 em perda auditiva e validação funcional em um modelo de zebrafish
Por que estruturas minúsculas do ouvido importam
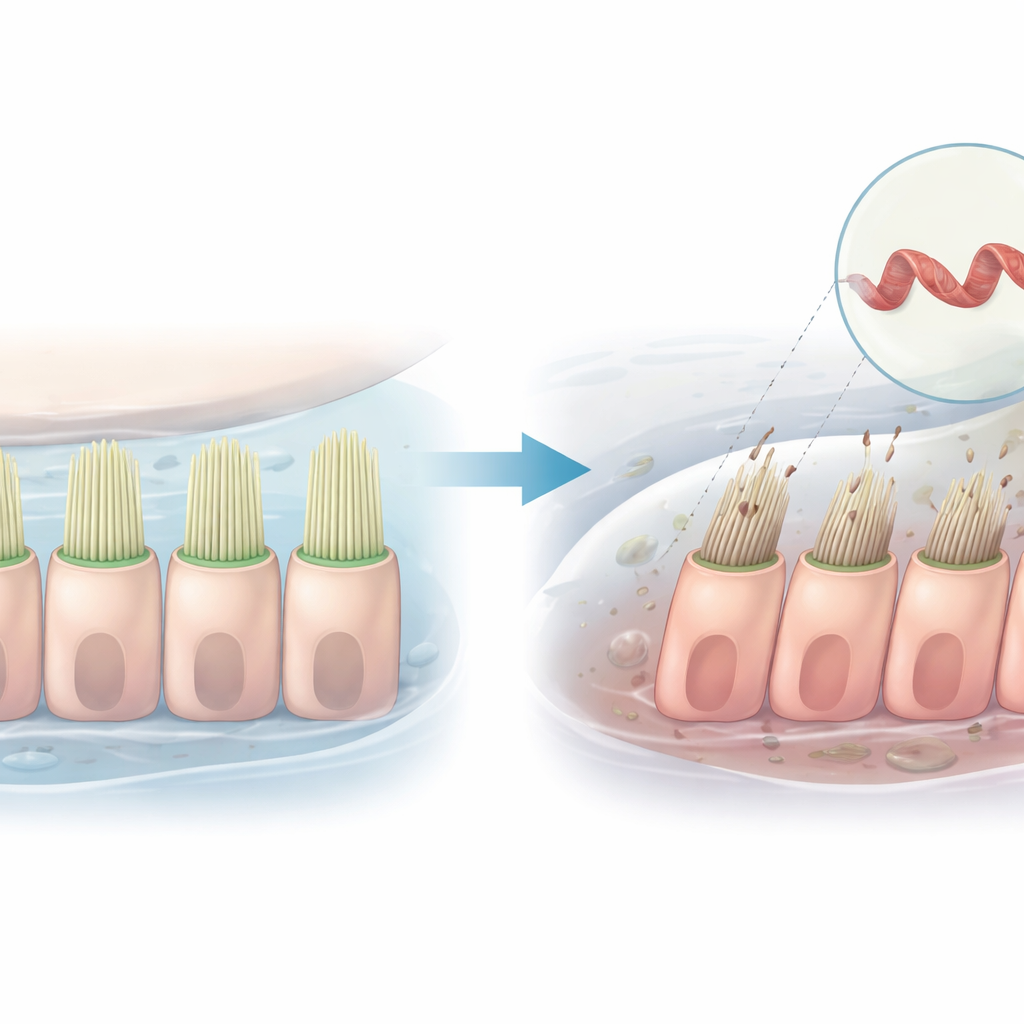
A audição depende de fileiras de projeções microscópicas semelhantes a cílios localizadas profundamente no ouvido interno. Quando as vibrações sonoras dobram esses cílios, abrem-se canais que permitem a entrada de partículas carregadas nas células, criando os sinais que nosso cérebro interpreta como som. Este estudo investiga como uma única alteração genética em uma proteína que ajuda a moldar esses feixes de cílios pode atrapalhar esse processo e levar à perda auditiva hereditária, usando tanto células humanas quanto zebrafish como modelos.
Um gene por trás do som silenciado
A pesquisa se concentra em um gene chamado PLS1, que codifica a plastina 1, uma proteína que organiza filamentos finos dentro das projeções tipo cílio das células do ouvido interno. Famílias com uma forma progressiva e não sindrômica de perda auditiva foram identificadas com variantes específicas em PLS1. Em uma família chinesa, uma alteração no gene provoca a perda de um pequeno segmento, conhecido como éxon 8. Membros afetados começam a perder audição em altas frequências durante a infância, e a audição piora com a idade, mas a razão celular para esse declínio não estava clara.
Como uma mudança estrutural se espalha pela célula
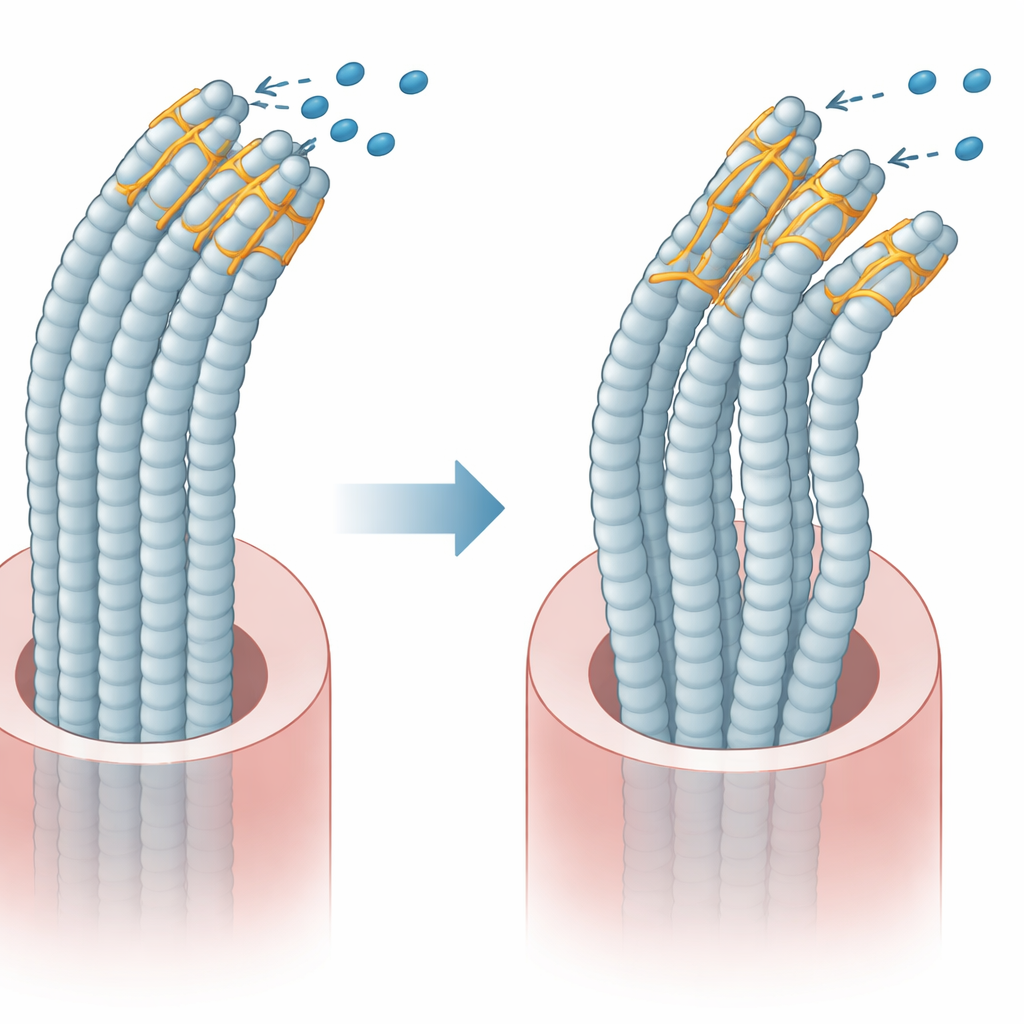
A plastina 1 tem duas regiões principais que se ligam a filamentos internos e, em condições normais, uma região regula a outra para que os feixes permaneçam flexíveis e ordenados. A equipe criou versões da plastina 1 com e sem o éxon 8 e as expressou em células cultivadas. Eles descobriram que a deleção do éxon 8 interrompe a interação normal entre essas duas regiões. Como resultado, a proteína mutante se liga de forma diferente aos filamentos internos e a proteínas parceiras que controlam movimento e tensão. Imagens tridimensionais do arcabouço interno mostraram que células com a proteína mutante tinham feixes em menor número, mais curtos e mais finos, e sua forma geral tornava-se mais arredondada, indicando uma arquitetura interna perturbada.
Consequências para estabilidade e parcerias
Os cientistas também descobriram que a plastina 1 mutante recebe mais marcas para descarte pelo sistema de degradação celular, o que significa que é degradada mais rapidamente e não se acumula em níveis normais. Ao mesmo tempo, a forma mutante se liga mais fortemente a certos parceiros chave, incluindo uma proteína comum de formação de filamentos e uma proteína motora chamada MYO1C, que ajuda a ajustar a tensão nas pontas das projeções tipo cílio. Na prática, a plastina 1 alterada tanto perde parte de sua função usual quanto interfere no ajuste fino do sistema mecânico que abre e fecha os canais sensores de som.
Lições dos ouvidos e do comportamento do zebrafish
Para entender como essas alterações celulares se manifestam em um ouvido vivo, os pesquisadores recorreram ao zebrafish, cujas estruturas e genes do ouvido interno são notavelmente semelhantes aos nossos. Eles usaram edição gênica para criar peixes que carecem completamente da versão animal de PLS1 e então tentaram resgatar essa perda adicionando o PLS1 humano normal ou a versão com deleção do éxon 8. Peixes sem PLS1 mostraram mudanças leves no tamanho e na forma dos sacos do ouvido interno e nas pequenas pedras (otólitos) que ajudam a detectar movimento, e esses defeitos foram em grande parte corrigidos pelo gene humano normal. Contudo, peixes que receberam o gene humano mutante continuaram a apresentar anomalias estruturais e não nadaram com a mesma vigorosidade em resposta ao som, sugerindo respostas reduzidas semelhantes à perda auditiva.
Canais que deixam de abrir corretamente
A equipe então investigou se os canais-chave nas células ciliadas estavam funcionando corretamente. Eles usaram um corante fluorescente que só entra nas células ciliadas por meio de canais abertos e mediram quanto corante entrou. Peixes expressando o gene mutante apresentaram captação de corante visivelmente menor, o que indica que esses canais tinham menos probabilidade de se abrir. Em contraste, peixes que simplesmente não tinham PLS1, sem a presença da forma mutante, mostraram um leve aumento na entrada de corante, como se seus canais estivessem mais abertos do que o habitual. Esse contraste sugere que a proteína mutante interfere ativamente no comportamento normal dos canais, em vez de apenas remover uma função benéfica.
O que isso significa para a perda auditiva hereditária
Em conjunto, os experimentos em células e em zebrafish apontam para um impacto duplo da variante de éxon 8 em PLS1. A plastina 1 mutante é menos estável e não consegue desempenhar plenamente seu papel habitual de moldar e suportar o arcabouço interno das células ciliadas, mas também se liga anormalmente a parceiros-chave e rigidifica ou desalinha as estruturas que controlam a abertura dos canais. Essa combinação provavelmente explica a perda auditiva observada em famílias afetadas. Para futuras terapias, o trabalho sugere que simplesmente aumentar a quantidade de PLS1 normal pode não ser suficiente; os tratamentos também podem precisar silenciar ou contornar a versão mutante nociva para restaurar a detecção sonora saudável.
Citação: Xu, T., Yang, T., Wang, H. et al. Pathogenic mechanism of the PLS1 gene variant in hearing loss and functional validation in a zebrafish model. Sci Rep 16, 14708 (2026). https://doi.org/10.1038/s41598-026-47079-4
Palavras-chave: perda auditiva hereditária, gene PLS1, células ciliadas, modelo zebrafish, mecanotransdução