Clear Sky Science · zh
脂质纳米颗粒递送环形RNA疫苗诱导强效免疫反应
为何一种新型疫苗很重要
基于遗传物质的疫苗已经改变了我们对抗像新冠这样的感染的方式,但现有的RNA疫苗往往脆弱且持续时间有限。本研究探讨了一种下一代方法:使用更稳定的RNA形式并封装在微小的脂质囊泡中,以激发针对癌症和传染病的免疫反应。对读者而言,这提供了未来疫苗如何变得更强效、持续时间更长、并且更易于储存和在全球范围内使用的一个前瞻性视角。 
一种环状的说明书
大多数人都听说过信使RNA(mRNA),这是当前RNA疫苗中使用的单链遗传信息。环形RNA(circRNA)则不同:它没有两端,而是形成一个闭合的环。这个简单的变化使得体内的酶更难以降解它,因此存活时间更长,能够在更长时间内指导细胞产生蛋白质。作者解释说,circRNA可以被设计为携带肿瘤标志物或病毒片段的蓝图,而且由于它不会进入我们染色体的DNA,避免了永久改变基因的风险。再加上可大规模生产的能力,这些特性使得circRNA成为一种具有持久性和灵活性的有吸引力的疫苗平台候选者。
微小脂质囊泡作为递送载体
将脆弱的RNA安全地送入细胞是一大难题。这就是脂质纳米颗粒发挥作用的地方——它们是由类脂分子组成的微小球体,能将circRNA包裹起来,保护其在体内迁移,并帮助其在注射后进入细胞。研究人员关注的是将circRNA通过这些颗粒递送给小鼠的研究,递送途径包括肌内、皮下、静脉内和鼻内注射。通过回顾并汇总多项独立动物试验的数据,他们评估了这些circRNA–纳米颗粒疫苗在缩小肿瘤、控制感染以及避免诸如体重下降或严重毒性等副作用方面的效果。
更强的免疫作战细胞,更小的肿瘤
综合的动物数据描绘出一个引人注目的图景。在十项肿瘤研究中,接受circRNA疫苗的小鼠无论注射到肌肉、皮下还是血液中,其肿瘤都明显比对照动物小。同时,体重——作为整体健康状况的粗略指标——保持稳定,表明治疗并未引起广泛毒性。详细的免疫学测量显示关键的白细胞活性增强:直接杀伤异常细胞的T细胞增多,巨噬细胞增加,树突状细胞——展示入侵者片段给免疫系统的哨兵——显著提升。这些变化表明疫苗不仅机械性地攻击肿瘤,而是重新教育免疫系统更有效地识别并摧毁癌细胞。 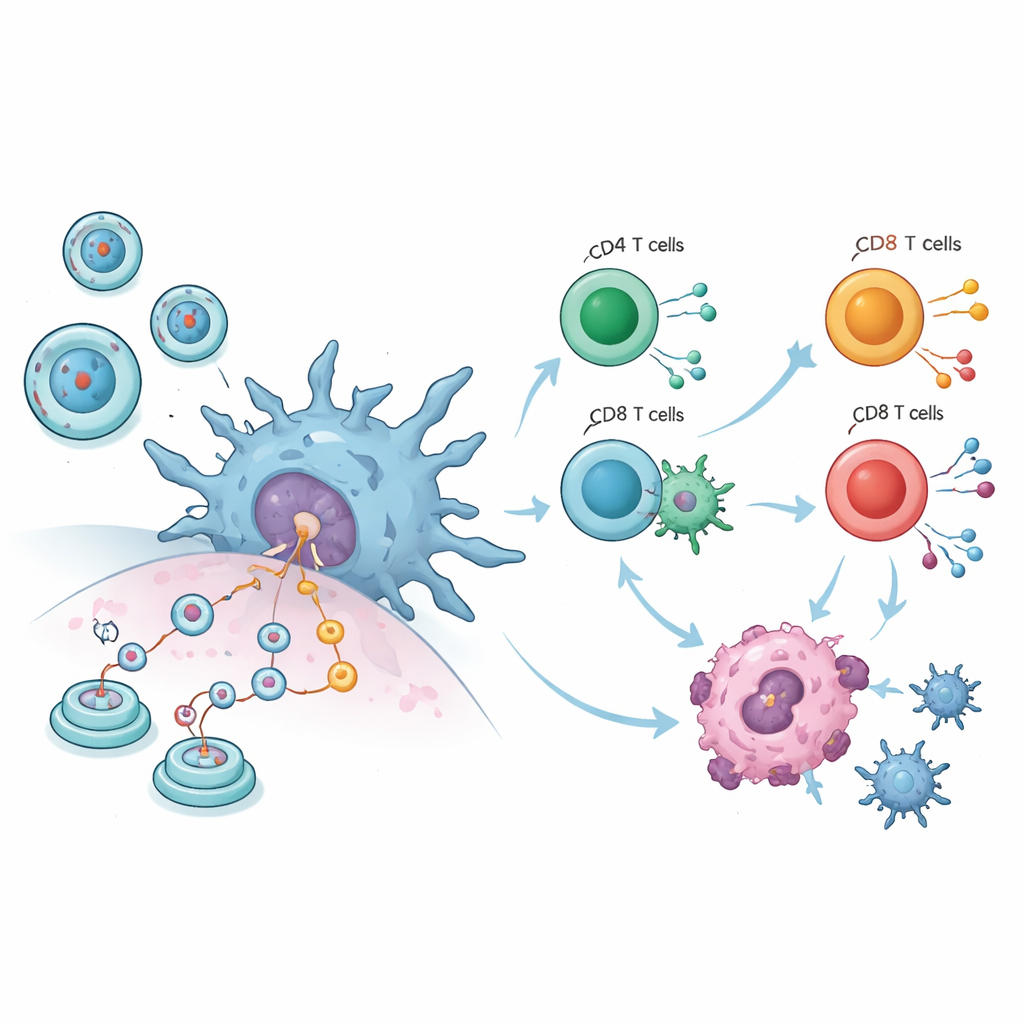
用相同工具对抗病毒
相同的circRNA技术在传染病模型中也表现出强大效果,包括流感、寨卡、SARS‑CoV‑2及其他病毒。在接种疫苗的小鼠中,血液中的抗体水平显著上升,肺部病毒负荷下降,干扰素‑γ和白细胞介素‑4等信号分子增加,表明免疫系统的速效与持久两端均被激活。鼻内递送针对气道黏膜,常常产生特别强的局部保护,而其他途径则更有利于全身性的广泛反应。总体而言,分析显示一个经调谐以不同目标的单一circRNA平台,既可用于防护多种病原体,也可用于对抗癌症。
在人类细胞中检验作用机制
为了超越动物数据,作者在实验室中使用来自人类血液的免疫细胞进行了试验。他们制备了编码测试蛋白的纯化circRNA,并去除可能触发非特异性报警信号的双链RNA杂质。当树突状细胞暴露于脂质包裹的circRNA时,它们开始产生新蛋白,开启成熟的关键表面标志,并释放炎症介质如IL‑6、IL‑1β和TNF‑α。当这些被激活的树突状细胞与人T细胞混合时,辅助性和杀伤性T细胞均被激活并分泌干扰素‑γ,且在计数单个应答细胞的检测中出现了更多抗原特异性的T细胞。这些发现证实circRNA能够精确指导人类免疫细胞,而不仅仅是小鼠的免疫细胞。
希望、警示与下一步
对非专业读者来说,结论是:环形RNA疫苗由脂质纳米颗粒携带,看起来像是现有RNA疫苗更为坚固、作用更持久的近亲。在小鼠中它们能缩小肿瘤、抑制病毒感染,且未见明显危害;在人类细胞中,它们能唤醒实现靶向防御所需的免疫成分。然而,所有这些证据仍停留在临床前阶段,不同的动物品系、疾病类型和注射途径会导致结果差异。要了解这种方法在人类中的有效性并优化剂量与递送方式,还需要大规模、精心设计的人体试验。如果这些障碍被克服,circRNA疫苗可能成为一种多用途的新工具,用于治疗癌症并预防未来的传染病暴发。
引用: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
关键词: 环形RNA疫苗, 脂质纳米颗粒, 癌症免疫治疗, 感染性疾病疫苗, T细胞激活