Clear Sky Science · he
עירוי נגיפי של חיסון RNA מעגלי במעברי ננו‑חלקיקים ליפידיים משרה תגובות חיסוניות חזקות
מדוע סוג חדש של חיסון חשוב
חיסונים המבוססים על חומר גנטי שינו את הדרך שבה אנחנו מתמודדים עם זיהומים כמו COVID‑19, אך הזריקות מבוססות ה‑RNA של היום עלולות להיות שבירות וקצרות מועד. המחקר הזה חוקר גישה מתקדמת המשתמשת בצורה עמידה יותר של RNA, המוכנסת בתוך בועיות שומן זעירות, כדי לעורר את המערכת החיסונית כנגד סרטן ומחלות זיהומיות. לקורא זה מציע הצצה לאופן שבו חיסונים עתידיים עשויים להיות חזקים יותר, פעילים לאורך זמן רב יותר וקליקים יותר לאחסון ושימוש ברחבי העולם. 
מדריך הוראות בצורת לולאה
רוב האנשים שמעו על mRNA, המסר הגנטי חד‑הגדילי המשמש בחיסוני RNA הנוכחיים. RNA מעגלי, או circRNA, שונה: במקום שני קצוות הוא יוצר לולאה סגורה. שינוי פשוט זה מקשה על האנזימים בגוף ‘‘לנגוס’’ אותו, ולכן הוא שורד זמן רב יותר ויכול להנחות תאים לייצר חלבונים לפרק זמן מוארך. המחברים מסבירים שניתן למהנדס את ה‑circRNA כדי לשאת תכניות לסמנים של גידולים או לחלקי וירוס, ומכיוון שהוא אף פעם אינו נכנס ל‑DNA שבכרומוזומים שלנו, הוא נמנע מהסיכון של שינוי גנטי קבוע. יחד עם היכולת לייצור בכמויות גדולות, התכונות הללו הופכות את ה‑circRNA למועמד מעניין לפלטפורמת חיסון עמידה וגמישה.
בועיות שומן זעירות כמשאיות משלוח
העברת RNA שביר לתאים בבטחה היא מכשול משמעותי. כאן נכנסים לתמונה ננו‑חלקיקים ליפידיים—כדורים זעירים עשויים מולקולות דמויי שומן. הם עוטפים את ה‑circRNA, מקנים לו הגנה בזמן שהוא נוסע בגוף ועוזרים לו להיכנס לתאים לאחר ההזרקה. החוקרים התמקדו בעבודות שבהן הוגש circRNA לעכברים באמצעות חלקיקים אלה, בדרכי מתן כמו תוך־שרירית, תת־עורית, תוך־ורידית ותוך‑אף. באמצעות סקירה ושילוב של נתונים ממספר ניסויים בעלי חיים בלתי תלויים הם שאלו עד כמה חיסוני circRNA–ננו‑חלקיקים מקטינים גידולים, שולטים בזיהומים ומונעים תופעות לוואי כמו ירידת משקל או רעילות קשה.
לוחמי חיסון חזקים יותר, גידולים קטנים יותר
הנתונים המשולבים מחיות מציירים תמונה חדה. בעשרת מחקרי הגידול, עכברים שקיבלו חיסוני circRNA פיתחו גידולים קטנים בהרבה מאשר בעלי החיים בקבוצת הביקורת, ללא קשר לדרך ההזרקה—לשריר, מתחת לעור או למחזור הדם. באותו זמן, משקל הגוף—סמן גס של בריאות כללית—נשאר יציב, מה שמרמז שהטיפול לא היה רעיל באופן נרחב. מדידות אימוניות מפורטות הראו שתאי דם לבנים מרכזיים הפכו לפעילים יותר: תאי T ההורגים הישירים התרחבו, מקרופאגים עלו במספרם ותאי דנדריט—השומרים שמציגים חלקיקי פולש למערכת החיסון—הוגברו במידה ניכרת. שינויים אלה מצביעים על כך שהחיסונים אינם תוקפים את הגידולים באופן מכני בלבד; הם מחדש־חונכים את המערכת החיסונית לזהות ולהשמיד תאי סרטן ביעילות רבה יותר. 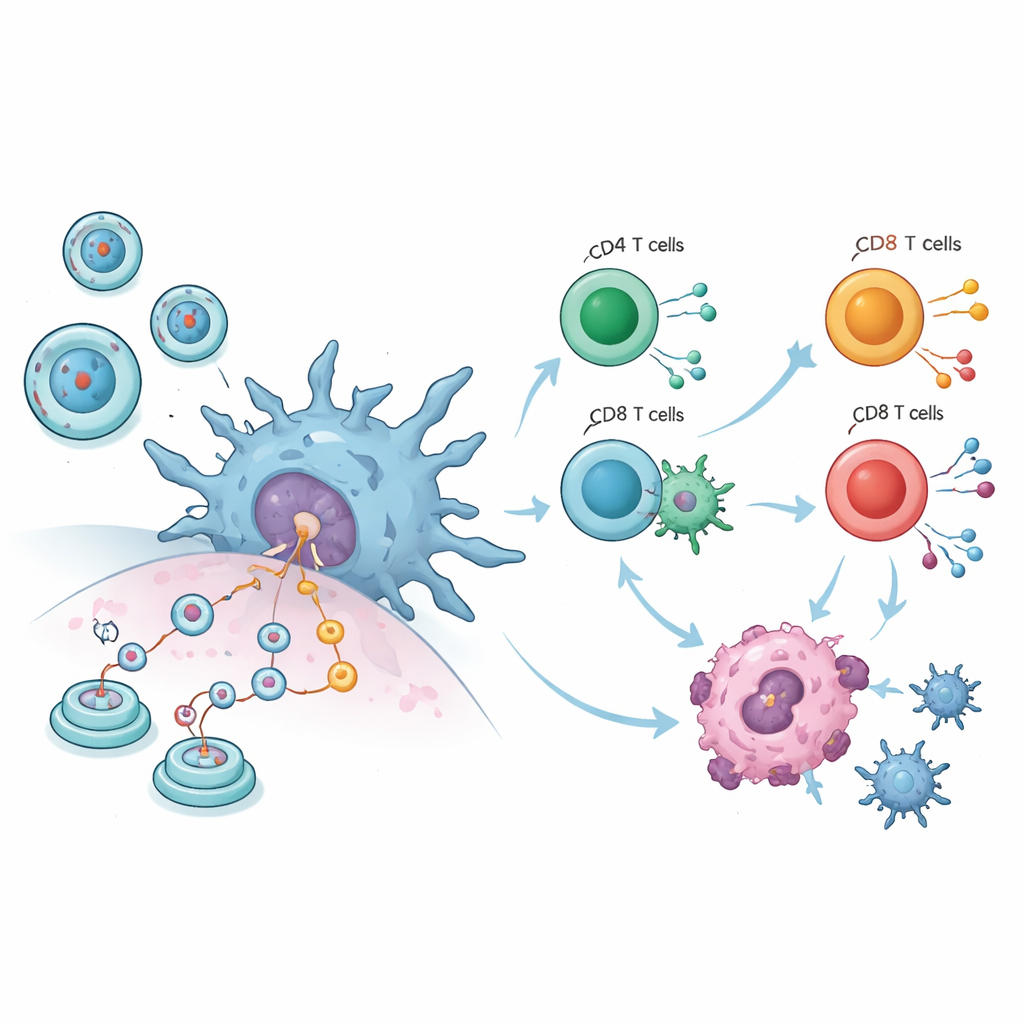
הילחם בווירוסים באמצעות אותו כלי
אותה טכנולוגיית circRNA הוכיחה עצמה גם במודלים של מחלות זיהומיות, כולל שפעת, זיקה, SARS‑CoV‑2 ווירוסים נוספים. בעכברים מחוסנים רמות הנוגדנים בדם עלו באופן חד, עומס הווירוס בריאות ירד, ומולקולות איתות כמו אינטרפרון‑גמא ואינטרלוקין‑4 עלו, מה שמראה ששתי זרועות המערכת החיסונית—המיידית והמתמשכת—הופעלו. מתן תוך‑אף, הפונה לרירית נתיבי הנשימה, לעיתים קרובות ייצר הגנה מקומית חזקה במיוחד, בעוד שדרכים אחרות הניבו תגובות רחבות יותר בכל הגוף. בסך הכל, הניתוח מציע כי פלטפורמת circRNA אחת, המותאמת ליעדים שונים, יכולה להגן מפני מגוון פתוגנים וכן מפני סוגי סרטן שונים.
בדיקת המנגנון בתאים אנושיים
כדי להתקדם מעבר לנתונים מחיות, המחברים ערכו ניסויים במעבדה בתאים חיסוניים שמקורם בדם אנושי. הם ייצרו circRNA מטוהר שקידד חלבון מבחן והסירו RNA דו‑גדילי מזהם שעלול לעורר אותות אזעקה לא ספציפיים. כאשר תאי דנדריט נחשפו ל‑circRNA עטוף בליפידים, הם החלו לייצר את החלבון החדש, הדליקו סמני בגרות חשובות על המשטח ושחררו שליחים דלקתיים כגון IL‑6, IL‑1β ו‑TNF‑α. כאשר תאי דנדריט אלה שהופעלו נמעכו עם תאי T אנושיים, גם תאי ה‑T המסייעים וגם ההורגים הופעלו ושלחו אינטרפרון‑גמא, ועוד תאי T הספציפיים לאנטיגן הופיעו בבדיקה שמונה תאים מגיבים בודדים. ממצאים אלו מאשרים כי circRNA יכול לכוון במדויק תאים חיסוניים אנושיים, ולא רק של עכברים.
הבטחה, הסתייגויות ומה הלאה
ללא‑מומחים, הסיכום הוא שחיסוני RNA מעגלי, המועמסים בננו‑חלקיקים ליפידיים, נראים כקרוב חזק ועמיד יותר של זריקות ה‑RNA הנוכחיות. בעכברים הם מקטינים גידולים, מצמצמים זיהומים ויעשו זאת מבלי לגרום נזק גלוי, ובעיניים של תאים אנושיים הם מעוררים את השחקנים החיסוניים הדרושים להגנה ממוקדת. עם זאת, כל הראיות האלה עדיין פרה‑קליניות, ומינים חיה שונים, סוגי מחלה ודרכי הזרקה הניבו תוצאות משתנות. נדרשים ניסויים קליניים גדולים ומתוכננים בקפידה כדי ללמוד עד כמה הגישה עובדת בבני אדם ולכייל מינונים ואסטרטגיות מתן. אם המכשולים הללו ייפתרו, חיסוני circRNA יכולים להפוך לכלי רב‑שימושי לטיפול בסרטן ולמניעת התפרצויות עתידיות של מחלות זיהומיות.
ציטוט: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
מילות מפתח: חיסוני RNA מעגלי, ננו‑חלקיקים ליפידיים, אימונותרפיה של סרטן, חיסונים למחלות זיהומיות, הפעלה של תאי T