Clear Sky Science · ja
円形RNAワクチンのリポイドナノ粒子送達が強力な免疫反応を誘導する
なぜ新しい種類のワクチンが重要か
遺伝情報に基づくワクチンは、COVID-19のような感染症への対抗法を一変させましたが、現行のRNAワクチンは壊れやすく作用時間が短いことがあります。本研究は、より安定した形のRNAを微小な脂質の泡に封入して、がんや感染症に対する免疫を刺激する次世代アプローチを探ります。読者にとっては、将来のワクチンがより強力で長持ちし、世界中で保存・使用が容易になる可能性の一端を示す内容です。 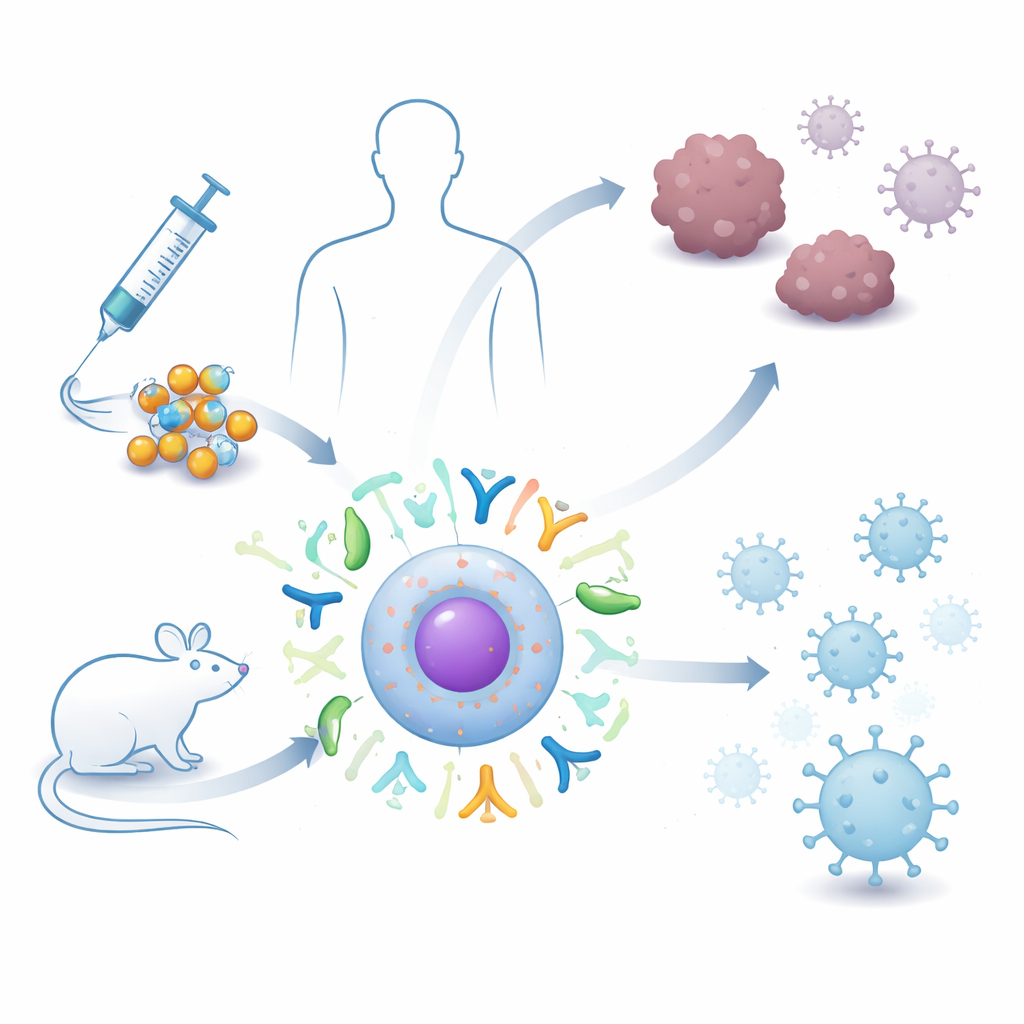
ループ状の取扱説明書
多くの人がmRNA、すなわち現在のRNAワクチンで使われる一本鎖の遺伝メッセージを知っています。円形RNA(circRNA)は異なります:両端がなく環状に閉じています。この単純な変化により体内の酵素に分解されにくくなり、長く生存して細胞により長期間タンパク質を作らせることができます。著者らは、circRNAを腫瘍マーカーやウイルスの断片の設計図として工学的に組み込めること、そして染色体のDNAに組み込まないため遺伝子を恒久的に変えるリスクを避けられることを説明しています。大量生産が可能である点と合わせて、これらの特性はcircRNAを耐久性と柔軟性を備えたワクチンプラットフォームの有望な候補にしています。
輸送トラックとしての微小な脂質の泡
壊れやすいRNAを安全に細胞内に届けることは大きな課題です。ここでリポイドナノ粒子――脂肪様分子でできた微小な球――が役立ちます。これらはcircRNAを包み、体内を移動する間に保護し、注射後に細胞へと入り込むのを助けます。研究者たちは、これらの粒子を用いてマウスにcircRNAを送達した研究に注目し、筋肉内、皮下、静脈内、鼻腔内などの投与経路を含む研究を検討しました。複数の独立した動物実験のデータをレビューして統合することで、circRNA–ナノ粒子ワクチンが腫瘍をどれほど縮小するか、感染を制御するか、体重減少や重篤な毒性といった副作用を避けられるかを問い直しました。
より強力な免疫の兵士、より小さな腫瘍
統合された動物データは印象的な図を描きます。10件の腫瘍研究全体で、circRNAワクチンを受けたマウスは対照群よりもはるかに小さな腫瘍を示し、投与が筋肉内であれ皮下であれ血流内であれ結果は同様でした。同時に、体重――全体的な健康の粗い指標――は安定しており、処置が広範な毒性を示さないことを示唆しています。詳細な免疫測定では主要な白血球がより活性化していることが分かりました:異常細胞を直接殺すT細胞が増殖し、マクロファージが増え、樹状細胞――侵入者の断片を免疫系に提示する番人――も著しく増強されました。これらの変化は、ワクチンが単に機械的に腫瘍を攻撃するだけでなく、免疫系を再教育してがん細胞をより効率的に認識し破壊することを示しています。 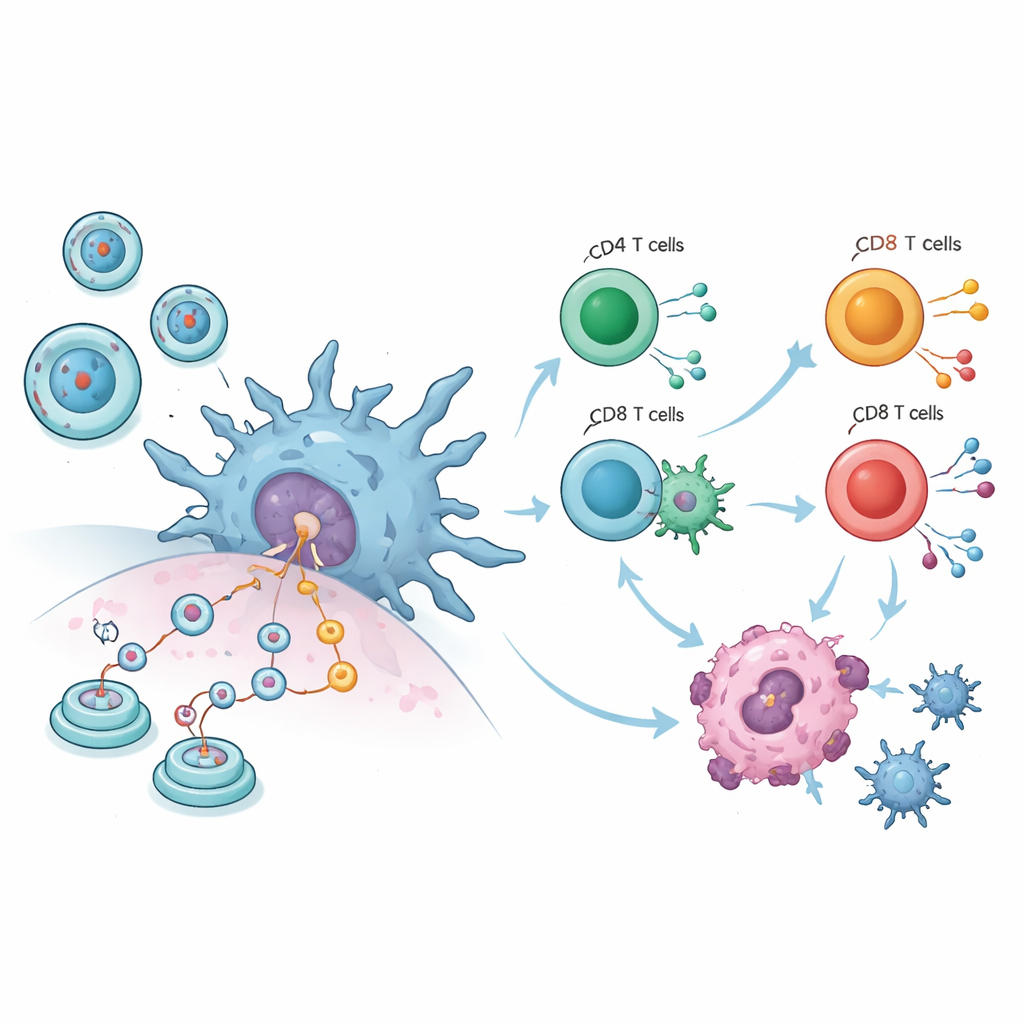
同じ道具でウイルスと戦う
同じcircRNA技術は、インフルエンザ、ジカ、SARS-CoV-2などのウイルスを含む感染症モデルでも強力であることが示されました。ワクチン接種を受けたマウスでは血中の抗体価が急上昇し、肺内のウイルス量が減少し、インターフェロンγやインターロイキン‑4などのシグナル分子が増加して、免疫系の速攻の反応とより長期の反応の両方が動員されていることが示されました。気道の粘膜を標的とする鼻腔内投与はしばしば特に強い局所防御を生み、他の経路は体全体にわたるより広い反応を促す傾向がありました。全体として、この解析は、標的を変えることで幅広い病原体やがんに対して適応可能な単一のcircRNAプラットフォームの可能性を示唆しています。
ヒト細胞でメカニズムを検証する
動物データを超えるために、著者らはヒトの血液由来免疫細胞を用いた実験室実験を行いました。試験用タンパク質をコードする精製されたcircRNAを作製し、非特異的な警報反応を引き起こす可能性のある二本鎖RNAの混入を除去しました。樹状細胞が脂質で包まれたcircRNAにさらされると、新しいタンパク質の産生を開始し、成熟の重要な表面マーカーを発現し、IL-6、IL-1β、TNF-αといった炎症性メッセンジャーを放出しました。これらの活性化した樹状細胞をヒトT細胞と混ぜると、ヘルパーとキラーの両方のT細胞がスイッチオンしてインターフェロンγを分泌し、単一応答細胞を数えるアッセイで抗原特異的なT細胞が増加しました。これらの所見は、circRNAがマウスだけでなくヒトの免疫細胞にも正確に指示を出せることを裏付けます。
期待、注意点、そして次の一歩
非専門家にとっての要点は、リポイドナノ粒子で運ばれる円形RNAワクチンは、現行のRNAワクチンのより頑丈で作用持続の長い系統に見えるということです。マウスでは腫瘍を縮小し、ウイルス感染を抑え、明らかな有害事象なしにそれを達成し、ヒト細胞では標的化された防御に必要な免疫の主要プレイヤーを目覚めさせました。しかし、これらの証拠はまだ前臨床段階にあり、動物の系統、疾病の種類、投与経路により結果は変動しました。人に対してこのアプローチがどの程度有効か、投与量や送達方法を最適化するには、大規模で慎重に設計された臨床試験が必要です。これらの課題がクリアされれば、circRNAワクチンはがん治療や将来の感染症流行の予防のための多用途な新しい道具となり得ます。
引用: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
キーワード: 環状RNAワクチン, リポイドナノ粒子, がん免疫療法, 感染症ワクチン, T細胞活性化