Clear Sky Science · tr
Döngüsel RNA aşısının lipid nanopartikül ile verilmesi güçlü bağışıklık yanıtları uyandırıyor
Neden Yeni Bir Aşı Türü Önemli
Genetik materyale dayalı aşılar, COVID‑19 gibi enfeksiyonlarla mücadelemizi kökten değiştirdi; ancak günümüz RNA aşıları kırılgan ve kısa ömürlü olabiliyor. Bu çalışma, daha sağlam bir RNA biçimi kullanarak ve bunu küçük yağ kabarcıklarına paketleyerek hem kanser hem de bulaşıcı hastalıklara karşı bağışıklık sistemini harekete geçirmeyi amaçlayan yeni nesil bir yaklaşımı inceliyor. Okuyucular için bu, gelecekte aşıların nasıl daha güçlü, daha uzun ömürlü ve dünyada saklanması ile kullanımı daha kolay hale gelebileceğine dair bir öngörü sunuyor. 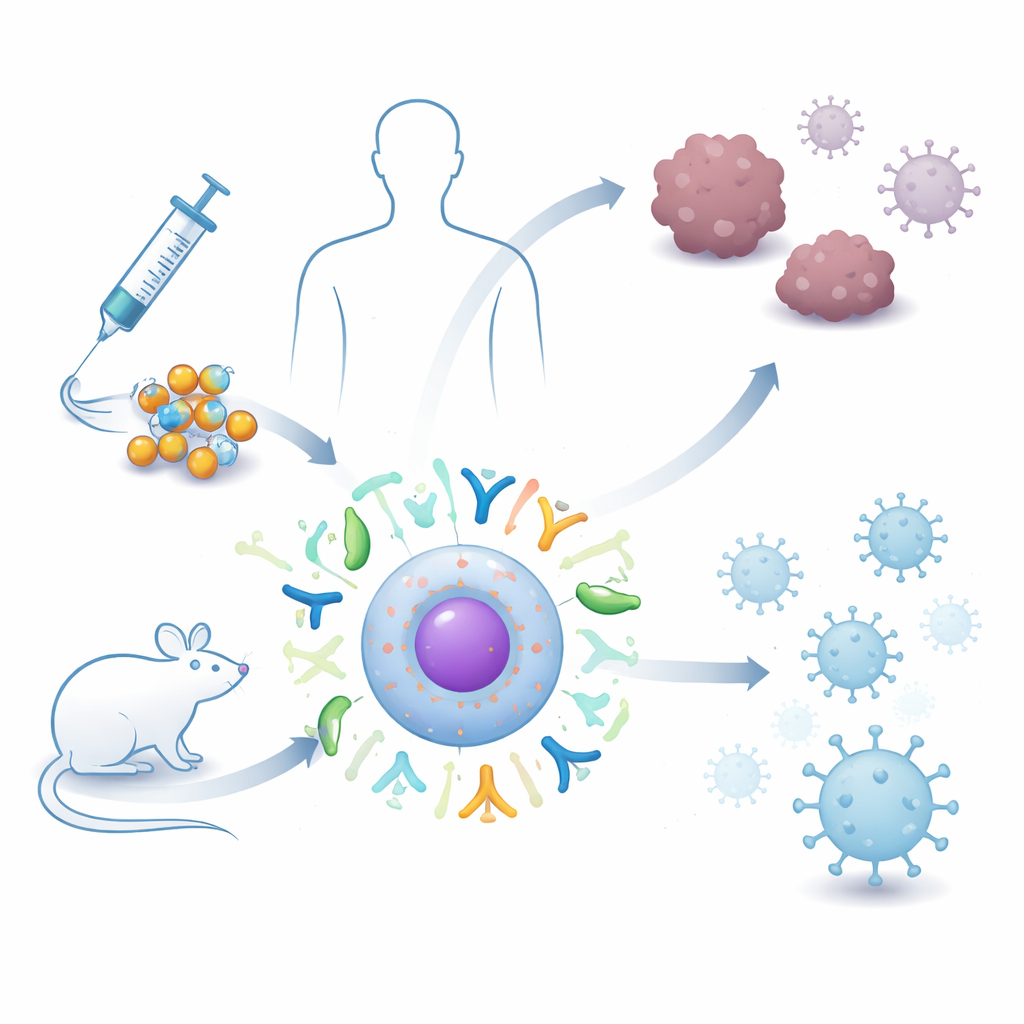
Halka Şeklinde Bir Talimat Kılavuzu
Çoğu kişi, mevcut RNA aşılarında kullanılan tek iplikçikli genetik mesaj olan mRNA’yı duymuştur. Dairesel RNA ya da circRNA farklıdır: iki ucu olmak yerine kapalı bir halka oluşturur. Bu basit değişiklik, vücudun enzimlerinin onu parçalamasını çok daha zorlaştırır; böylece daha uzun yaşar ve hücrelere daha uzun süre protein üretmeleri talimatını verebilir. Yazarlar, circRNA’nın tümör belirteçleri veya viral parçalar için şablonlar taşıyacak şekilde tasarlanabileceğini ve kromozomlarımızdaki DNA’ya asla girmediği için genlerimizi kalıcı olarak değiştirme riski taşımadığını açıklıyor. Büyük miktarlarda üretilebilme yeteneğiyle birleştiğinde, bu özellikler circRNA’yı dayanıklı, esnek bir aşı platformu için cazip bir aday yapıyor.
Teslim Kamyonu Olarak Küçük Yağ Kabarcıkları
Kırılgan RNA’yı hücrelerin içine güvenle sokmak büyük bir engeldir. İşte lipid nanopartiküller—yağa benzeyen moleküllerden yapılmış küçük küreler—devreye girer. Bunlar circRNA’yı sararak vücutta yolculuk ederken korur ve enjeksiyondan sonra hücrelere girmesine yardımcı olur. Araştırmacılar, circRNA’nın bu partiküllerle farelere intramüsküler, subkutan, intravenöz ve intranazal gibi yollarla verildiği çalışmalara odaklandı. Birden fazla bağımsız hayvan deneyinden gelen verileri inceleyip birleştirerek, bu circRNA–nanoparçacık aşılarının tümörleri ne kadar küçülttüğünü, enfeksiyonları ne ölçüde kontrol altına aldığını ve kilo kaybı veya ciddi toksisite gibi yan etkilerden kaçınıp kaçınmadığını değerlendirdiler.
Daha Güçlü Bağışıklık Askerleri, Küçük Tümörler
Birleştirilmiş hayvan verileri çarpıcı bir tablo çiziyor. On tümör çalışmasında, circRNA aşısı alan farelerin tümörleri, enjeksiyon kas içi, deri altı veya kan dolaşımına yapılsın fark etmeksizin, kontrol hayvanlara göre çok daha küçüktü. Aynı zamanda vücut ağırlığı—genel sağlık için kaba bir gösterge—stabil kaldı; bu da tedavinin yaygın bir toksisiteye yol açmadığını düşündürüyor. Ayrıntılı bağışıklık ölçümleri, ana beyaz kan hücrelerinin daha aktif hale geldiğini gösterdi: doğrudan anormal hücreleri öldüren T hücreleri genişledi, makrofajlar arttı ve işgalci parçacıkları bağışıklık sisteminin geri kalanına gösteren nöbetçi hücreler olan dendritik hücreler belirgin şekilde güçlendi. Bu değişiklikler, aşıların sadece mekanik olarak tümörleri hedef almadığını; bağışıklık sistemini kanser hücrelerini daha verimli tanıyıp yok edecek şekilde yeniden eğittiğini gösteriyor. 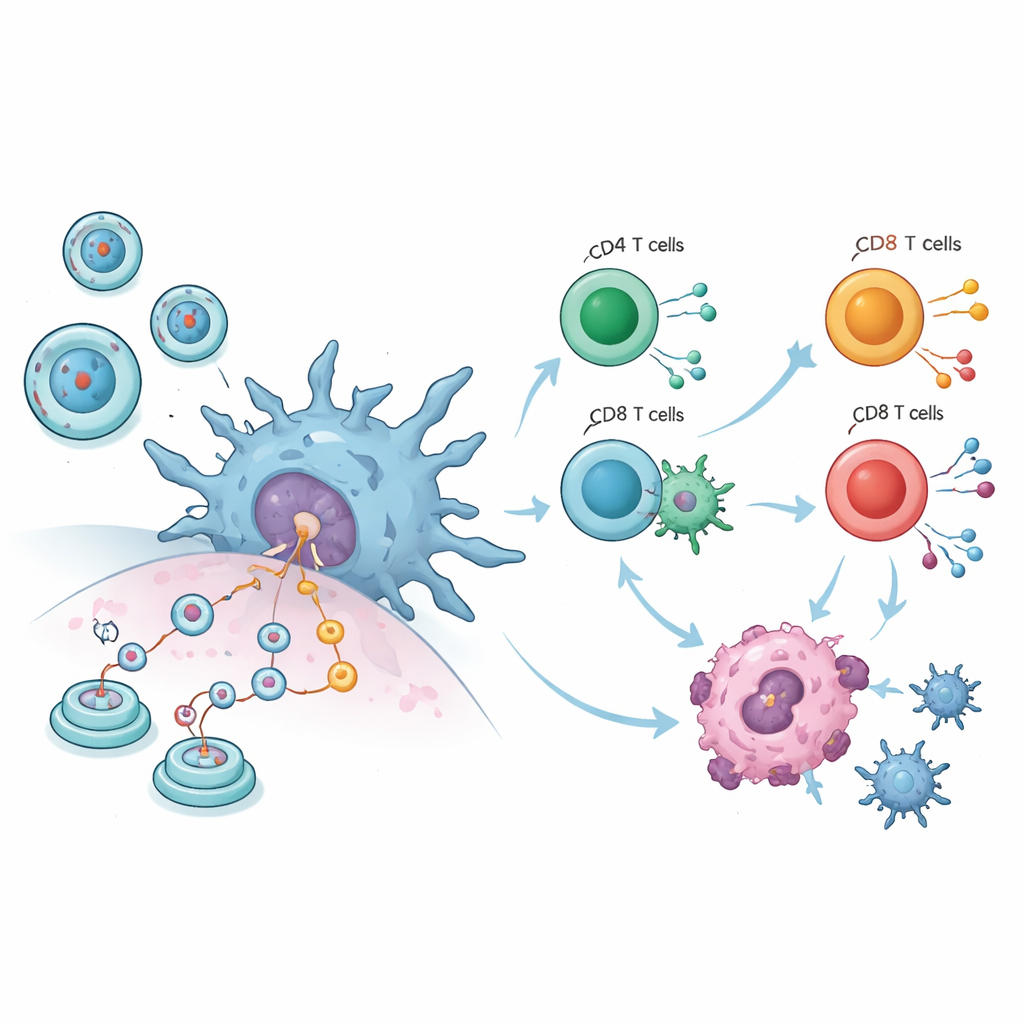
Aynı Araçla Virüslerle Mücadele
Aynı circRNA teknolojisi, influenza, Zika, SARS‑CoV‑2 ve diğer virüsler dahil bulaşıcı hastalık modellerinde de güçlü bulundu. Aşılanan farelerde kanda antikor düzeyleri hızla yükseldi, akciğerlerdeki viral yük azaldı ve interferon‑gamma ile interlökin‑4 gibi sinyal molekülleri arttı; bu, hem hızlı hem de daha uzun dönemli bağışıklık kollarının devreye girdiğini gösteriyor. Hava yolunun yüzeyini hedefleyen intranazal verilme, genellikle özellikle güçlü yerel koruma sağlarken, diğer yollar vücudun tamamında daha geniş yanıtları teşvik etti. Genel olarak, analiz tek bir circRNA platformunun, farklı hedeflere göre ayarlandığında, çok çeşitli patojenlere ve aynı zamanda kanserlere karşı korunmak için uyarlandığını düşündürüyor.
İnsan Hücrelerinde Mekanizmanın Kontrolü
Hayvan verilerinin ötesine geçmek için, yazarlar insan kan kaynaklı bağışıklık hücreleri kullanarak laboratuvar deneyleri yürüttü. Test proteini kodlayan saflaştırılmış circRNA ürettiler ve isteksizce nonspecifik alarm tetikleyebilecek çift iplikçikli RNA gibi kontaminantları temizlediler. Dendritik hücreler lipidle sarılmış circRNA’ya maruz kaldığında yeni proteini üretmeye başladı, olgunluğun ana yüzey belirteçlerini açtı ve IL‑6, IL‑1β ve TNF‑α gibi inflamatuar göndericiler saldı. Bu aktive olmuş dendritik hücreler insan T hücreleriyle karıştırıldığında, hem yardımcı hem de öldürücü T hücreleri etkinleşti ve interferon‑gamma salgıladı; bireysel yanıt veren hücreleri sayan bir testte daha fazla antijen‑spesifik T hücresi ortaya çıktı. Bu bulgular, circRNA’nın sadece farelerin değil, insan bağışıklık hücrelerini de hassas biçimde yönlendirebildiğini doğruluyor.
Umut, İhtiyat ve Sonraki Adımlar
Uzman olmayanlar için çıkarılacak sonuç şudur: lipid nanopartiküllerle taşınan dairesel RNA aşıları, mevcut RNA aşılarının daha dayanıklı, daha uzun etkili bir akrabası gibi görünüyor. Farelerde tümörleri küçültüyor, viral enfeksiyonları kontrol altına alıyor ve bunu belirgin zarar olmadan yapıyor; insan hücrelerinde ise hedefe yönelik savunma için gereken bağışıklık oyuncularını uyandırıyor. Ancak tüm bu kanıtlar hâlâ preklinik aşamada ve farklı hayvan türleri, hastalık tipleri ile enjeksiyon yolları değişken sonuçlar verdi. Bu yaklaşımın insanlarda ne kadar etkili olduğunu öğrenmek ve dozaj ile verilme şeklini ince ayarlamak için büyük, dikkatle tasarlanmış insan çalışmalarına ihtiyaç var. Bu engeller aşılırsa, circRNA aşıları kanser tedavisi ve gelecekteki bulaşıcı hastalık salgınlarını önlemede çok yönlü yeni bir araç olabilir.
Atıf: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
Anahtar kelimeler: dairesel RNA aşıları, lipid nanopartiküller, kanser immünoterapisi, bulaşıcı hastalık aşıları, T hücresi aktivasyonu