Clear Sky Science · de
Lipid-Nanopartikel‑Verabreichung eines circular RNA-Impfstoffs ruft starke Immunantworten hervor
Warum ein neuer Impfstofftyp wichtig ist
Impfstoffe auf Basis genetischen Materials haben die Bekämpfung von Infektionen wie COVID‑19 revolutioniert, doch die heutigen RNA‑Präparate können fragil und kurzlebig sein. Diese Studie untersucht einen nächsten Entwicklungsschritt, der eine robustere Form von RNA verwendet, verpackt in winzigen Fettbläschen, um das Immunsystem gegen Krebs und Infektionskrankheiten zu mobilisieren. Für Leserinnen und Leser bietet sie einen Ausblick darauf, wie künftige Impfstoffe leistungsfähiger, langanhaltender und leichter zu lagern und einzusetzen sein könnten. 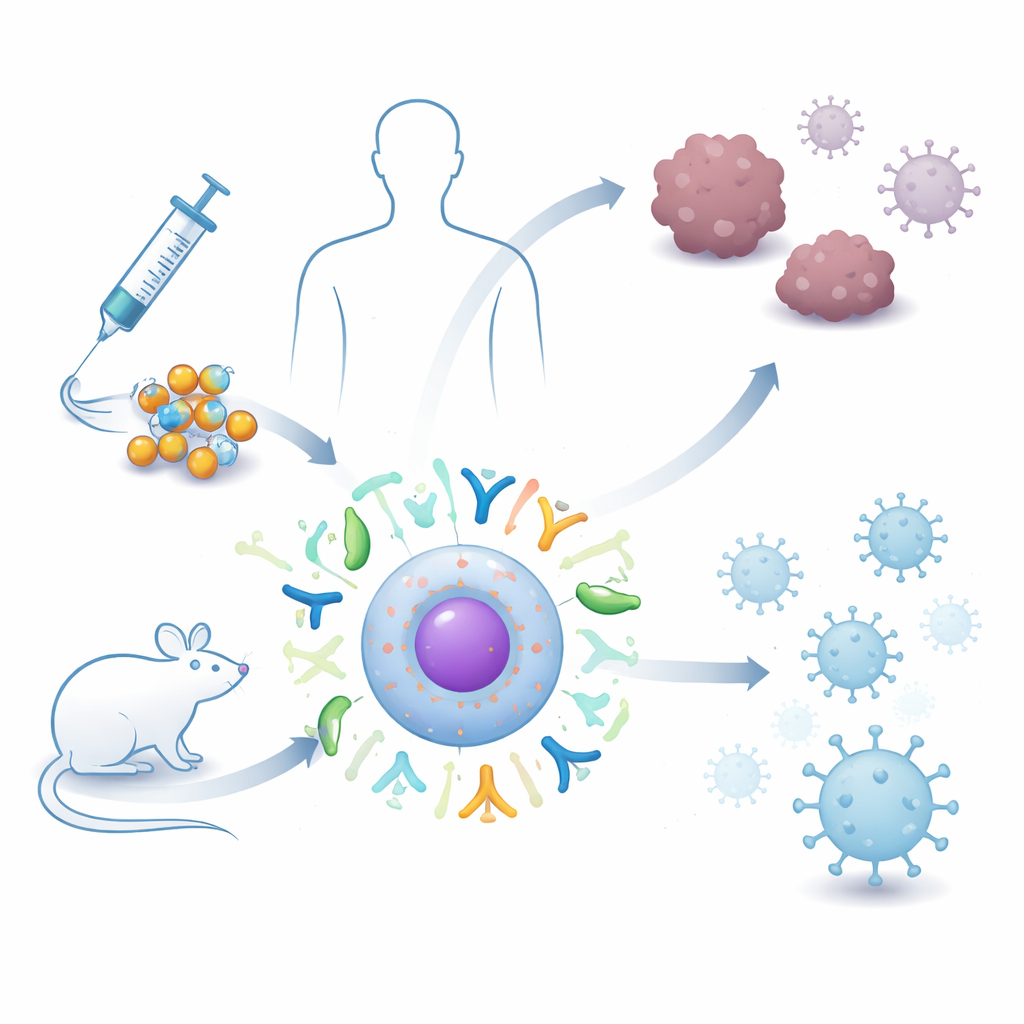
Ein schlaufenförmiges Bedienungshandbuch
Die meisten Menschen haben von mRNA gehört, der einzelsträngigen genetischen Botschaft, die in aktuellen RNA‑Impfstoffen verwendet wird. Circular RNA, oder circRNA, ist anders: Anstatt zwei Enden zu haben, bildet sie eine geschlossene Schleife. Diese einfache Änderung macht es den Enzymen des Körpers viel schwerer, sie zu zersetzen, sodass sie länger überdauert und Zellen über einen längeren Zeitraum zur Proteinsynthese anleiten kann. Die Autorinnen und Autoren erklären, dass circRNA so konstruiert werden kann, dass sie Baupläne für Tumormarker oder virale Bausteine trägt, und weil sie niemals in die DNA unserer Chromosomen eingebaut wird, vermeidet sie das Risiko einer dauerhaften Genveränderung. Zusammen mit der Möglichkeit, sie in großen Mengen herzustellen, machen diese Eigenschaften circRNA zu einer attraktiven Kandidatin für eine langlebige, vielseitige Impfstoffplattform.
Winzige Fettbläschen als Transportfahrzeuge
Fragile RNA sicher in Zellen zu bringen ist eine große Hürde. Hier kommen Lipidnanopartikel—winzige Kugeln aus fettähnlichen Molekülen—ins Spiel. Sie umhüllen die circRNA, schützen sie auf dem Weg durch den Körper und helfen ihr, nach der Injektion in Zellen einzudringen. Die Forschenden konzentrierten sich auf Studien, in denen circRNA Mäusen mithilfe dieser Partikel verabreicht wurde, über Wege wie intramuskuläre, subkutane, intravenöse und intranasale Injektion. Durch die Auswertung und Kombination von Daten aus mehreren unabhängigen Tierexperimenten fragten sie, wie gut diese circRNA–Nanopartikel‑Impfstoffe Tumore verkleinern, Infektionen kontrollieren und Nebenwirkungen wie Gewichtsverlust oder ernsthafte Toxizität vermeiden.
Stärkere Immun‑Kämpfer, kleinere Tumore
Die zusammengefassten Tierdaten zeichnen ein eindrückliches Bild. In zehn Tumorstudien hatten Mäuse, die circRNA‑Impfstoffe erhielten, deutlich kleinere Tumore als Kontrolltiere, unabhängig davon, ob die Injektion in den Muskel, unter die Haut oder in die Blutbahn erfolgte. Gleichzeitig blieb das Körpergewicht—ein grober Indikator für den allgemeinen Gesundheitszustand—stabil, was darauf hindeutet, dass die Behandlung nicht allgemein toxisch war. Detaillierte Immunmessungen zeigten, dass wichtige weiße Blutzellen aktiver wurden: zytotoxische T‑Zellen, die abnormalen Zellen direkt töten, vermehrten sich, Makrophagen nahmen zu, und dendritische Zellen—die Wächter, die Bruchstücke von Eindringlingen dem Immunsystem präsentieren—wurden deutlich verstärkt. Diese Veränderungen deuten darauf hin, dass die Impfstoffe Tumore nicht nur mechanisch angreifen; sie bilden das Immunsystem um, sodass es Krebszellen effizienter erkennt und vernichtet. 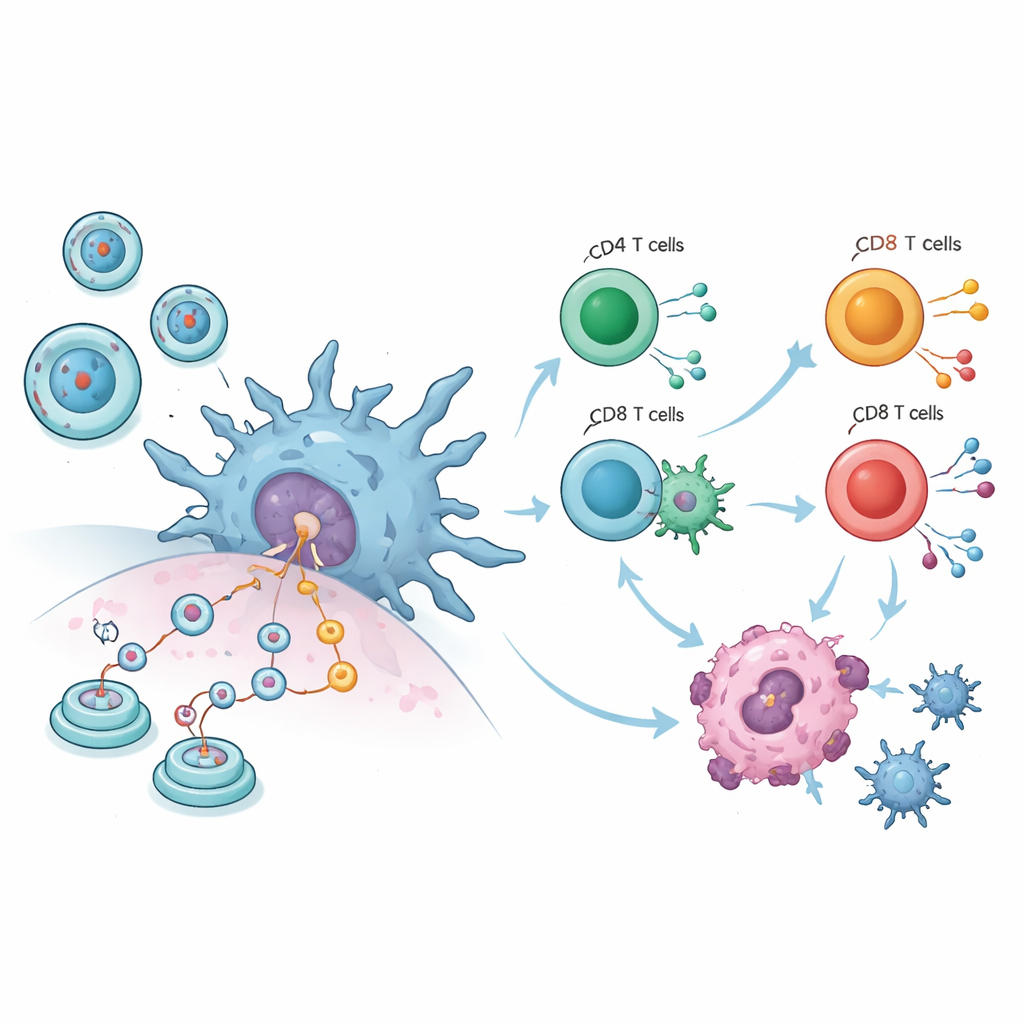
Mit demselben Werkzeug gegen Viren
Die gleiche circRNA‑Technologie erwies sich auch in Modellen zu Infektionskrankheiten als wirkungsvoll, darunter Influenza, Zika, SARS‑CoV‑2 und andere Viren. Bei geimpften Mäusen stiegen die Antikörperspiegel im Blut stark an, die Viruslast in der Lunge sank, und Signalstoffe wie Interferon‑gamma und Interleukin‑4 nahmen zu—ein Hinweis darauf, dass sowohl die schnelle als auch die längerfristige Komponente des Immunsystems aktiviert wurden. Die intranasale Verabreichung, die die Schleimhaut der Atemwege adressiert, erzeugte oft besonders starken lokalen Schutz, während andere Wege eher systemischere Reaktionen im ganzen Körper förderten. Insgesamt legt die Analyse nahe, dass eine einzige circRNA‑Plattform, auf unterschiedliche Ziele abgestimmt, zum Schutz gegen eine Vielzahl von Krankheitserregern sowie gegen Krebs adaptiert werden könnte.
Überprüfung des Mechanismus in menschlichen Zellen
Um über Tierdaten hinauszugehen, führten die Autorinnen und Autoren Laborversuche mit aus menschlichem Blut gewonnenen Immunzellen durch. Sie stellten gereinigte circRNA her, die ein Testprotein codierte, und entfernten kontaminierende doppelsträngige RNA, die unspezifische Alarmsignale auslösen könnte. Wurden dendritische Zellen mit lipid‑ummantelte circRNA exponiert, begannen sie, das neue Protein zu produzieren, aktivierten wichtige Oberflächenmarker der Reife und setzten entzündliche Botenstoffe wie IL‑6, IL‑1β und TNF‑α frei. Wenn diese aktivierten dendritischen Zellen mit menschlichen T‑Zellen gemischt wurden, schalteten sowohl Helfer‑ als auch Killer‑T‑Zellen ein und sezernierten Interferon‑gamma, und in einem Test, der einzelne reagierende Zellen zählt, traten mehr antigenspezifische T‑Zellen auf. Diese Ergebnisse bestätigen, dass circRNA menschliche Immunzellen präzise ansteuern kann, nicht nur die von Mäusen.
Versprechen, Vorbehalte und die nächsten Schritte
Für Nichtfachleute lautet die Quintessenz, dass zirkuläre RNA‑Impfstoffe, getragen von Lipidnanopartikeln, wie ein robusterer, länger wirkender Verwandter der heutigen RNA‑Präparate erscheinen. In Mäusen verkleinern sie Tumore, dämpfen virale Infektionen und tun dies ohne offensichtlichen Schaden, während sie in menschlichen Zellen genau jene Immunakteure wecken, die für eine gezielte Abwehr nötig sind. Dennoch basieren all diese Erkenntnisse noch auf präklinischen Daten, und unterschiedliche Tierstämme, Krankheitsmodelle und Injektionswege führten zu variablen Ergebnissen. Große, sorgfältig gestaltete Humanstudien werden erforderlich sein, um zu ermitteln, wie gut dieser Ansatz beim Menschen wirkt und um Dosierung und Verabreichung zu optimieren. Werden diese Hürden genommen, könnten circRNA‑Impfstoffe zu einem vielseitigen neuen Instrument in der Krebsbehandlung und der Prävention künftiger Ausbrüche von Infektionskrankheiten werden.
Zitation: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
Schlüsselwörter: zirkuläre RNA-Impfstoffe, Lipidnanopartikel, Krebsimmuntherapie, Impfstoffe gegen Infektionskrankheiten, T‑Zell‑Aktivierung