Clear Sky Science · ru
Доставка кольцевой РНК в липидных наночастицах вызывает сильные иммунные ответы
Почему важен новый тип вакцины
Вакцины на основе генетического материала изменили подход к борьбе с инфекциями, такими как COVID‑19, но современные РНК‑препараты могут быть хрупкими и кратковременными. В этом исследовании рассматривается подход следующего поколения, использующий более устойчивую форму РНК, упакованную в крошечные жировые пузырьки, чтобы стимулировать иммунную систему против рака и инфекционных болезней. Для читателя это даёт представление о том, как будущие вакцины могут стать более мощными, более длительно действующими и проще в хранении и применении по всему миру. 
Инструкция в виде петли
Большинство людей слышали о мРНК — одноцепочечном генетическом послании, используемом в современных РНК‑вакцинах. Кольцевая РНК, или circRNA, отличается: вместо двух концов она образует замкнутую петлю. Это простое изменение делает её гораздо труднее для расщепления ферментами организма, поэтому она дольше сохраняется и может дольше направлять клетки на синтез белков. Авторы объясняют, что circRNA можно сконструировать так, чтобы она несла чертежи опухолевых маркеров или вирусных фрагментов, и поскольку она не встраивается в ДНК наших хромосом, она не несёт риска постоянного изменения генов. В сочетании со способностью к массовому производству эти свойства делают circRNA привлекательным кандидатом для прочной и гибкой платформы вакцин.
Крошечные жировые пузырьки в роли грузовиков‑доставщиков
Безопасная доставка хрупкой РНК в клетки — серьёзная проблема. Здесь на помощь приходят липидные наночастицы — крошечные сферические структуры из молекул, похожих на жиры. Они обволакивают circRNA, защищая её во время путешествия по организму и помогая проникнуть в клетки после инъекции. Исследователи сосредоточились на работах, где circRNA доставляли мышам с помощью таких частиц через разные пути: мышечно, подкожно, внутривенно и интраназально. Объединив и сопоставив данные из нескольких независимых экспериментов на животных, они оценивали, насколько эффективно эти вакцины на основе circRNA и наночастиц уменьшают опухоли, контролируют инфекции и избегают побочных эффектов, таких как потеря веса или серьёзная токсичность.
Сильнее иммунные солдаты, меньшие опухоли
Суммарные данные на животных рисуют впечатляющую картину. В десяти исследованиях опухолей у мышей, получивших вакцины на основе circRNA, опухоли были значительно меньше, чем у контрольных животных, независимо от того, был ли укол сделан в мышцу, под кожу или в кровоток. При этом масса тела — грубый показатель общего состояния здоровья — оставалась стабильной, что указывает на отсутствие выраженной токсичности. Детальные иммунологические измерения показали повышение активности ключевых белых кровяных клеток: увеличивалось количество цитотоксических Т‑клеток, возрастало число макрофагов, а дендритные клетки — стражи, представляющие фрагменты захватчиков остальной иммунной системе — заметно активировались. Эти изменения говорят о том, что вакцины действуют не механически на опухоли, а переобучают иммунную систему распознавать и эффективнее уничтожать раковые клетки. 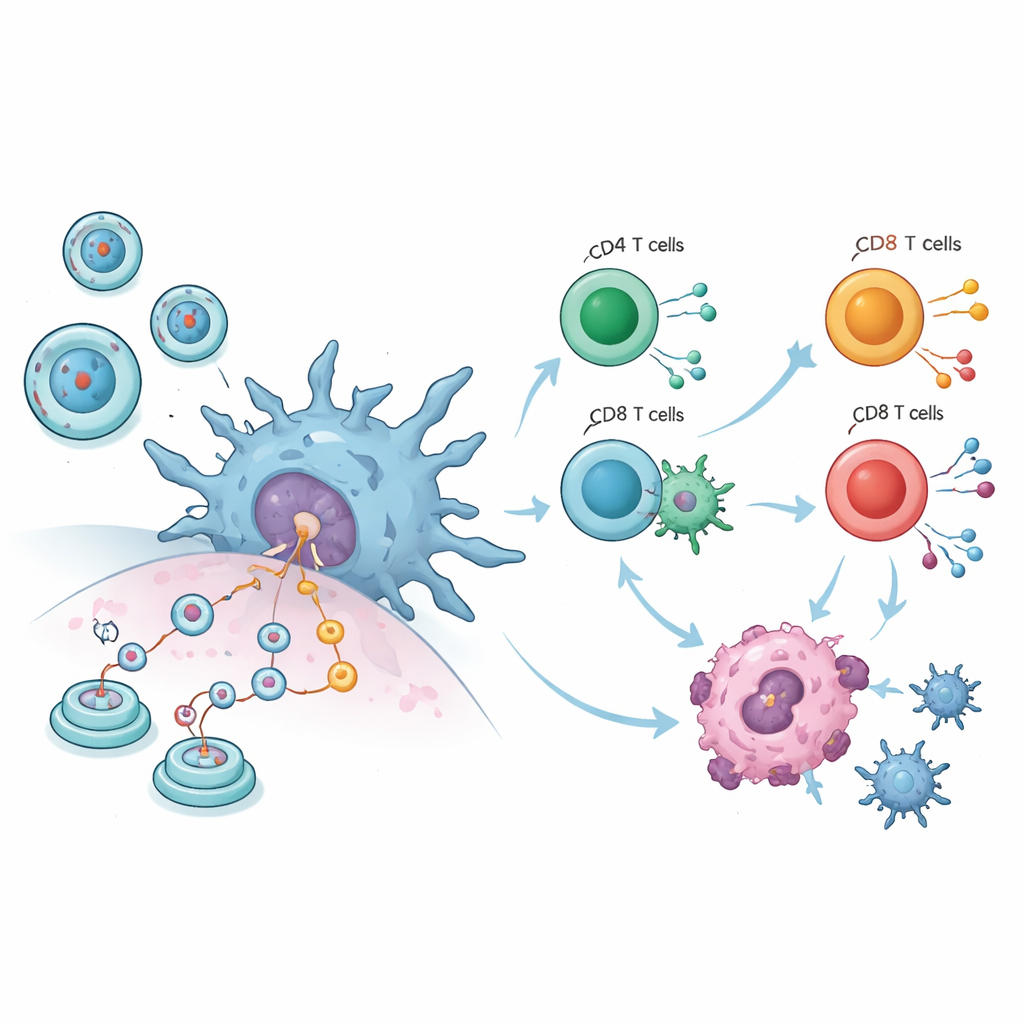
Борьба с вирусами тем же инструментом
Та же технология circRNA оказалась эффективной и в моделях инфекционных заболеваний, включая грипп, Зику, SARS‑CoV‑2 и другие вирусы. У вакцинированных мышей резко повысился уровень антител в крови, снизилась вирусная нагрузка в лёгких, а такие сигнальные молекулы, как интерферон‑гамма и интерлейкин‑4, увеличились, показывая вовлечение как быстрых, так и более длительных звеньев иммунитета. Интраназальная доставка, нацеленная на слизистую дыхательных путей, часто обеспечивала особенно сильную местную защиту, в то время как другие пути давали более системные ответы. В целом анализ указывает на то, что единая платформа circRNA, настроенная на разные мишени, может быть адаптирована для защиты от широкого круга патогенов, а также от рака.
Проверка механизма в человеческих клетках
Чтобы выйти за пределы данных на животных, авторы провели лабораторные эксперименты на иммунных клетках, полученных из крови человека. Они получили очищенную circRNA, кодирующую тестовый белок, и удалили загрязняющие двухцепочечные РНК, которые могли бы вызывать неспецифические сигнальные реакции. Когда дендритные клетки подвергались действию липид‑упакованной circRNA, они начали синтезировать новый белок, включили ключевые поверхностные маркеры созревания и выделяли провоспалительные медиаторы, такие как IL‑6, IL‑1β и TNF‑α. При смешивании этих активированных дендритных клеток с человеческими Т‑клетками и вспомогательные, и цитотоксические Т‑клетки активировались и выделяли интерферон‑гамма, а в анализе, подсчитывающем отдельные реагирующие клетки, появлялось больше антиген‑специфичных Т‑клеток. Эти данные подтверждают, что circRNA может точно направлять ответ именно человеческих иммунных клеток, а не только клеток мышей.
Обещание, оговорки и что дальше
Для неспециалистов вывод таков: вакцины на основе кольцевой РНК, доставляемые липидными наночастицами, выглядят как более прочный и долгодействующий родственник современных РНК‑препаратов. У мышей они уменьшают опухоли, сдерживают вирусные инфекции и делают это без очевидного вреда, а в человеческих клетках пробуждают ключевые звенья иммунной защиты. Однако все эти данные пока доклинические, и различные штаммы животных, типы заболеваний и пути введения давали переменные результаты. Чтобы понять, насколько этот подход эффективен у людей, и оптимизировать дозирование и способы доставки, потребуются крупные, тщательно спланированные клинические испытания. Если эти барьеры будут преодолены, вакцины на основе circRNA могут стать универсальным новым инструментом для лечения рака и предотвращения будущих вспышек инфекционных заболеваний.
Цитирование: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
Ключевые слова: вакцины на основе циркулярной РНК, липидные наночастицы, иммунотерапия рака, вакцины против инфекционных заболеваний, активация Т‑клеток