Clear Sky Science · ar
توصيل اللقاح القائم على RNA الدائري بجسيمات دهنية نانوية يحفز استجابات مناعية قوية
لماذا يهم نوع جديد من اللقاحات
لقد غيّرت اللقاحات المبنية على المادة الجينية طريقة مواجهة الإصابات مثل كوفيد‑19، لكن لقاحات RNA الحالية قد تكون هشة وقصيرة الأمد. تستكشف هذه الدراسة نهجاً من الجيل التالي يستخدم شكلاً أكثر متانة من RNA، مغلفاً في فقاعات دهنية صغيرة، لتحفيز الجهاز المناعي ضد كل من السرطان والأمراض المعدية. تقدم هذه القراءة لمحة عن كيف قد تصبح اللقاحات المستقبلية أقوى، أطول أمداً، وأسهل في التخزين والاستخدام حول العالم. 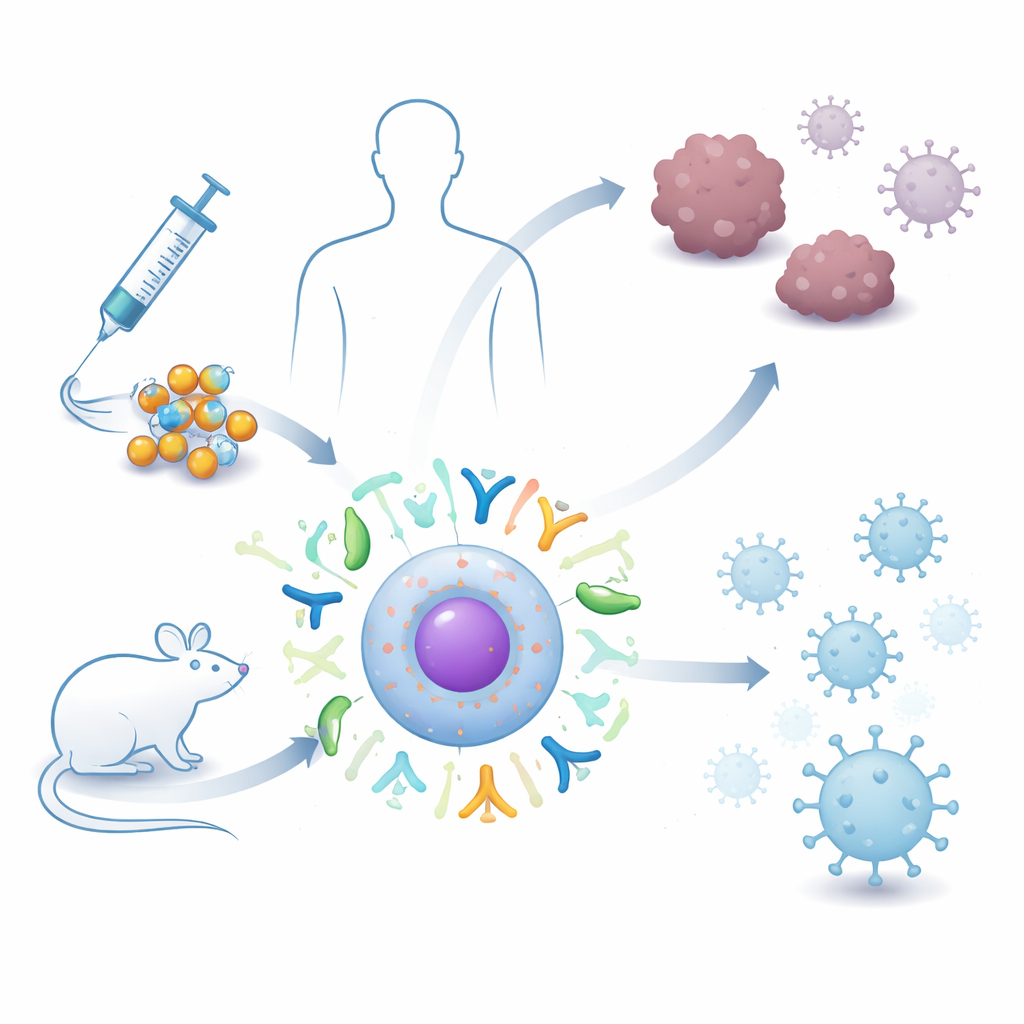
دليل تعليمات على شكل حلقة
سمع معظم الناس عن mRNA، الرسالة الوراثية ذات السلسلة الواحدة المستخدمة في لقاحات RNA الحالية. RNA الدائري، أو circRNA، مختلف: بدلاً من وجود طرفين، يشكل حلقة مغلقة. هذا التغيير البسيط يجعل إنزيمات الجسم أكثر صعوبة في تفكيكه، لذلك يبقى لفترة أطول ويمكنه توجيه الخلايا لإنتاج بروتينات لفترة ممتدة. يشرح المؤلفون أن circRNA يمكن تصميمه لحمل مخططات لمؤشرات الأورام أو أجزاء فيروسية، وبما أنه لا يدخل إلى DNA في كروموسوماتنا، فإنه يتفادى خطر تغيير جيناتنا بشكل دائم. مع إمكانية تصنيعه بكميات كبيرة، تجعل هذه الخصائص circRNA مرشحاً جذاباً لمنصة لقاحات مرنة وطويلة الأمد.
فقاعات دهنية صغيرة كـ"شاحنات توصيل"
إدخال RNA الهش بأمان إلى الخلايا هو عقبة رئيسية. هنا تأتي أهمية الجسيمات النانوية الدهنية—كرات صغيرة مصنوعة من جزيئات شبيهة بالدهون. تلتف هذه الجسيمات حول circRNA، تحميه أثناء انتقاله في الجسم وتساعده على الدخول إلى الخلايا بعد الحقن. ركز الباحثون على دراسات وُصل فيها circRNA إلى الفئران باستخدام هذه الجسيمات، عبر طرق مثل الحقن العضلي، تحت الجلد، داخل الوريد، والأنفي. من خلال مراجعة ودمج بيانات من تجارب حيوانية مستقلة متعددة، بحثوا في مدى فعالية هذه اللقاحات القائمة على circRNA–الجسيمات النانوية في تقليص الأورام، السيطرة على العدوى، وتجنب الآثار الجانبية مثل فقدان الوزن أو السمية الخطيرة.
جنود مناعيون أقوى، أورام أصغر
تصوّر بيانات الحيوانات المجمعة صورة لافتة. عبر عشر دراسات للأورام، كانت الأورام لدى الفئران التي تلقت لقاحات circRNA أصغر بكثير مقارنة بالحيوانات الضابطة، بغض النظر عن ما إذا تم حقن اللقاح في العضلات، تحت الجلد، أو في مجرى الدم. في الوقت ذاته، ظل وزن الجسم—كمؤشر تقريبي على الصحة العامة—ثابتاً، ما يوحي بأن العلاج لم يكن ساماً على نطاق واسع. أظهرت القياسات المناعية التفصيلية أن خلايا الدم البيضاء الرئيسية أصبحت أكثر نشاطاً: توسعت الخلايا التائية القاتلة للخلايا الشاذة، ازدادت البلعميات، وزادت الخلايا الشجيرية—الحراس الذين يعرضون شظايا المهاجمين لباقي الجهاز المناعي—بشكل ملحوظ. تشير هذه التغيرات إلى أن اللقاحات لا تهاجم الأورام ميكانيكياً فقط؛ بل تعيد تعليم الجهاز المناعي للتعرف على خلايا السرطان وتدميرها بكفاءة أكبر. 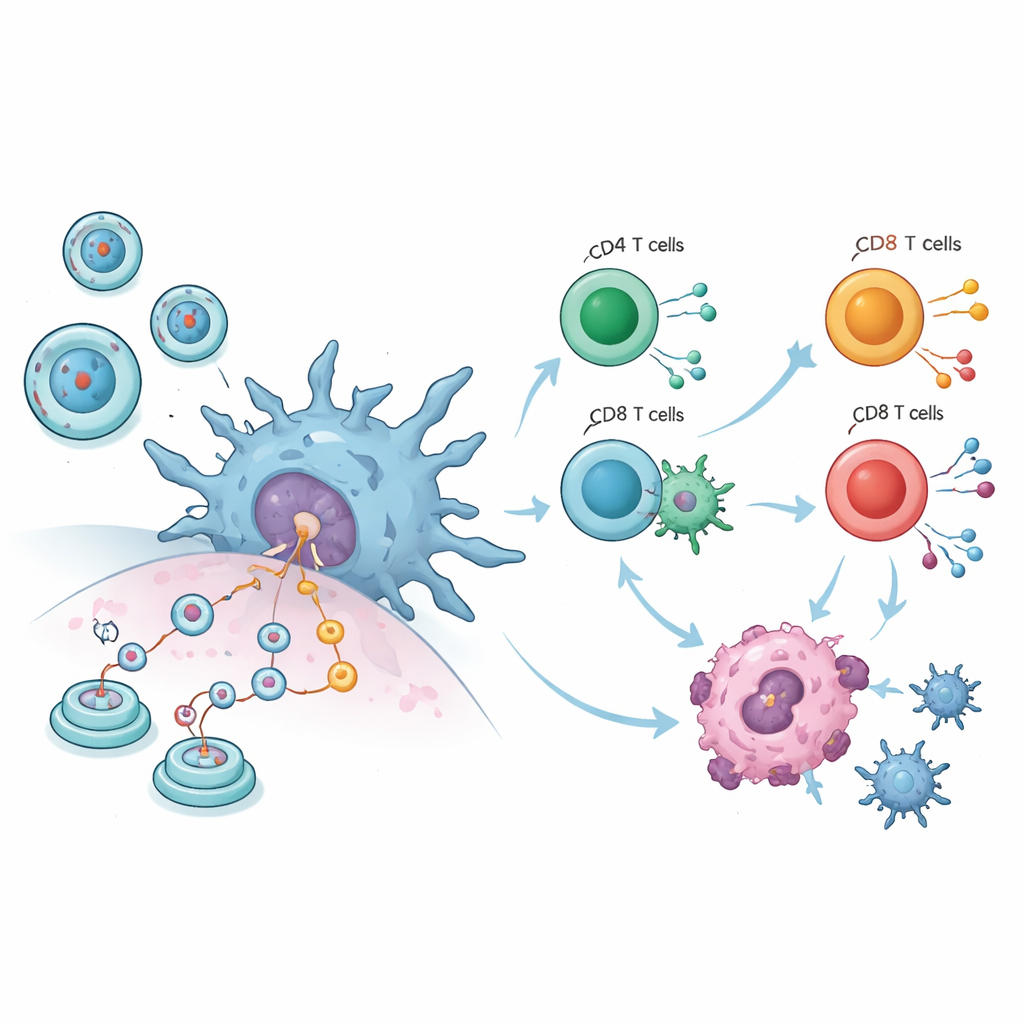
مكافحة الفيروسات بنفس الأداة
أثبتت تقنية circRNA نفسها أيضاً قوية في نماذج الأمراض المعدية، بما في ذلك الإنفلونزا، زيكا، SARS‑CoV‑2 وفيروسات أخرى. في الفئران المطعّمة ارتفعت مستويات الأجسام المضادة في الدم بشكل حاد، انخفضت حمولات الفيروس في الرئتين، وزادت جزيئات الإشارة مثل إنترفيرون‑غاما وإنترلوكين‑4، مما يُظهر أن فرعي الاستجابة المناعية السريعة وطويلة الأمد شاركا معاً. غالباً ما أنتج الإعطاء عبر الأنف، الذي يستهدف بطانة المجاري الهوائية، حماية محلية قوية بشكل خاص، بينما فضّلت طرق أخرى استجابات أوسع النطاق في الجسم بأكمله. بشكل عام، توحي التحليلات بأن منصة circRNA واحدة قابلة للضبط نحو أهداف مختلفة، يمكن تكييفها للحماية من مجموعة واسعة من العوامل الممرضة وكذلك من السرطانات.
التحقق من الآلية في خلايا بشرية
للانتقال إلى ما بعد بيانات الحيوانات، أجرى المؤلفون تجارب مختبرية باستخدام خلايا مناعية مشتقة من دم بشري. أنتجوا circRNA مُنَقّى يشفر بروتين اختبار وأزالوا RNA مزدوج السلسلة الملوث الذي قد يطلق إشارات إنذار غير محددة. عندما تعرّضت الخلايا الشجيرية لـ circRNA المغلف بالدهون، بدأت في صنع البروتين الجديد، وأشعلت علامات سطحية رئيسية للنضج، وأطلقت رسوليات التهابية مثل IL‑6، IL‑1β، وTNF‑α. عندما خُلطت هذه الخلايا الشجيرية المنشّطة مع الخلايا التائية البشرية، نشطت الخلايا التائية المساعدة والقاتلة وأفرزت إنترفيرون‑غاما، وظهرت خلايا تائية أكثر تحديداً للمستضد في اختبار يعد الخلايا المستجيبة بشكل فردي. تؤكد هذه النتائج أن circRNA يمكنه توجيه الخلايا المناعية البشرية بدقة، وليس خلايا الفئران فقط.
الوعد والتحفظات والخطوات التالية
بالنسبة لغير المتخصصين، الخلاصة أن لقاحات RNA الدائري، المحمولة بجسيمات دهنية نانوية، تبدو كنسخة أكثر متانة وطويلة الأمد من لقاحات RNA الحالية. في الفئران تقلل الأورام، تكبح العدوى الفيروسية، وتفعل ذلك دون أضرار واضحة، بينما في الخلايا البشرية توقظ اللاعبين المناعيين الضروريين للدفاع الموجه. ومع ذلك، تظل كل هذه الأدلة قبل سريرية، وأنتجت سلالات حيوانية وأنواع الأمراض وطرق الحقن المختلفة نتائج متباينة. ستكون هناك حاجة إلى تجارب بشرية كبيرة مصممة بعناية لمعرفة مدى فعالية هذا النهج في البشر ولضبط الجرعات وطرق التوصيل. إذا جرى اجتياز تلك العقبات، قد تصبح لقاحات circRNA أداة متعددة الاستخدامات لعلاج السرطان والوقاية من التفشيات المستقبلية للأمراض المعدية.
الاستشهاد: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
الكلمات المفتاحية: لقاحات RNA الدائري, الجسيمات النانوية الدهنية, المناعة لعلاج السرطان, لقاحات الأمراض المعدية, تنشيط الخلايا التائية