Clear Sky Science · es
Entrega mediante nanopartículas lipídicas de una vacuna de ARN circular induce respuestas inmunitarias potentes
Por qué importa un nuevo tipo de vacuna
Las vacunas basadas en material genético han transformado la forma en que combatimos infecciones como la COVID-19, pero las vacunas de ARN actuales pueden ser frágiles y de acción relativamente breve. Este estudio explora un enfoque de próxima generación que emplea una forma de ARN más resistente, empaquetada en pequeñas burbujas grasas, para estimular el sistema inmunitario frente al cáncer y las enfermedades infecciosas. Para el lector, ofrece una idea de cómo las futuras vacunas podrían ser más potentes, durar más tiempo y ser más fáciles de almacenar y usar en todo el mundo. 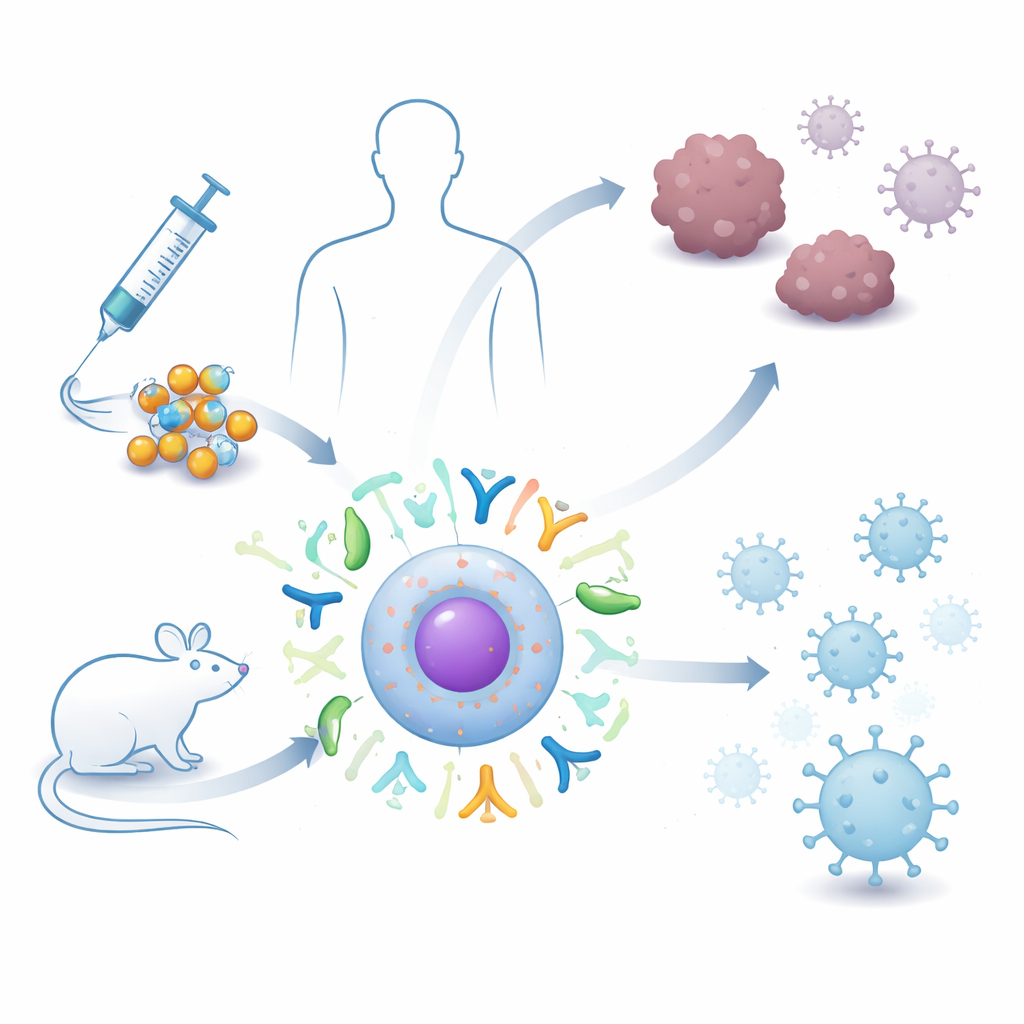
Un manual de instrucciones en forma de lazo
La mayoría conoce el ARNm, el mensaje genético de cadena simple usado en las vacunas de ARN actuales. El ARN circular, o circRNA, es distinto: en lugar de tener dos extremos, forma un lazo cerrado. Este cambio sencillo lo hace mucho más difícil de degradar por las enzimas del cuerpo, por lo que sobrevive más tiempo y puede dirigir a las células para producir proteínas durante un periodo prolongado. Los autores explican que el circRNA puede diseñarse para llevar planos de marcadores tumorales o fragmentos virales y que, dado que nunca se integra en el ADN de nuestros cromosomas, evita el riesgo de alterar permanentemente nuestros genes. Combinado con la posibilidad de fabricarse en grandes cantidades, estas propiedades convierten al circRNA en un candidato atractivo para una plataforma vacunal duradera y flexible.
Pequeñas burbujas grasas como camiones de entrega
Lograr que el ARN frágil llegue con seguridad a las células es un obstáculo importante. Aquí entran las nanopartículas lipídicas—esferas diminutas hechas de moléculas similares a las grasas. Envuelven el circRNA, protegiéndolo mientras viaja por el cuerpo y ayudando a que penetre en las células tras la inyección. Los investigadores se centraron en estudios en los que el circRNA se administró a ratones usando estas partículas, por vías como intramuscular, subcutánea, intravenosa e intranasal. Al revisar y combinar datos de múltiples experimentos animales independientes, preguntaron qué tan bien estas vacunas de circRNA–nanopartícula reducen tumores, controlan infecciones y evitan efectos secundarios como pérdida de peso o toxicidad grave.
Soldados inmunitarios más fuertes, tumores más pequeños
Los datos combinados en animales dibujan un panorama llamativo. En diez estudios tumorales, los ratones que recibieron vacunas de circRNA tenían tumores mucho más pequeños que los animales control, independientemente de si la inyección fue en el músculo, bajo la piel o en el torrente sanguíneo. Al mismo tiempo, el peso corporal—un marcador aproximado de salud general—se mantuvo estable, lo que sugiere que el tratamiento no era tóxico de forma general. Medidas inmunitarias detalladas mostraron que células clave de la sangre blanca se activaron: los linfocitos T citotóxicos se expandieron, aumentaron los macrófagos y las células dendríticas—los centinelas que presentan fragmentos de invasores al resto del sistema inmunitario—se vieron claramente potenciadas. Estos cambios indican que las vacunas no solo atacan los tumores de forma mecánica; reeducan al sistema inmunitario para reconocer y destruir las células cancerosas con mayor eficacia. 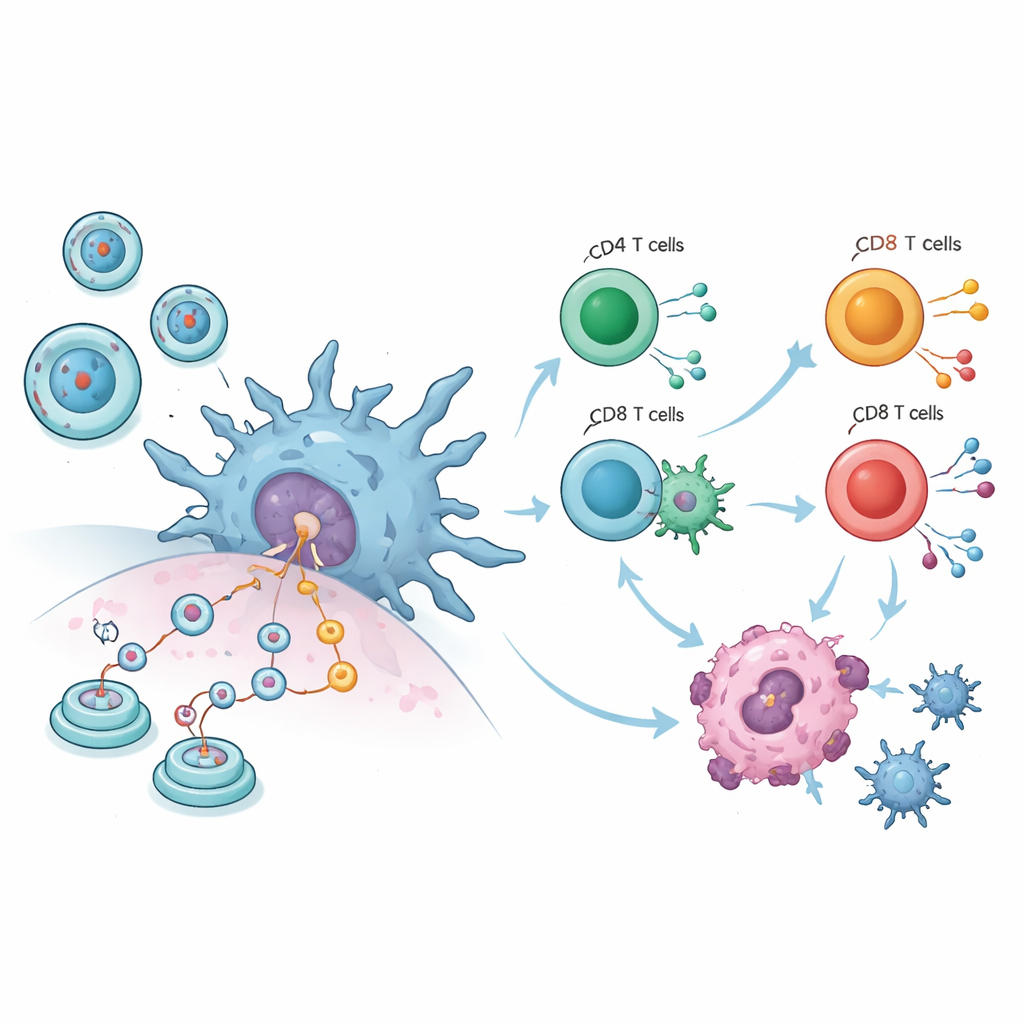
Combatir virus con la misma herramienta
La misma tecnología de circRNA también demostró ser potente en modelos de enfermedades infecciosas, incluidas la influenza, Zika, SARS-CoV-2 y otros virus. En ratones vacunados, los niveles de anticuerpos en sangre aumentaron con fuerza, las cargas virales en el pulmón cayeron y moléculas de señalización como el interferón gamma y la interleucina-4 se incrementaron, mostrando que tanto los brazos rápidos como los de más largo plazo del sistema inmune se activaron. La administración intranasal, que dirige la mucosa de las vías respiratorias, produjo a menudo una protección local especialmente intensa, mientras que otras vías favorecieron respuestas más amplias por todo el organismo. En conjunto, el análisis sugiere que una sola plataforma de circRNA, ajustada a distintos objetivos, podría adaptarse para proteger frente a una amplia gama de patógenos además de frente a cánceres.
Comprobación del mecanismo en células humanas
Para ir más allá de los datos animales, los autores realizaron experimentos de laboratorio con células inmunitarias humanas derivadas de sangre. Produjeron circRNA purificado que codificaba una proteína de prueba y eliminaron ARN de doble cadena contaminante que podría desencadenar señales de alarma inespecíficas. Cuando las células dendríticas fueron expuestas a circRNA envuelto en lípidos, empezaron a fabricar la nueva proteína, activaron marcadores de superficie asociados a la madurez y liberaron mensajeros inflamatorios como IL-6, IL-1β y TNF-α. Al mezclar estas células dendríticas activadas con linfocitos T humanos, tanto las células T colaboradoras como las citotóxicas se activaron y secretaron interferón gamma, y aparecieron más células T específicas de antígeno en un ensayo que cuenta células individuales respondientes. Estos hallazgos confirman que el circRNA puede dirigir con precisión células inmunitarias humanas, no solo las de los ratones.
Promesa, salvedades y siguientes pasos
Para no especialistas, la conclusión es que las vacunas de ARN circular, transportadas por nanopartículas lipídicas, parecen un pariente más resistente y de acción más prolongada de las vacunas de ARN actuales. En ratones reducen tumores, atenúan infecciones virales y lo hacen sin daños evidentes, mientras que en células humanas activan a los agentes inmunitarios necesarios para una defensa dirigida. Sin embargo, toda esta evidencia sigue siendo preclínica, y distintas cepas animales, tipos de enfermedad y vías de inyección produjeron resultados variables. Serán necesarios ensayos humanos amplios y bien diseñados para saber qué tan bien funciona este enfoque en personas y para afinar dosis y vías de administración. Si se superan esos obstáculos, las vacunas de circRNA podrían convertirse en una herramienta nueva y versátil para tratar el cáncer y prevenir futuros brotes de enfermedades infecciosas.
Cita: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
Palabras clave: vacunas de ARN circular, nanopartículas lipídicas, inmunoterapia contra el cáncer, vacunas contra enfermedades infecciosas, activación de células T