Clear Sky Science · nl
Lipide-nanodeeltjes als drager van circulair RNA-vaccin wekken krachtige immuunresponsen op
Waarom een nieuw soort vaccin ertoe doet
Vaccins op basis van genetisch materiaal hebben de manier veranderd waarop we infecties zoals COVID-19 bestrijden, maar de huidige RNA-injecties kunnen kwetsbaar en van korte duur zijn. Deze studie onderzoekt een volgende generatie aanpak die een robuustere vorm van RNA gebruikt, verpakt in piepkleine vetbellen, om het immuunsysteem tegen zowel kanker als infectieziekten te stimuleren. Voor lezers biedt het een blik op hoe toekomstige vaccins krachtiger, duurzamer en makkelijker te bewaren en toe te passen over de hele wereld zouden kunnen worden. 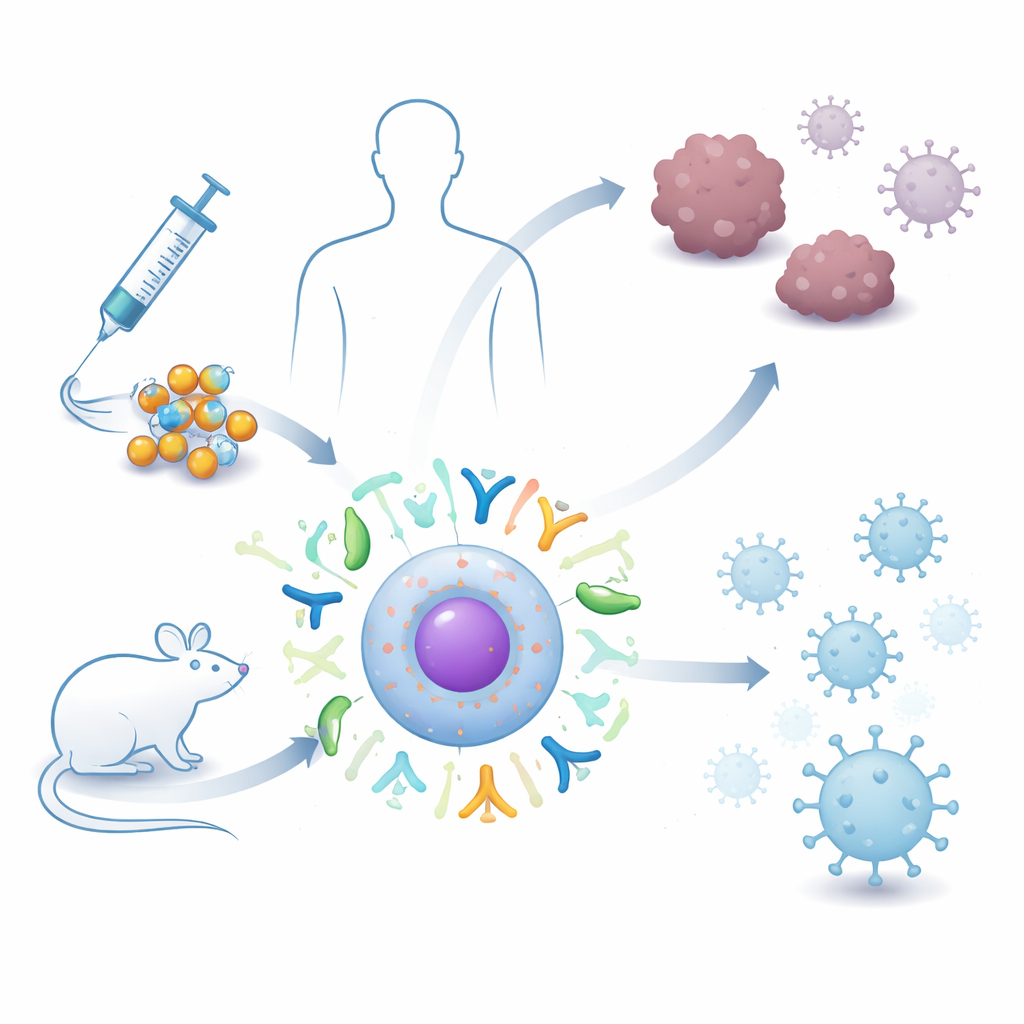
Een instructiehandleiding in lusvorm
De meeste mensen hebben gehoord van mRNA, het enkelstrengs genetische bericht dat in huidige RNA-vaccins wordt gebruikt. Circulair RNA, of circRNA, is anders: in plaats van twee uiteinden vormt het een gesloten lus. Deze eenvoudige verandering maakt het veel moeilijker voor de enzymen van het lichaam om het af te breken, zodat het langer overleeft en gedurende een langere periode cellen kan aansturen om eiwitten te produceren. De auteurs leggen uit dat circRNA zo kan worden ontworpen dat het blauwdrukken draagt voor tumormerkers of virale onderdelen, en omdat het nooit in het DNA van onze chromosomen terechtkomt, vermijdt het het risico van permanente wijziging van onze genen. Gecombineerd met de mogelijkheid om in grote hoeveelheden geproduceerd te worden, maken deze eigenschappen circRNA tot een aantrekkelijk kandidaat voor een duurzame, flexibele vaccinplatform.
Kleine vetbellen als bezorgwagens
Kwetsbaar RNA veilig in cellen krijgen is een grote uitdaging. Hier komen lipide-nanodeeltjes — piepkleine bolletjes gemaakt van vetachtige moleculen — in beeld. Zij wikkelen zich rond het circRNA, beschermen het tijdens de reis door het lichaam en helpen het na injectie in cellen terecht te komen. De onderzoekers concentreerden zich op studies waarin circRNA aan muizen werd toegediend met deze deeltjes, via routes zoals intramusculaire, subcutane, intraveneuze en intranasale injectie. Door gegevens uit meerdere onafhankelijke dierexperimenten te beoordelen en te combineren, onderzochten zij hoe goed deze circRNA–nanodeeltje-vaccins tumoren verkleinen, infecties onder controle houden en bijwerkingen zoals gewichtsverlies of ernstige toxiciteit vermijden.
Krachtigere immuunsoldaten, kleinere tumoren
De gecombineerde diergegevens schetsen een opvallend beeld. In tien tumorstudies hadden muizen die circRNA-vaccins kregen veel kleinere tumoren dan controledieren, ongeacht of de injectie in de spier, onder de huid of in de bloedbaan werd gegeven. Tegelijk bleef het lichaamsgewicht — een ruwe maat voor de algehele gezondheid — stabiel, wat suggereert dat de behandeling niet algemeen toxisch was. Gedetailleerde immuunmetingen lieten zien dat belangrijke witte bloedcellen actiever werden: cytotoxische T‑cellen die abnormale cellen direct doden namen toe, macrofagen stegen en dendritische cellen — de wachters die fragmenten van indringers aan de rest van het immuunsysteem tonen — werden duidelijk versterkt. Deze veranderingen geven aan dat de vaccins tumoren niet alleen mechanisch aanvallen; ze herprogrammeren het immuunsysteem om kankercellen efficiënter te herkennen en te vernietigen. 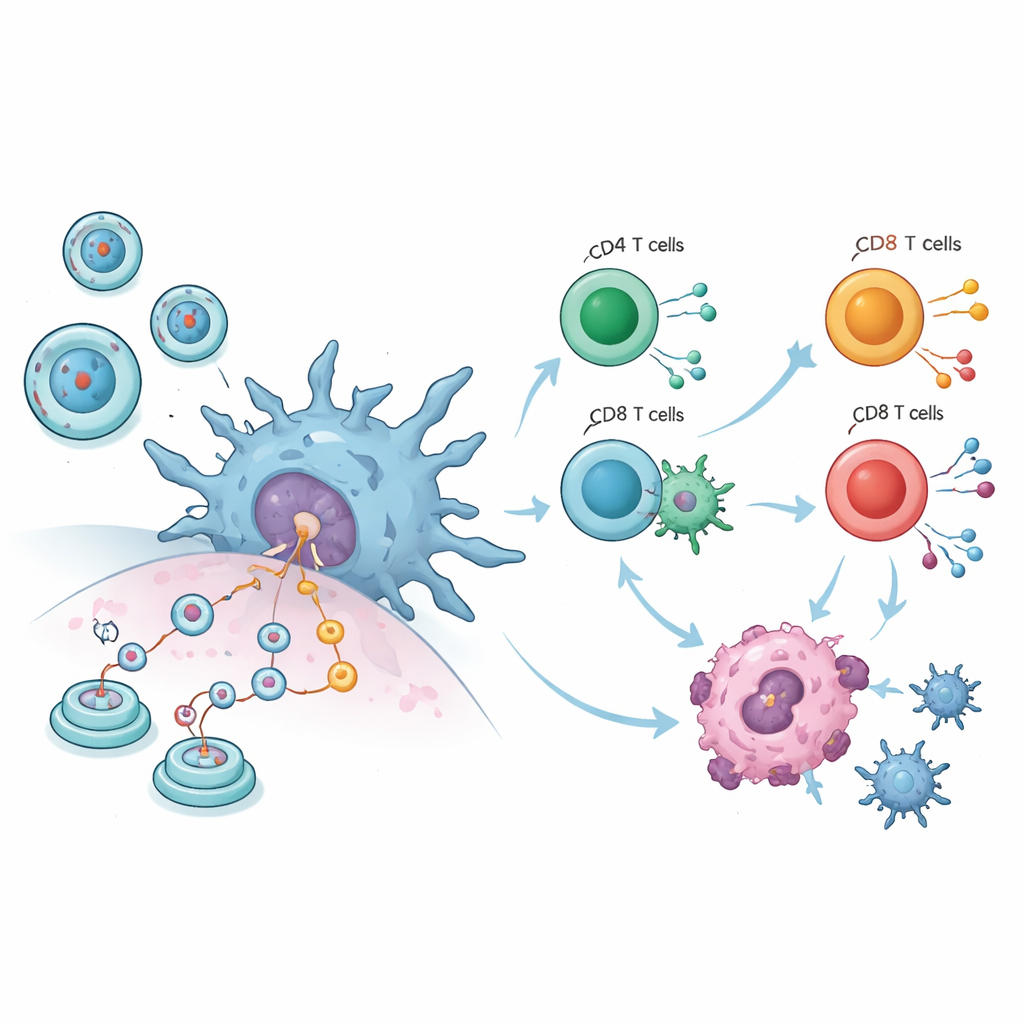
Virussen bestrijden met hetzelfde instrument
Dezelfde circRNA-technologie bleek ook krachtig in modellen van infectieziekten, waaronder influenza, Zika, SARS‑CoV‑2 en andere virussen. Bij gevaccineerde muizen stegen de antistoffenniveaus in het bloed sterk, daalden de virusbelastingen in de longen en namen signaleringsmoleculen zoals interferon‑gamma en interleukine‑4 toe, wat aantoont dat zowel de snelle als de meer langdurige armen van het immuunsysteem werden geactiveerd. Intranasale toediening, die gericht is op het slijmvlies van de luchtwegen, gaf vaak bijzonder sterke lokale bescherming, terwijl andere routes bredere responsen door het hele lichaam bevorderden. Over het geheel genomen suggereert de analyse dat één circRNA-platform, afgestemd op verschillende doelwitten, kan worden aangepast om te beschermen tegen een breed scala aan pathogenen evenals tegen kankers.
Het mechanisme controleren in menselijke cellen
Om verder te gaan dan dierlijke gegevens, voerden de auteurs laboratoriumexperimenten uit met menselijke, uit bloed afgeleide immuuncellen. Ze produceerden gezuiverd circRNA dat codeerde voor een testeiwit en verwijderden dubbelstrengig RNA‑verontreinigingen die nonspecifieke alarmsignalen zouden kunnen activeren. Toen dendritische cellen werden blootgesteld aan lipide-omhulde circRNA, begonnen ze het nieuwe eiwit te maken, zetten ze belangrijke oppervlaktemarkers van rijping aan en gaven ze inflammatoire boodschappers zoals IL‑6, IL‑1β en TNF‑α vrij. Wanneer deze geactiveerde dendritische cellen werden gemengd met menselijke T‑cellen, schakelden zowel helper- als killer T‑cellen aan en secreten ze interferon‑gamma, en verschenen er meer antigeenspecifieke T‑cellen in een test die individuele reagerende cellen telt. Deze bevindingen bevestigen dat circRNA menselijke immuuncellen nauwkeurig kan aansturen, niet alleen die van muizen.
Belofte, kanttekeningen en wat volgt
Voor niet‑specialisten is de kernboodschap dat circulaire RNA‑vaccins, gedragen door lipide-nanodeeltjes, lijken op een robuustere, langduriger werkende verwant van de huidige RNA-prikken. Bij muizen verkleinen ze tumoren, beperken ze virusinfecties en doen ze dat zonder duidelijke schade, terwijl ze in menselijke cellen de immuuncomponenten wekken die nodig zijn voor gerichte afweer. Al deze bewijsvoering is echter nog preklinisch, en verschillende dierlijke stammen, ziektetypes en injectieroutes gaven variabele resultaten. Grote, zorgvuldig ontworpen humane onderzoeken zullen nodig zijn om te onderzoeken hoe goed deze aanpak bij mensen werkt en om dosering en toediening te optimaliseren. Als die hobbels worden genomen, zou circRNA‑vaccins een veelzijdig nieuw instrument kunnen worden voor de behandeling van kanker en het voorkomen van toekomstige uitbraken van infectieziekten.
Bronvermelding: Yang, R., Jia, L. & Cui, J. Lipid nanoparticle delivery of circle RNA vaccine induces potent immune responses. Sci Rep 16, 13268 (2026). https://doi.org/10.1038/s41598-026-46871-6
Trefwoorden: circulaire RNA-vaccins, lipide-nanodeeltjes, kankerimmunotherapie, vaccins tegen infectieziekten, T-celactivatie