Clear Sky Science · zh
ROS-NLRP3参与包虫原头节囊液外泌-分泌物对肝细胞焦亡反应的作用
为什么这种微小寄生虫对肝脏健康很重要
囊性包虫病由一种体型较小的绦虫引起,该虫通常寄生于绵羊、犬等动物,但也可偶发感染人类。寄生虫在体内形成充液囊肿,最常见于肝脏,囊肿可在多年内静静生长,随后引起疼痛、消化不良或严重并发症。临床上已知感染会损伤肝细胞,但寄生虫存在如何具体导致细胞死亡的机制尚不清楚。本研究聚焦于一种“火性”细胞死亡形式,探讨由活性氧分子与细胞内报警系统驱动的过程,以理解寄生虫分泌物如何直接损伤肝细胞。
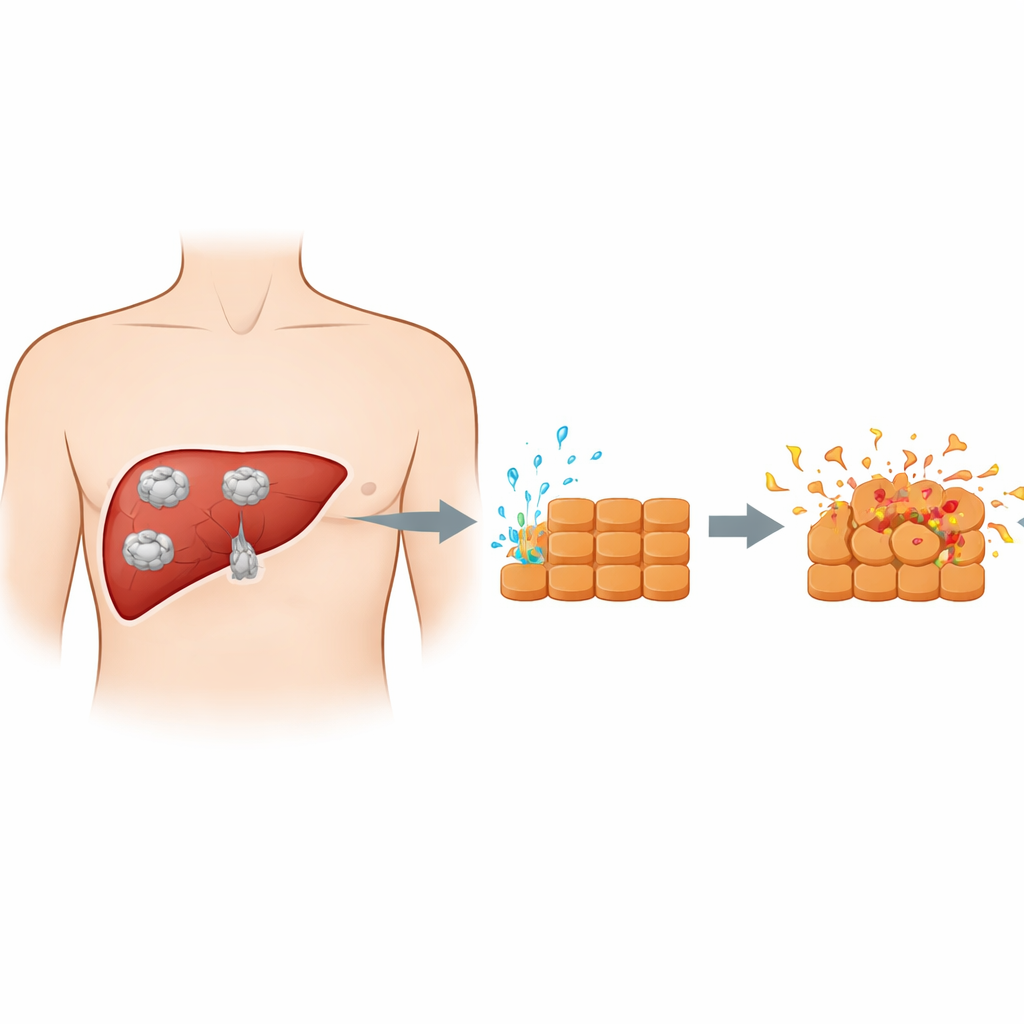
寄生虫与肝细胞如何相遇
人体吞入寄生虫虫卵后,幼虫由肠道迁移至肝脏并发育为囊肿。这些囊肿并非被动的空泡;随着寄生虫生长,它会持续向周围组织释放由蛋白质及其他物质组成的混合物。早期研究常使用整个囊肿液,其中混杂大量宿主来源成分,难以分辨寄生虫本身的作用。本研究改用从早期寄生虫阶段——原头节——纯化获得的外泌-分泌产物,随后将其作用于体外培养的小鼠肝细胞,构建了一个更干净的模型以模拟寄生虫扩张囊肿时与肝细胞之间的直接化学“对话”。
肝内的一种“火焰式”细胞死亡
团队关注的是焦亡(pyroptosis),这是一种不同于正常细胞有序死亡的程序性细胞死亡形式。发生焦亡时,细胞肿胀、膜形成穿孔并破裂,释放出促炎分子,招募免疫细胞并加剧组织损伤。该过程由称为炎症小体的分子装置控制,尤其是以传感蛋白NLRP3为核心的类型。当研究者用寄生虫分泌物处理肝细胞时,观察到了典型的预警信号:细胞存活率下降、提示膜损伤的乳酸脱氢酶(LDH)渗漏增加、显微镜下死亡细胞增多,以及促进膜孔形成和炎性因子释放的关键焦亡相关蛋白水平升高。
关闭危险报警
为验证该破坏性反应是否确实依赖于NLRP3报警系统,研究者使用了一种小分子抑制剂MCC950,该物质可特异性阻断NLRP3活性。预先用该抑制剂处理的肝细胞在暴露于寄生虫分泌物时表现出更强的抵抗力:细胞存活更好、膜受损细胞更少、LDH渗漏降低、与焦亡相关的炎性蛋白产生减少。在荧光成像下,细胞内可见的NLRP3显著减少。综合这些结果表明,寄生虫分泌物并非以非特异性毒性直接杀死肝细胞,而是主动触发了细胞自身基于NLRP3的自毁与炎症机制。
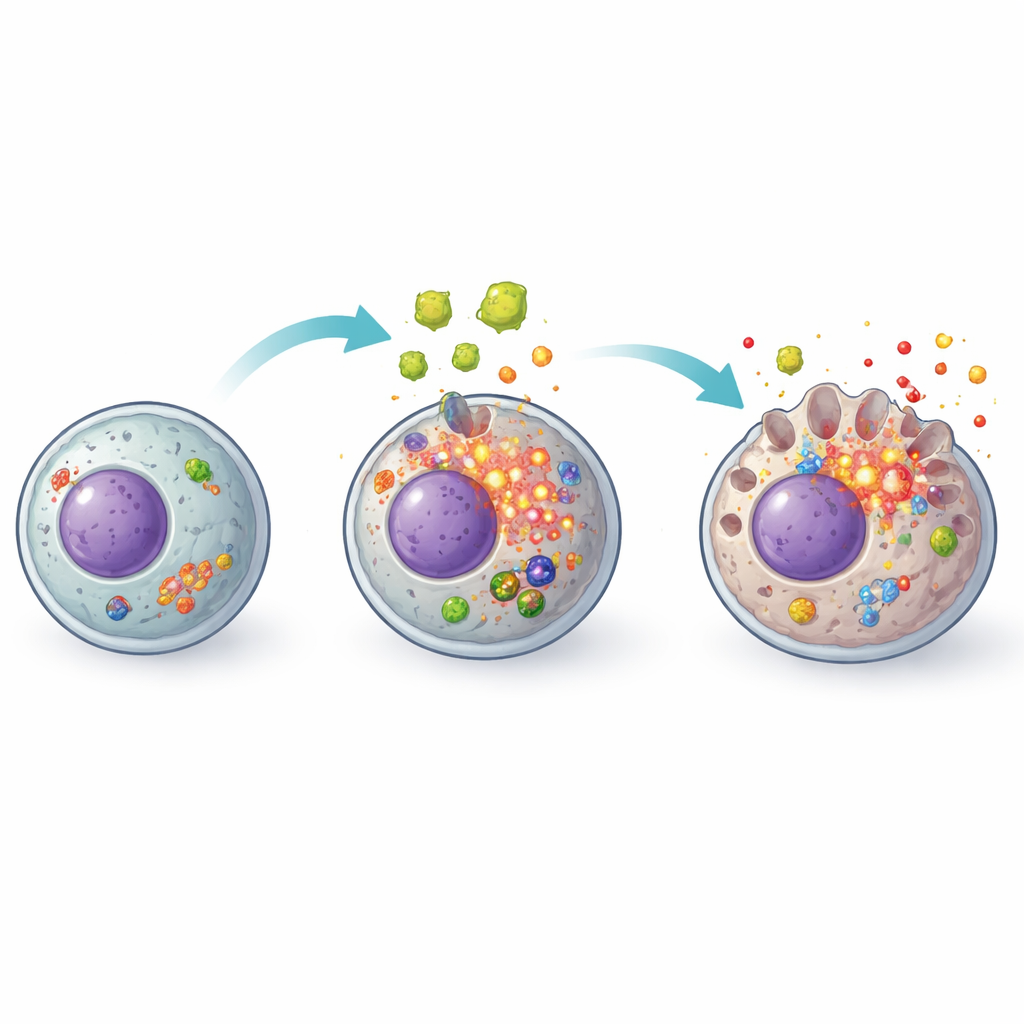
起火点:细胞内的氧化应激
研究接着探究是什么点燃了这一报警系统。一个主要的嫌疑者是活性氧(ROS),即代谢过程中产生的化学活性副产物,当其积累时会变得有害。寄生虫分泌物使肝细胞积累大量这类活性分子,同时削弱其抗氧化防御。当研究者加入临床上用于保护肝脏的广泛抗氧化剂——乙酰半胱氨酸(N-acetylcysteine)时,情况发生了改变:活性氧水平下降、抗氧化标志物恢复、NLRP3复合体及其下游焦亡机制的激活被强烈抑制。细胞存活改善,释放的炎性分子减少,表明氧化应激是这一连锁反应的关键上游触发因素。
对高风险人群的意义
综合来看,研究描绘了一条清晰的脉络:包虫(Echinococcus granulosus)在肝囊周围分泌的蛋白质可使邻近肝细胞累积过量活性氧,进而激活NLRP3炎症小体并诱导一种爆发性、促炎性的细胞死亡形式。这一机制有助解释看似沉寂的寄生囊肿如何逐步侵蚀肝组织并维持慢性炎症。对患者而言,该研究提示了除手术和常规抗寄生虫药之外的潜在治疗方向:降低氧化应激或特异性阻断NLRP3炎症小体的策略,未来或可用于保护肝细胞、延缓疾病进展并降低囊性包虫病并发症的风险。
引用: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
关键词: 囊性包虫病, 肝脏炎症, 焦亡, 活性氧, NLRP3炎症小体