Clear Sky Science · tr
ROS-NLRP3, Echinococcus granulosus protoskolekslerinin ekskretuar-sekretuar ürünlerinin hepatositlerdeki piroptoz tepkisine katılıyor
Neden küçük bir parazit karaciğer sağlığı için önemlidir
Kistik ekinokokkoz, genellikle koyun ve köpek gibi hayvanlarda yaşayan, ancak kazara insanları da enfekte edebilen küçük bir tenyadan kaynaklanan bir hastalıktır. Parazit genellikle karaciğerde sıvı dolu kistler oluşturur; bu kistler yıllarca sessizce büyüyebilir ve sonra ağrı, sindirim sorunları veya ciddi komplikasyonlara neden olabilir. Doktorlar bu enfeksiyon sırasında karaciğer hücrelerinin zarar gördüğünü biliyor, ancak parazitin varlığının nasıl hücre ölümüyle sonuçlandığı tam olarak net değildi. Bu çalışma, reaktif oksijen türleri ve hücresel bir alarm sistemi olarak işlev gören bir mekanizma tarafından yönlendirilen belirli bir tür şiddetli hücre ölümünü yakından inceleyerek parazit salgılarının karaciğer hücrelerine doğrudan nasıl zarar verebileceğini anlamayı amaçlıyor.
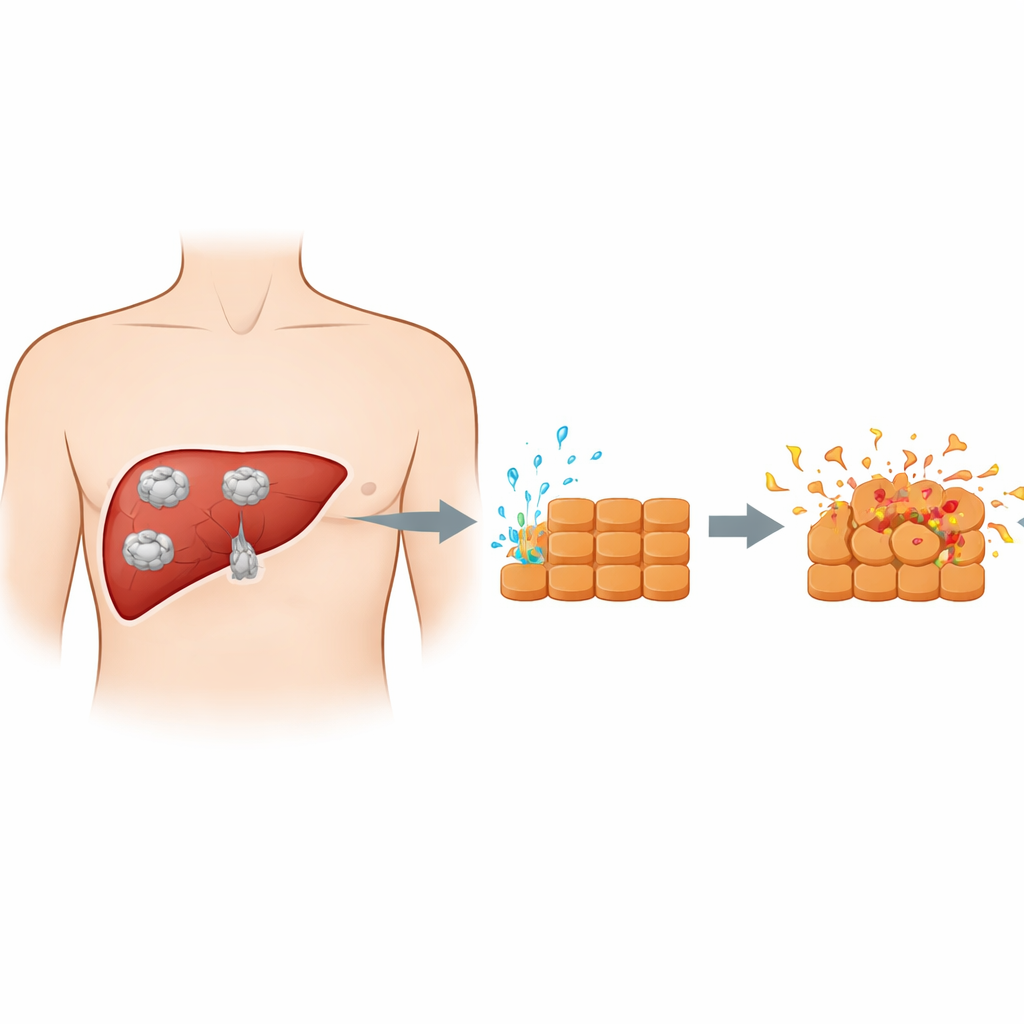
Parazit ile karaciğer hücrelerinin karşılaşması nasıl olur
İnsanlar parazit yumurtalarını yuttuğunda, genç formlar bağırsaktan karaciğere geçer ve kistlere dönüşür. Bu kistler sadece pasif kabarcıklar değildir; büyüyen parazit çevre dokuya sürekli olarak proteinler ve diğer maddelerden oluşan bir karışım salar. Önceki çalışmalarda genellikle tüm kist sıvısı kullanıldı; oysa bu sıvı birçok konağa ait bileşen içerir ve parazitin kendisinin ne yaptığı görmek zorlaşır. Bu çalışmada araştırmacılar bunun yerine protoskoleks adı verilen erken parazit evresinden saflaştırılmış salgıları topladılar. Ardından laboratuvarda yetiştirilen fare karaciğer hücrelerini bu ekskretuvar–sekretuvar ürünlere maruz bırakarak kist genişlerken parazit ile karaciğer hücreleri arasındaki doğrudan kimyasal iletişimin daha temiz bir modelini oluşturdular.
Karaciğer içinde alevli bir hücre ölümü türü
Araştırma ekibi, normal hücre yenilenmesinde görülen sessiz, düzenli kapanıştan farklı olan programlı bir hücre ölümü türü olan piroptoz üzerine odaklandı. Piroptozda hücreler şişer, zarları delinmeye başlar ve hücreler patlayarak bağışıklık hücrelerini çeken ve doku hasarını artıran iltihabi moleküller salar. Bu süreç inflammazom olarak bilinen moleküler bir makine tarafından kontrol edilir; özellikle NLRP3 adı verilen bir sensör proteini etrafında kurulan bir versiyonu önemlidir. Araştırmacılar karaciğer hücrelerini parazit salgılarıyla muamele ettiğinde klasik uyarı işaretleri görüldü: azalmış hücre canlılığı, zar hasarını gösteren bir hücre enziminde (LDH) artış, mikroskop altında daha fazla ölü hücre ve zar gözenek oluşumunu ve iltihabi haberci salınımını yönlendiren piroptozla ilişkili anahtar proteinlerin artmış düzeyleri.
Tehlike alarmını kapatmak
Bu yıkıcı yanıtın gerçekten NLRP3 alarm sistemine bağlı olup olmadığını test etmek için araştırmacılar NLRP3 aktivitesini özgül olarak engelleyen MCC950 adlı küçük bir molekül kullandılar. Bu engelleyiciyle ön işlem uygulanan karaciğer hücreleri parazit salgılarına maruz kaldığında çok daha dirençliydi. Daha iyi hayatta kalma, daha az zar hasarlı hücre, daha düşük LDH sızıntısı ve piroptoza bağlı iltihaplı protein üretiminde azalma gözlendi. Floresan görüntülemede hücre içinde görülen NLRP3 miktarı keskin şekilde düştü. Bu bulgular birlikte, parazitin salgılarının karaciğer hücrelerini rastgele zehirlemediğini; bunun yerine hücrelerin kendi NLRP3 tabanlı kendini yok etme ve iltihap mekanizmasını aktif olarak tetiklediğini gösteriyor.
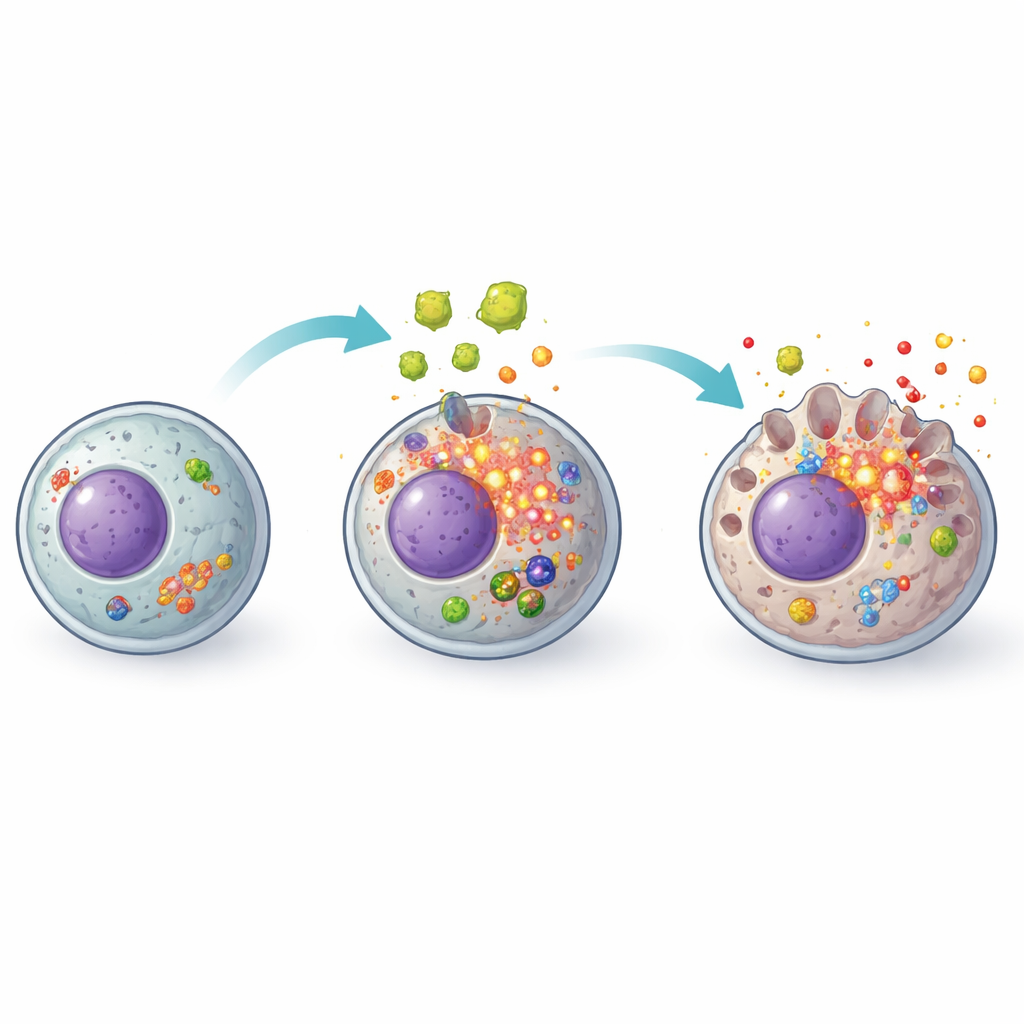
Kıvılcım: hücre içindeki oksidatif stres
Çalışma daha sonra bu alarm sisteminin fitilini neyin ateşlediğini sordu. Baş şüpheli, normal metabolizmanın kimyasal olarak reaktif yan ürünleri olan ve biriktiğinde zararlı hale gelen reaktif oksijen türleriydi. Parazit salgıları, karaciğer hücrelerinde bu reaktif moleküllerin yüksek düzeyde birikmesine ve antioksidan savunmaların zayıflamasına neden oldu. Araştırmacılar klinikte karaciğeri korumak için kullanılan iyi bilinen bir antioksidan olan N-asetilsistein eklediklerinde tablo değişti. Reaktif oksijen düzeyleri düştü, antioksidan göstergeler toparlandı ve NLRP3 kompleksinin ve onun aşağı akış piroptoz mekanizmasının aktivasyonu büyük ölçüde baskılandı. Hücre canlılığı iyileşti ve daha az iltihabi molekül salındı; bu da oksidatif stresin bu zincir reaksiyon için kritik bir yukarı akış tetikleyicisi olduğunu düşündürüyor.
Risk altındaki insanlar için bunun anlamı
Birlikte ele alındığında bulgular açık bir hikâye ortaya koyuyor: Echinococcus granulosus’un karaciğer kistleri etrafına salgıladığı proteinler yakındaki karaciğer hücrelerini reaktif oksijen türleriyle aşırı yükleyebiliyor; bu da NLRP3 inflammazomunu aktive ederek patlayıcı, iltihabi bir hücre ölümü türünü tetikliyor. Bu mekanizma, görünüşte sessiz bir parazitik kistin nasıl yavaş yavaş karaciğer dokusunu aşındırdığını ve kronik iltihabı körüklediğini açıklamaya yardımcı oluyor. Hastalar için çalışma, cerrahi ve standart antiparazitik ilaçların ötesinde yeni potansiyel tedavi yaklaşımlarına işaret ediyor. Oksidatif stresi azaltan veya özellikle NLRP3 inflammazomunu bloke eden yaklaşımlar bir gün karaciğer hücrelerini korumaya, hastalık ilerlemesini yavaşlatmaya ve kistik ekinokokkozda komplikasyon riskini azaltmaya yardımcı olabilir.
Atıf: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Anahtar kelimeler: kistik ekinokokkoz, karaciğer iltihabı, piroptoz, reaktif oksijen türleri, NLRP3 inflammazom