Clear Sky Science · pl
ROS-NLRP3 uczestniczy w odpowiedzi piroptotycznej na produkty wydalniczo‑wydzielnicze protoskoleksów Echinococcus granulosus w hepatocytach
Dlaczego mały pasożyt ma znaczenie dla zdrowia wątroby
Wodniak bąblowcowy to choroba wywoływana przez małego tasiemca, który zwykle żyje u zwierząt, takich jak owce i psy, ale może przypadkowo zakażać ludzi. Pasożyt tworzy wypełnione płynem torbiele, najczęściej w wątrobie, które przez lata mogą rosnąć bezobjawowo, zanim wywołają ból, problemy trawienne lub poważne powikłania. Lekarze wiedzą, że komórki wątroby są uszkadzane w przebiegu tej infekcji, ale nie było jasne, w jaki sposób obecność pasożyta prowadzi do śmierci komórek. W tym badaniu badacze przyjrzeli się z bliska określonemu, „ognistemu” rodzajowi śmierci komórkowej, napędzanemu przez cząsteczki zwane reaktywnymi formami tlenu oraz wewnętrzny system alarmowy, aby zrozumieć, jak wydzieliny pasożyta mogą bezpośrednio uszkadzać hepatocyty.
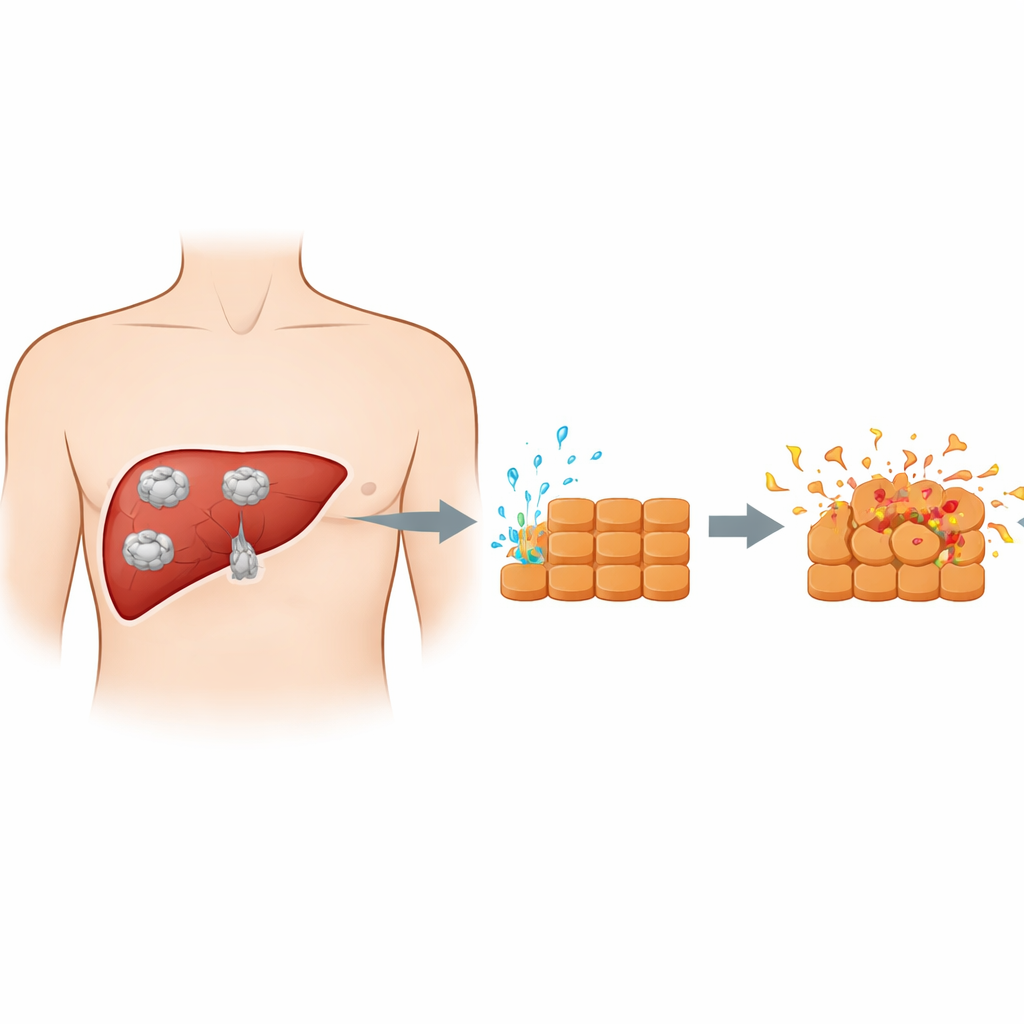
Gdzie spotyka się pasożyt z komórkami wątroby
Gdy ludzie połykają jaja pasożyta, młode formy przemieszczają się z jelita do wątroby i rozwijają się w torbiele. Te torbiele to nie tylko bierne pęcherze; rozwijający się pasożyt nieustannie uwalnia mieszaninę białek i innych substancji do otaczającej tkanki. Wcześniejsze badania często wykorzystywały całe płyny torbielowe, które zawierają także wiele składników pochodzenia gospodarza, co utrudniało rozróżnienie, co robi sam pasożyt. W tym badaniu badacze zamiast tego zebrali oczyszczone wydzieliny z wczesnego stadium pasożyta, zwanego protoskoleksem. Następnie wystawili hodowane in vitro mysie komórki wątroby na te produkty wydalniczo‑wydzielnicze, tworząc czystszy model bezpośredniej chemicznej „rozmowy” między pasożytem a komórkami wątroby w miarę rozwoju torbieli.
„Ognisty” rodzaj śmierci komórki w wątrobie
Zespół skupił się na piroptozie, formie zaprogramowanej śmierci komórkowej, która różni się od cichego, uporządkowanego wygaszania obserwowanego przy normalnej wymianie komórek. W piroptozie komórki pęcznieją, ich błony ulegają perforacji i pękają, uwalniając zapalne cząsteczki, które przyciągają komórki układu odpornościowego i nasilają uszkodzenie tkanki. Proces ten jest kontrolowany przez maszynerię molekularną znaną jako inflamazom, w szczególności wariant zbudowany wokół białka sensorycznego NLRP3. Gdy badacze traktowali komórki wątroby wydzielinami pasożyta, zaobserwowali klasyczne objawy ostrzegawcze: zmniejszoną przeżywalność komórek, zwiększone uwalnianie enzymu komórkowego (LDH) świadczące o uszkodzeniu błony, więcej martwych komórek w mikroskopie oraz wyższe poziomy kluczowych białek związanych z piroptozą, które napędzają tworzenie porów w błonie i uwalnianie zapalnych mediatorów.
Wyłączenie alarmu niebezpieczeństwa
Aby sprawdzić, czy ta destrukcyjna odpowiedź rzeczywiście zależy od systemu alarmowego NLRP3, badacze użyli małocząsteczkowego inhibitora MCC950, który specyficznie blokuje aktywność NLRP3. Komórki wątroby wstępnie traktowane tym inhibitorem były znacznie bardziej odporne po wystawieniu na wydzieliny pasożyta. Wykazywały lepszą przeżywalność, mniej uszkodzonych błon komórkowych, niższe uwalnianie LDH i zmniejszoną produkcję białek zapalnych związanych z piroptozą. W obrazowaniu fluorescencyjnym ilość widocznego NLRP3 wewnątrz komórek gwałtownie spadła. Razem te wyniki wskazują, że wydzieliny pasożyta nie zatruwają hepatocytów w sposób niespecyficzny; zamiast tego aktywnie uruchamiają w komórkach mechanizm autodestrukcji i zapalenia oparty na NLRP3.
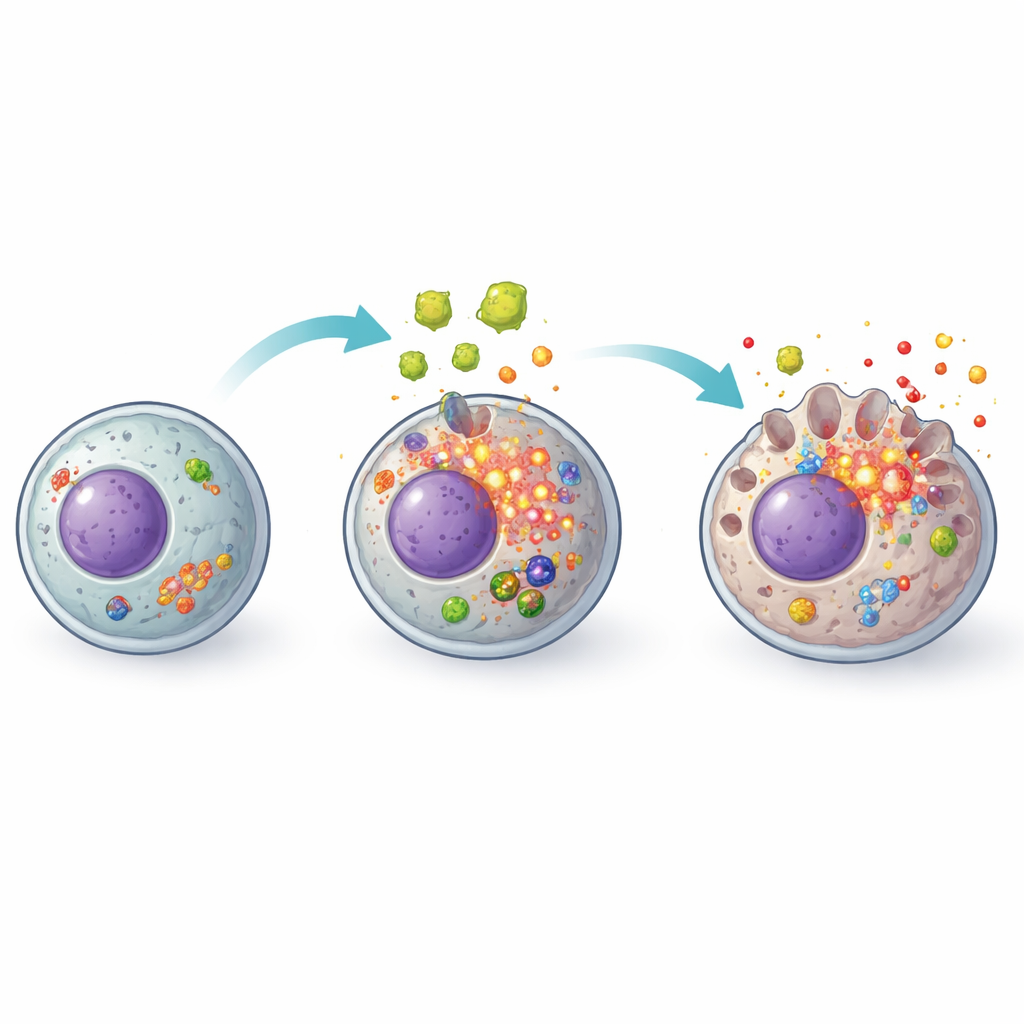
Iskra: stres oksydacyjny wewnątrz komórki
W dalszej części badania pytano, co zapala lont tego systemu alarmowego. Głównym podejrzanym były reaktywne formy tlenu, chemicznie reaktywne produkty uboczne normalnego metabolizmu, które stają się szkodliwe, gdy się kumulują. Wydzieliny pasożyta spowodowały, że komórki wątroby gromadziły wysokie poziomy tych reaktywnych cząsteczek, jednocześnie osłabiając ich mechanizmy antyoksydacyjne. Gdy badacze dodali N‑acetylocysteinę, dobrze znany antyoksydant stosowany klinicznie do ochrony wątroby w innych sytuacjach, obserwacje uległy zmianie. Poziomy reaktywnych form tlenu spadły, markery antyoksydacyjne się poprawiły, a aktywacja kompleksu NLRP3 i jego dalszych elementów piroptotycznych została silnie stłumiona. Przeżywalność komórek wzrosła, a uwalnianie mediatorów zapalnych zmniejszyło się, co sugeruje, że stres oksydacyjny jest kluczowym wyzwalaczem tej kaskady.
Co to oznacza dla osób zagrożonych
Podsumowując, wyniki ukazują przejrzystą narrację: białka wydzielane przez Echinococcus granulosus wokół torbieli wątroby mogą przeciążyć pobliskie komórki wątroby reaktywnymi formami tlenu, które z kolei aktywują inflamazom NLRP3 i wywołują wybuchową, zapalną postać śmierci komórkowej. Ten mechanizm pomaga wyjaśnić, jak pozornie cicha torbiel pasożytnicza stopniowo niszczy tkankę wątroby i podtrzymuje przewlekłe zapalenie. Dla pacjentów praca wskazuje nowe potencjalne strategie leczenia wykraczające poza chirurgię i standardowe leki przeciwpasożytnicze. Podejścia zmniejszające stres oksydacyjny lub specyficznie blokujące inflamazom NLRP3 mogą pewnego dnia pomóc chronić hepatocyty, spowalniać postęp choroby i zmniejszać ryzyko powikłań w wodniaku bąblowcowym.
Cytowanie: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Słowa kluczowe: wodniak bąblowcowy, zapalenie wątroby, piroptoza, reaktywne formy tlenu, inflamazom NLRP3