Clear Sky Science · sv
ROS-NLRP3 deltar i pyroptos-responsen mot utsöndringsprodukter från protoskolexer av Echinococcus granulosus i hepatocyter
Varför en liten parasit spelar roll för leverhälsan
Cystisk echinokockinfektion är en sjukdom orsakad av en liten bandmask som vanligtvis lever i djur som får och hundar men som av misstag kan infektera människor. Parasiten bildar vätskefyllda cystor, oftast i levern, som tyst kan växa i åratal innan de orsakar smärta, matsmältningsproblem eller allvarliga komplikationer. Läkare vet att leverceller skadas under denna infektion, men det har varit oklart exakt hur parasitens närvaro leder till celldöd. Denna studie undersöker noggrant en särskild, explosiv form av celldöd, styrd av molekyler kallade reaktiva syreradikaler och ett internt larmssystem, för att förstå hur parasitutskiljningar kan skada leverceller direkt.
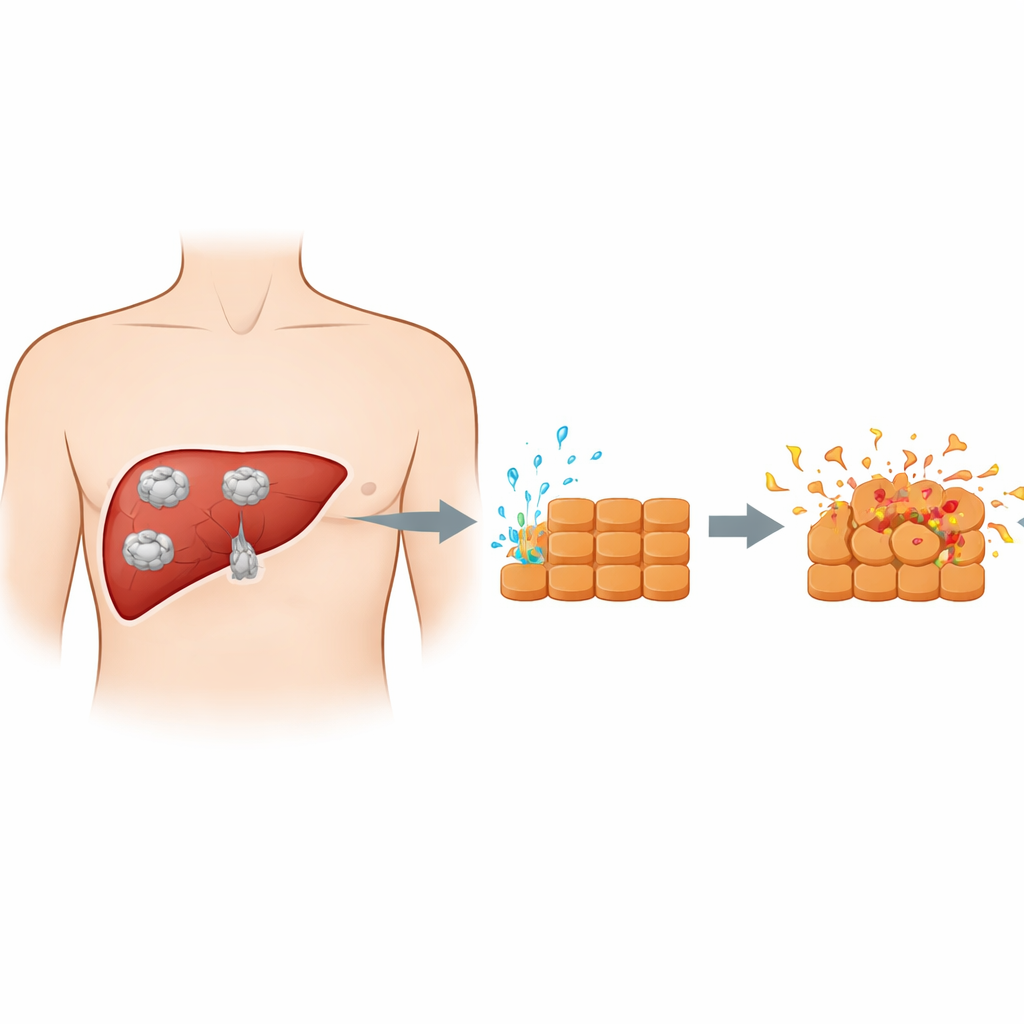
Hur parasiten och levercellerna möts
När människor sväljer parasitägg, färdas de unga formerna från tarmen till levern och utvecklas till cystor. Dessa cystor är inte bara passiva bubblor; den växande parasiten frisätter ständigt en blandning av proteiner och andra ämnen i omgivande vävnad. Tidigare arbete använde ofta hela cystvätskan, som också innehåller många värd‑härledda komponenter, vilket försvårade tolkningen av vad parasiten själv gör. I denna studie samlade forskarna istället renade utsöndringar från ett tidigt parasitstadium kallat protoskolexer. De exponerade därefter odlade musleverceller i labbet för dessa exkretions–sekretionsprodukter och skapade därmed en renare modell för den direkta kemiska dialogen mellan parasit och leverceller i takt med att egy cysta växer.
En explosiv form av celldöd i levern
Gruppen fokuserade på pyroptos, en form av programmerad celldöd som skiljer sig från det tysta, prydliga avslutet vid normal cellomsättning. Vid pyroptos sväller cellerna, deras membran får perforationer och de spricker upp och spiller ut inflammatoriska molekyler som rekryterar immunceller och förvärrar vävnadsskadan. Denna process kontrolleras av en molekylär apparat känd som inflammasomet, i synnerhet en variant byggd kring en sensorprotein kallad NLRP3. När forskarna behandlade leverceller med parasitutskiljningar såg de klassiska varningstecken: minskad cellöverlevnad, ökad läckage av enzymet LDH som signalerar membranskada, fler döda celler under mikroskopet och högre nivåer av centrala pyroptosrelaterade proteiner som driver bildandet av membranporer och frisättningen av inflammatoriska budbärarmolekyler.
Att stänga av larmsignalen
För att testa om denna destruktiva respons verkligen berodde på NLRP3‑larmsystemet använde forskarna en liten molekyl kallad MCC950 som specifikt blockerar NLRP3‑aktivitet. Leverceller som förbehandlats med denna blockerare var mycket mer motståndskraftiga när de exponerades för parasitutskiljningarna. De visade bättre överlevnad, färre membranskadade celler, lägre LDH‑läckage och minskad produktion av inflammatoriska proteiner associerade med pyroptos. Vid fluorescensavbildning minskade mängden synligt NLRP3 inne i cellerna kraftigt. Tillsammans tyder dessa resultat på att parasitens sekret inte bara förgiftar leverceller ospecifikt; de utlöser aktivt cellernas eget NLRP3‑baserade självdestruktions‑ och inflammationsmaskineri.
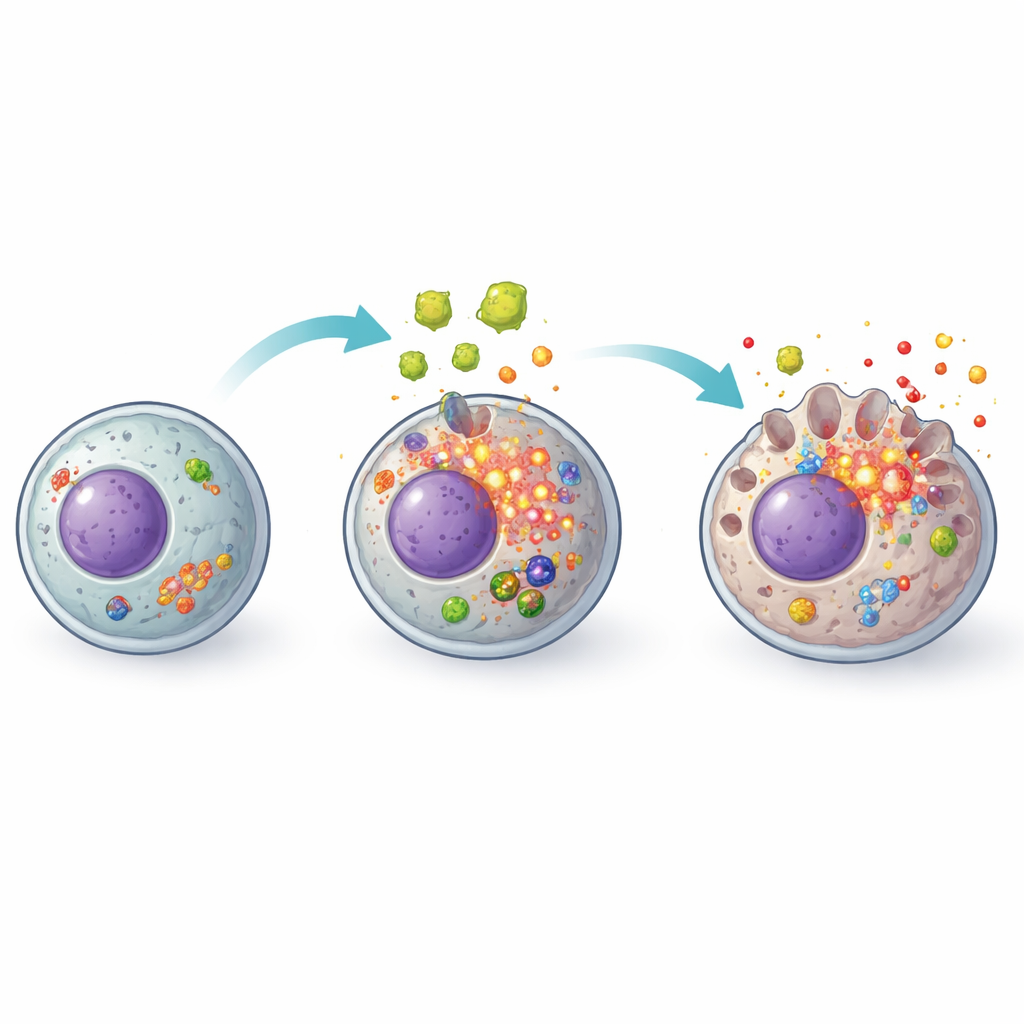
Tändningen: oxidativ stress inne i cellen
Studien undersökte sedan vad som tänder säkringen på detta larmsystem. En huvudmisstänkt var reaktiva syreradikaler, kemiskt reaktiva biprodukter av normal ämnesomsättning som blir skadliga när de ansamlas. Parasitutskiljningarna gjorde att leverceller samlade på sig höga nivåer av dessa reaktiva molekyler samtidigt som deras antioxidantförsvar försvagades. När forskarna tillsatte N‑acetylcystein, en välkänd antioxidant som kliniskt används för att skydda levern i andra sammanhang, förändrades bilden. Halterna av reaktiva syreradikaler sjönk, antioxidantmarkörer återhämtade sig och aktiveringen av NLRP3‑komplexet och dess nedströmspycroptosmaskineri dämpades kraftigt. Cellöverlevnaden förbättrades och färre inflammatoriska molekyler frisattes, vilket tyder på att oxidativ stress är en avgörande uppströms utlösare för denna kedjereaktion.
Vad detta betyder för personer i riskzonen
Sammantaget avslöjar fynden en tydlig berättelse: proteiner som utsöndras av Echinococcus granulosus kring dess levercystor kan överbelasta närliggande leverceller med reaktiva syreradikaler, vilka i sin tur aktiverar NLRP3‑inflammasomet och driver en explosiv, inflammatorisk form av celldöd. Denna mekanism hjälper till att förklara hur en till synes lugn parasitisk cysta gradvis urholkar levervävnad och driver på kronisk inflammation. För patienter pekar arbetet på nya potentiella behandlingsinriktningar utöver kirurgi och standard antiparasitära läkemedel. Strategier som minskar oxidativ stress eller specifikt blockerar NLRP3‑inflammasomet kan en dag bidra till att skydda leverceller, bromsa sjukdomsprogression och sänka risken för komplikationer vid cystisk echinokockinfektion.
Citering: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Nyckelord: cystisk echinokockinfektion, leverinflammation, pyroptos, reaktiva syreradikaler, NLRP3-inflammasom