Clear Sky Science · nl
ROS-NLRP3 draagt bij aan de pyroptotische respons op excretiesekreties van protoskolecen van Echinococcus granulosus in hepatocyten
Waarom een kleine parasiet belangrijk is voor levergezondheid
Cystische echinokokkose is een ziekte veroorzaakt door een kleine lintworm die doorgaans in dieren zoals schapen en honden leeft, maar per ongeluk mensen kan besmetten. De parasiet vormt met vloeistof gevulde cysten, meestal in de lever, die jarenlang stil kunnen groeien voordat ze pijn, spijsverteringsklachten of ernstige complicaties veroorzaken. Artsen weten dat levercellen tijdens deze infectie beschadigd raken, maar het was onduidelijk hoe de aanwezigheid van de parasiet precies leidt tot celdood. Deze studie bekijkt nauwgezet een specifiek, 'vurig' type celdood, aangedreven door moleculen die reactieve zuurstofsoorten heten en een intern waarschuwingssysteem, om te begrijpen hoe parasitaire secreties levercellen rechtstreeks kunnen beschadigen.
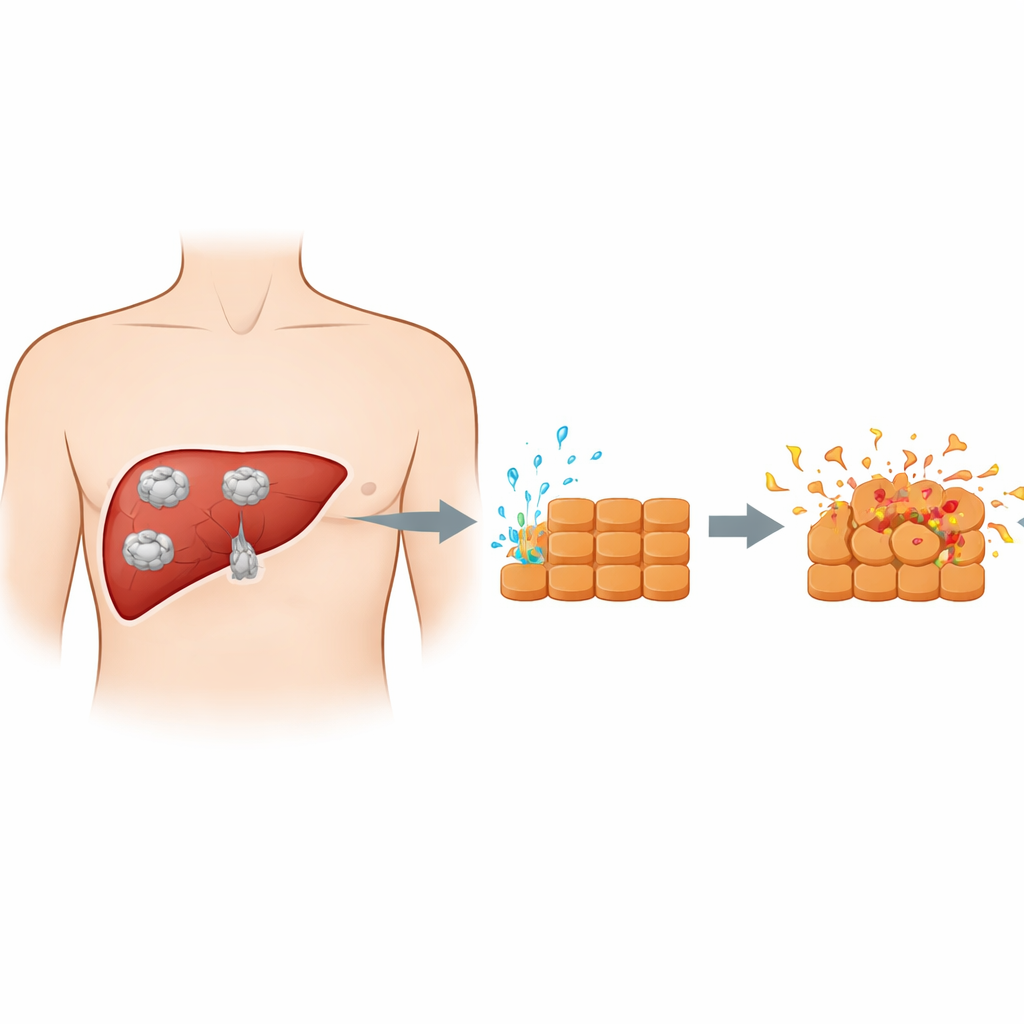
Hoe de parasiet en levercellen elkaar ontmoeten
Wanneer mensen parasitaire eitjes inslikken, reizen de jonge vormen van de darm naar de lever en ontwikkelen zich tot cysten. Die cysten zijn geen passieve blazen; de groeiende parasiet geeft voortdurend een mengsel van eiwitten en andere stoffen af in het omliggende weefsel. Eerder werk gebruikte vaak volledig cystevloeistof, die ook veel gastherkomstige componenten bevat en het moeilijk maakte om te zien wat de parasiet zelf doet. In deze studie verzamelden de onderzoekers in plaats daarvan gezuiverde secreties van een vroeg parasitair stadium, de protoskolecen. Daarna brachten ze muislevercellen die in het laboratorium gekweekt waren in contact met deze excretie–secretieproducten, wat een schoner model creëert van de directe chemische uitwisseling tussen parasiet en levercellen terwijl een cyste groeit.
Een vurige vorm van celdood in de lever
Het team concentreerde zich op pyroptose, een vorm van geprogrammeerde celdood die verschilt van de stille, opgeruimde afbouw die bij normaal celverval voorkomt. Bij pyroptose zwellen cellen op, worden hun membranen doorboord en barsten ze open, waardoor ontstekingsbevorderende moleculen vrijkomen die immuuncellen aantrekken en weefselschade verergeren. Dit proces wordt gecontroleerd door een moleculair stelstel dat het inflammasoom wordt genoemd, in het bijzonder een variant rond een sensor-eiwit dat NLRP3 heet. Wanneer de onderzoekers levercellen behandelden met parasitaire secreties, zagen ze klassieke waarschuwingssignalen: verminderde celoverleving, verhoogde lekkage van het enzym LDH dat membranschade aangeeft, meer dode cellen onder de microscoop, en hogere niveaus van sleutel-eiwitten die betrokken zijn bij pyroptose en die porievorming van membranen en de vrijgave van ontstekingsboodschappers aansturen.
Het uitschakelen van het alarm
Om te testen of deze destructieve respons echt afhankelijk was van het NLRP3-waarschuwingssysteem, gebruikten de onderzoekers een klein molecuul genaamd MCC950 dat specifiek de NLRP3-activiteit blokkeert. Hepatocyten die voorbehandeld waren met deze remmer waren veel veerkrachtiger wanneer ze aan parasitaire secreties werden blootgesteld. Ze vertoonden betere overleving, minder cellen met membraanschade, lagere LDH-lekkage en verminderde productie van ontstekingsbevorderende eiwitten die met pyroptose geassocieerd zijn. Onder fluorescentiemicroscopie daalde de hoeveelheid zichtbare NLRP3 in de cellen sterk. Gezamenlijk wijzen deze resultaten erop dat de secreties van de parasiet levercellen niet simpelweg op een niet-specifieke manier vergiftigen; ze activeren in plaats daarvan actief het NLRP3-gebaseerde zelfdestructie- en ontstekingsmechanisme van de cellen.
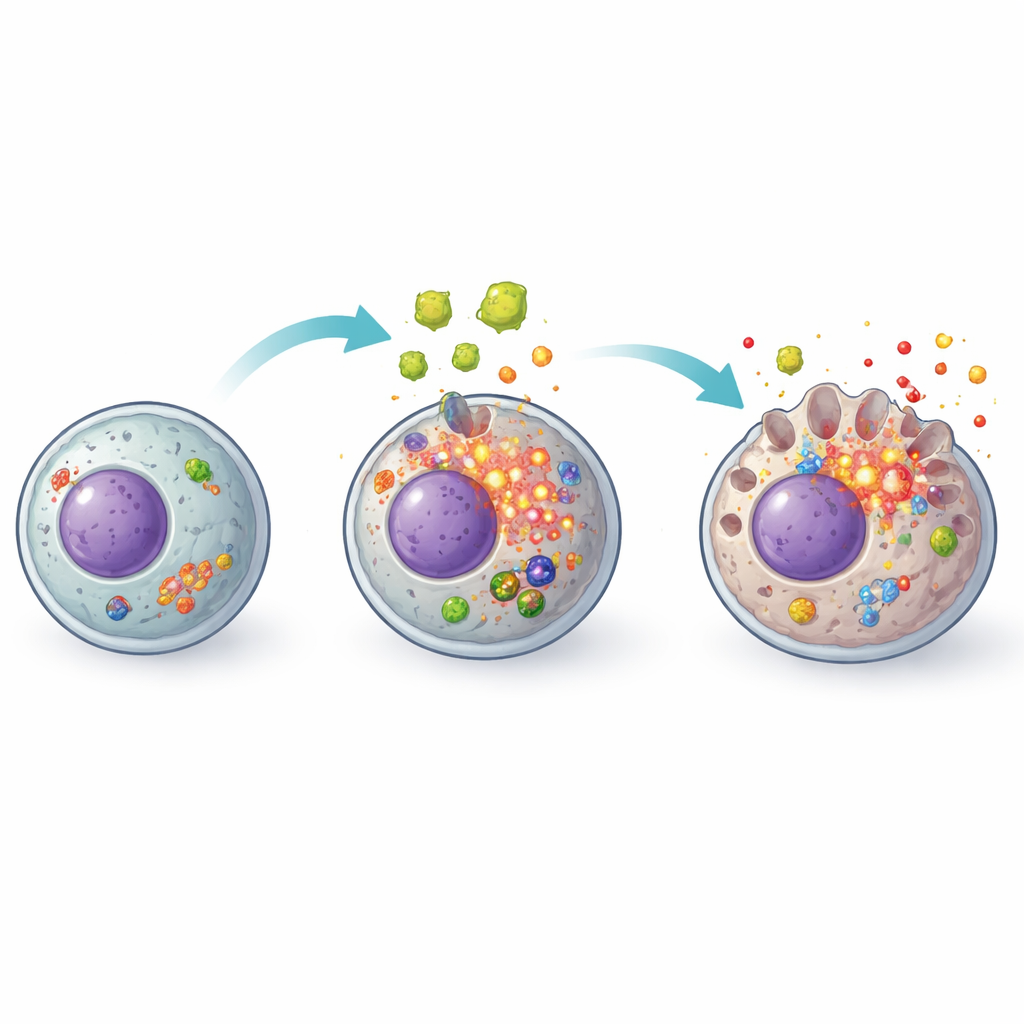
De vonk: oxidatieve stress binnenin de cel
De studie onderzocht vervolgens wat de lont van dit alarmsysteem ontstak. Een voor de hand liggende verdachte waren reactieve zuurstofsoorten, chemisch reactieve bijproducten van normaal metabolisme die schadelijk worden wanneer ze zich ophopen. Parasitaire secreties zorgden ervoor dat levercellen hoge niveaus van deze reactieve moleculen ophoopten terwijl hun antioxidatieve verdediging verzwakte. Toen de onderzoekers N-acetylcysteïne toevoegden, een bekend antioxidant dat klinisch wordt gebruikt om de lever in andere situaties te beschermen, veranderde het beeld. De niveaus van reactieve zuurstof daalden, antioxidatiemarkers herstelden zich, en de activatie van het NLRP3-complex en de daaropvolgende pyroptotische machinerie werd sterk gedempd. De celoverleving verbeterde en minder ontstekingsmoleculen werden vrijgegeven, wat suggereert dat oxidatieve stress een cruciale upstream-trigger is voor deze ketenreactie.
Wat dit betekent voor mensen met risico
Samengevat onthullen de bevindingen een helder verhaal: eiwitten die door Echinococcus granulosus rond zijn levercysten worden uitgescheiden, kunnen nabijgelegen levercellen overloaden met reactieve zuurstofsoorten, die op hun beurt het NLRP3-inflammasoom activeren en een explosieve, ontstekingsrijke vorm van celdood veroorzaken. Dit mechanisme helpt verklaren hoe een ogenschijnlijk stille parasitaire cyste geleidelijk leverweefsel aantast en chronische ontsteking aanwakkert. Voor patiënten wijst dit werk op nieuwe potentiële behandelrichtingen naast chirurgie en standaard antiparasitaire middelen. Benaderingen die oxidatieve stress verminderen of specifiek het NLRP3-inflammasoom blokkeren, zouden mogelijk levercellen kunnen beschermen, de ziekteprogressie vertragen en het risico op complicaties bij cystische echinokokkose kunnen verlagen.
Bronvermelding: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Trefwoorden: cystische echinokokkose, leverontsteking, pyroptose, reactieve zuurstofsoorten, NLRP3-inflammasoom