Clear Sky Science · de
ROS-NLRP3 beteiligt sich an der Pyroptose-Reaktion auf exkretorisch-sekretorische Produkte von Protoskolizes von Echinococcus granulosus in Hepatozyten
Warum ein winziger Parasit für die Lebergesundheit wichtig ist
Die zystische Echinokokkose ist eine von einem kleinen Bandwurm verursachte Erkrankung, die vorwiegend bei Tieren wie Schafen und Hunden vorkommt, aber versehentlich auch Menschen infizieren kann. Der Parasit bildet flüssigkeitsgefüllte Zysten, meist in der Leber, die jahrelang unbemerkt wachsen können, bevor sie Schmerzen, Verdauungsprobleme oder schwere Komplikationen verursachen. Ärztinnen und Ärzte wissen, dass Leberzellen bei dieser Infektion geschädigt werden, aber es war bisher unklar, wie genau die Anwesenheit des Parasiten zum Zelltod führt. Diese Studie untersucht eingehend eine spezielle, „feurige“ Form des Zelltods, die durch reaktive Sauerstoffspezies und ein internes Alarmsystem gesteuert wird, um zu verstehen, wie Parasitensekrete Leberzellen direkt schädigen können.
Wie Parasit und Leberzellen aufeinandertreffen
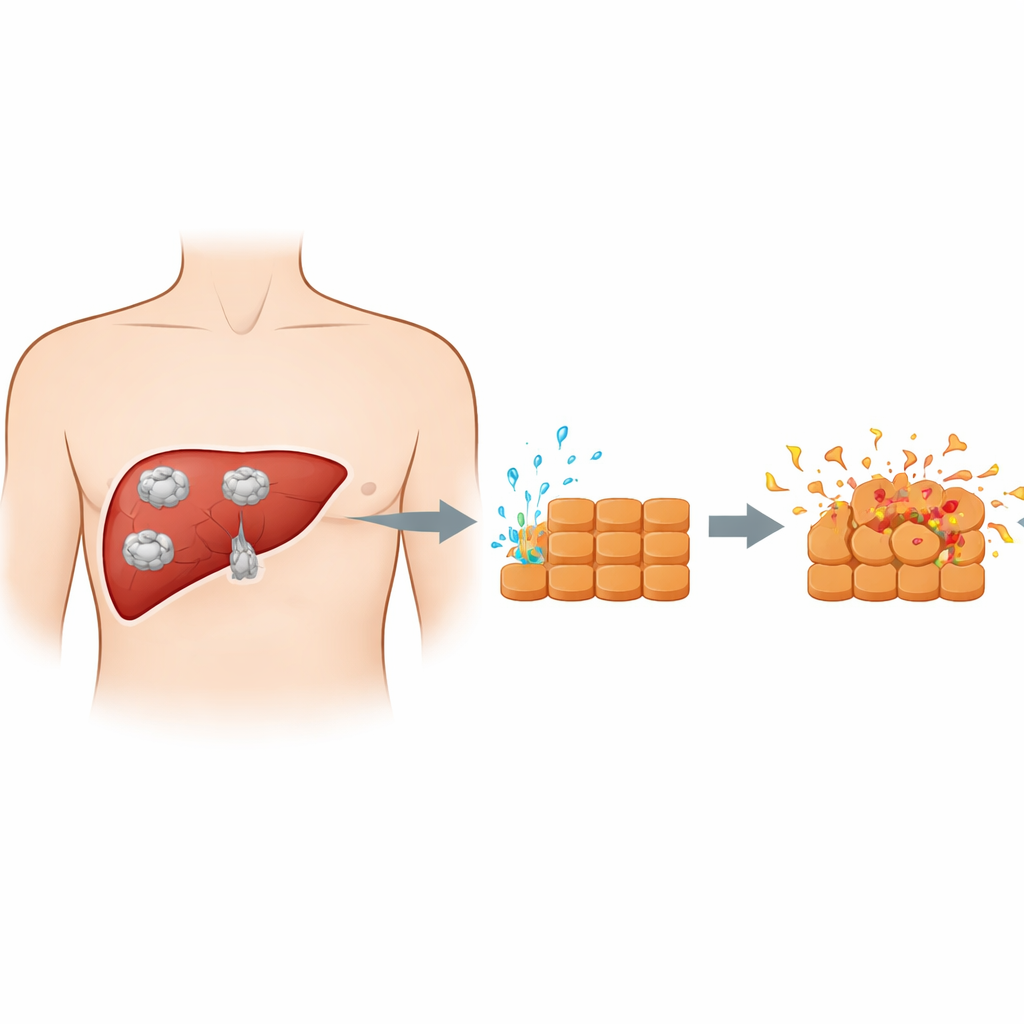
Wenn Menschen Parasiten-Eier verschlucken, wandern die jungen Formen aus dem Darm in die Leber und entwickeln sich dort zu Zysten. Diese Zysten sind nicht bloß passive Hohlräume; der wachsende Parasit gibt kontinuierlich ein Gemisch aus Proteinen und anderen Substanzen in das umgebende Gewebe ab. Frühere Arbeiten verwendeten häufig die gesamte Zystenflüssigkeit, die viele vom Wirt stammende Komponenten enthält, wodurch es schwer war zu unterscheiden, was der Parasit selbst verursacht. In dieser Studie sammelten die Forscher stattdessen gereinigte Sekrete aus einem frühen Parasitenstadium, den Protoskolizes. Diese exkretorisch–sekretorischen Produkte setzten sie dann Kulturen von Maus-Leberzellen im Labor aus, um ein klareres Modell der direkten chemischen Wechselwirkung zwischen Parasit und Leberzellen während des Wachstums einer Zyste zu schaffen.
Eine „feurige“ Form des Zelltods in der Leber
Das Team konzentrierte sich auf die Pyroptose, eine Form des programmierten Zelltods, die sich von dem ruhigen, ordentlichen Abbau bei normalem Zellumsatz unterscheidet. Bei der Pyroptose schwellen Zellen an, ihre Membranen werden durchlöchert und sie platzen auf, wobei sie entzündungsfördernde Moleküle freisetzen, die Immunzellen anlocken und die Gewebeschädigung verstärken. Dieser Prozess wird von einem molekularen Komplex, dem Inflammasom, gesteuert, insbesondere einer Variante, die auf einem Sensorprotein namens NLRP3 basiert. Behandelten die Forscher Leberzellen mit Parasitensekreten, zeigten sich klassische Alarmzeichen: verringerte Zellüberlebensrate, vermehrtes Austreten eines Zellenzym( LDH), das Membranschäden signalisiert, mehr tote Zellen unter dem Mikroskop und erhöhte Mengen an zentralen pyroptosebezogenen Proteinen, die Memporen bilden und die Freisetzung entzündlicher Botenstoffe antreiben.
Den Gefahrenalarm ausschalten
Um zu prüfen, ob diese zerstörerische Reaktion wirklich vom NLRP3-Alarmsystem abhängt, setzten die Forschenden ein kleines Molekül namens MCC950 ein, das die NLRP3-Aktivität spezifisch blockiert. Vorbehandelte Leberzellen mit diesem Hemmer waren gegenüber Parasitensekreten deutlich widerstandsfähiger. Sie zeigten besseres Überleben, weniger membranbeschädigte Zellen, geringeres LDH-Austreten und eine reduzierte Produktion entzündlicher Proteine, die mit Pyroptose verbunden sind. In der Fluoreszenzmikroskopie verringerte sich die sichtbare Menge an NLRP3 in den Zellen deutlich. Zusammengenommen deuten diese Ergebnisse darauf hin, dass die Sekrete des Parasiten Leberzellen nicht unspezifisch vergiften; vielmehr aktivieren sie gezielt die NLRP3-basierte Selbstzerstörungs- und Entzündungsmaschinerie der Zellen.
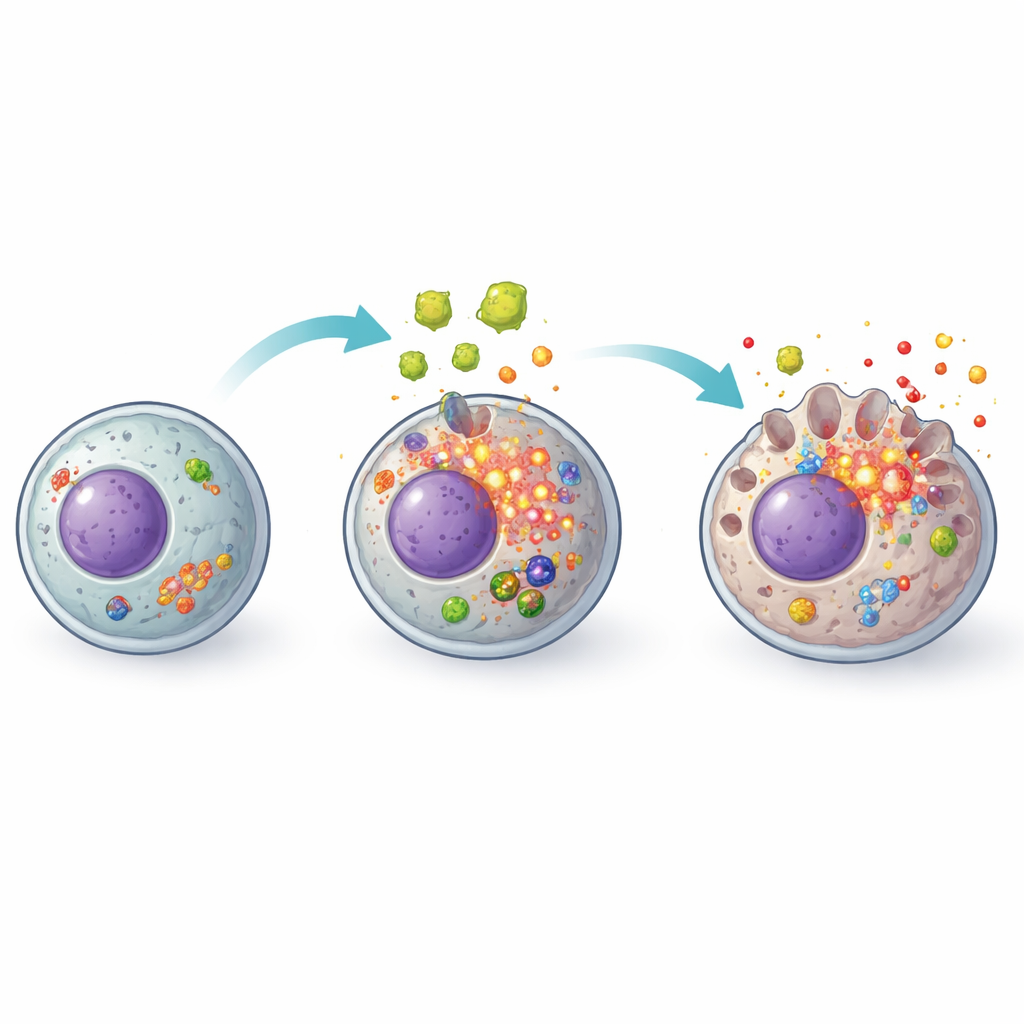
Der Funke: oxidativer Stress in der Zelle
Die Studie fragte weiter, was diesen Alarm auslöst. Ein Hauptverdächtiger waren reaktive Sauerstoffspezies, chemisch reaktive Nebenprodukte des normalen Stoffwechsels, die schädlich werden, wenn sie sich anhäufen. Parasitensekrete führten dazu, dass Leberzellen hohe Mengen dieser reaktiven Moleküle anhäuften und zugleich ihre antioxidativen Abwehrsysteme schwächten. Gaben die Forschenden N-Acetylcystein zu, ein bekanntes Antioxidans, das klinisch zum Schutz der Leber in anderen Kontexten verwendet wird, änderte sich das Bild: Die reaktiven Sauerstofflevel sanken, antioxidative Marker erholten sich, und die Aktivierung des NLRP3-Komplexes sowie dessen nachgeschaltete Pyroptose-Maschinerie wurde stark gedämpft. Das Zellüberleben verbesserte sich und weniger entzündliche Moleküle wurden freigesetzt, was darauf hindeutet, dass oxidativer Stress ein entscheidender früher Auslöser dieser Kaskade ist.
Was das für gefährdete Menschen bedeutet
In der Gesamtschau legen die Ergebnisse eine klare Handlungskette nahe: Von Echinococcus granulosus um seine Leberzysten freigesetzte Proteine können benachbarte Leberzellen mit reaktiven Sauerstoffspezies überlasten, die wiederum das NLRP3-Inflammasom aktivieren und eine explosive, entzündliche Form des Zelltods hervorrufen. Dieser Mechanismus hilft zu erklären, wie eine scheinbar ruhige parasitäre Zyste allmählich Lebergewebe abbaut und chronische Entzündungen antreibt. Für Patientinnen und Patienten weist die Arbeit auf neue potenzielle Therapieansätze jenseits von Operation und konventionellen Antiparasitika hin. Strategien, die oxidativen Stress reduzieren oder gezielt das NLRP3-Inflammasom blockieren, könnten künftig dazu beitragen, Leberzellen zu schützen, das Fortschreiten der Erkrankung zu verlangsamen und das Komplikationsrisiko bei zystischer Echinokokkose zu senken.
Zitation: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Schlüsselwörter: zystische Echinokokkose, Leberentzündung, Pyroptose, reaktive Sauerstoffspezies, NLRP3-Inflammasom