Clear Sky Science · pt
ROS-NLRP3 participa na resposta de piroptose dos produtos excretores-secretórios de protósceros de Echinococcus granulosus em hepatócitos
Por que um parasita minúsculo importa para a saúde do fígado
A echinococose cística é uma doença causada por um pequeno verme platelminto que normalmente vive em animais como ovelhas e cães, mas que pode infectar pessoas acidentalmente. O parasita forma cistos cheios de líquido, mais frequentemente no fígado, que podem crescer silenciosamente por anos antes de causar dor, problemas digestivos ou complicações graves. Os médicos sabem que os hepatócitos são danificados durante essa infecção, mas não estava claro exatamente como a presença do parasita se traduz em morte celular. Este estudo examina de perto um tipo específico de morte celular inflamável, impulsionada por moléculas chamadas espécies reativas de oxigênio e por um sistema de alarme interno, para entender como as secreções do parasita podem ferir diretamente as células do fígado.
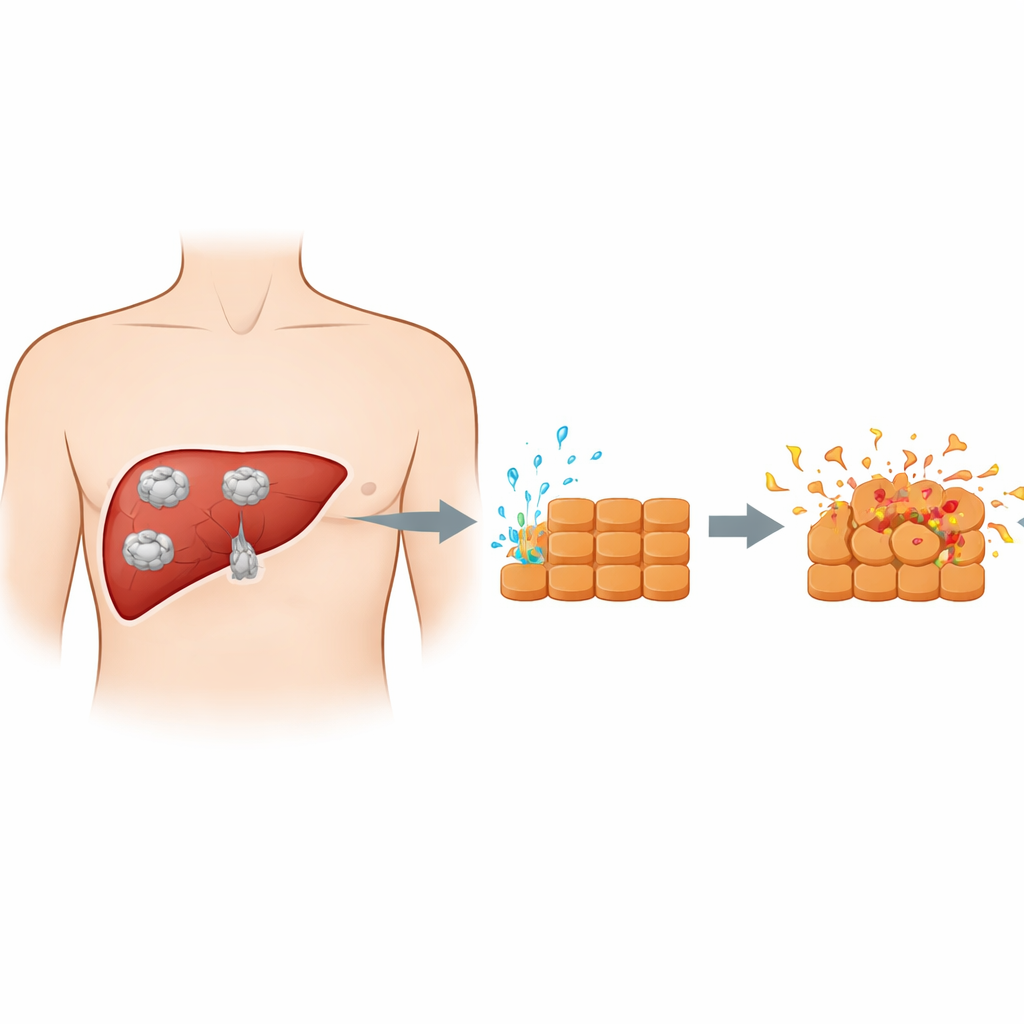
Como o parasita e as células do fígado se encontram
Quando pessoas ingerem ovos do parasita, as formas jovens viajam do intestino para o fígado e se desenvolvem em cistos. Esses cistos não são apenas bolhas passivas; o parasita em crescimento libera constantemente uma mistura de proteínas e outras substâncias no tecido ao redor. Trabalhos anteriores frequentemente usavam o fluido cístico completo, que também contém muitos componentes derivados do hospedeiro, dificultando ver o que o próprio parasita está fazendo. Neste estudo, os pesquisadores coletaram em vez disso secreções purificadas de um estágio inicial do parasita chamado protóscero. Em seguida, expuseram hepatócitos de camundongo cultivados em laboratório a esses produtos excretores–secretórios, criando um modelo mais limpo da conversa química direta entre parasita e células hepáticas conforme o cisto se expande.
Uma forma inflamável de morte celular dentro do fígado
A equipe concentrou-se na piroptose, uma forma de morte celular programada que difere do desligamento calmo e organizado observado na renovação celular normal. Na piroptose, as células incham, suas membranas ficam perfuradas e elas se rompem, derramando moléculas inflamatórias que recrutam células imunes e intensificam o dano tecidual. Esse processo é controlado por uma máquina molecular conhecida como inflamassoma, em particular uma versão centrada em uma proteína sensor chamada NLRP3. Quando os pesquisadores trataram os hepatócitos com as secreções do parasita, observaram sinais clássicos: redução da sobrevivência celular, aumento do vazamento de uma enzima celular (LDH) que indica dano de membrana, mais células mortas ao microscópio e níveis elevados de proteínas chave relacionadas à piroptose que promovem a formação de poros na membrana e a liberação de mediadores inflamatórios.
Desligando o alarme de perigo
Para testar se essa resposta destrutiva realmente dependia do sistema de alarme NLRP3, os pesquisadores usaram uma pequena molécula chamada MCC950 que bloqueia especificamente a atividade do NLRP3. Hepatócitos pré-tratados com esse bloqueador foram muito mais resistentes quando expostos às secreções do parasita. Eles mostraram melhor sobrevivência, menos células com membrana danificada, menor vazamento de LDH e produção reduzida de proteínas inflamatórias associadas à piroptose. Em imagens por fluorescência, a quantidade de NLRP3 visível dentro das células diminuiu acentuadamente. Juntos, esses resultados indicam que as secreções do parasita não simplesmente envenenam as células hepáticas de forma inespecífica; em vez disso, elas ativam ativamente o maquinário de autodestruição e inflamação baseado em NLRP3 das próprias células.
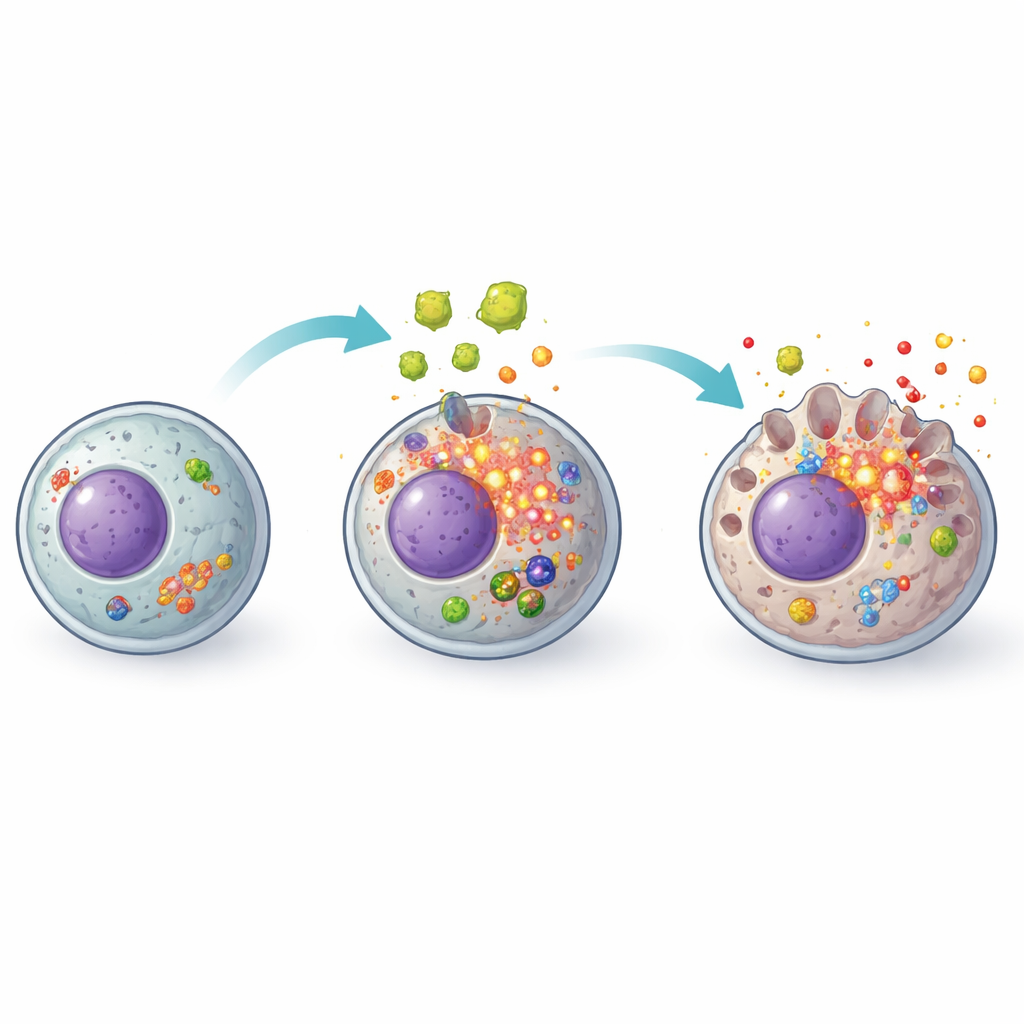
A faísca: estresse oxidativo dentro da célula
O estudo então investigou o que acende o gatilho desse sistema de alarme. Um suspeito principal foram as espécies reativas de oxigênio, subprodutos quimicamente reativos do metabolismo normal que se tornam prejudiciais quando se acumulam. As secreções do parasita fizeram com que os hepatócitos acumulassem altos níveis dessas moléculas reativas enquanto enfraqueciam suas defesas antioxidantes. Quando os pesquisadores adicionaram N-acetilcisteína, um antioxidante bem conhecido usado clinicamente para proteger o fígado em outros contextos, o quadro mudou. Os níveis de espécies reativas caíram, marcadores antioxidantes se recuperaram e a ativação do complexo NLRP3 e seu maquinário de piroptose a jusante foi fortemente atenuada. A sobrevivência celular melhorou e menos mediadores inflamatórios foram liberados, sugerindo que o estresse oxidativo é um gatilho crucial a montante dessa reação em cadeia.
O que isso significa para pessoas em risco
Em conjunto, os achados revelam uma história clara: proteínas secretadas por Echinococcus granulosus ao redor de seus cistos hepáticos podem sobrecarregar as células do fígado próximas com espécies reativas de oxigênio, que por sua vez ativam o inflamassoma NLRP3 e desencadeiam uma forma explosiva e inflamatória de morte celular. Esse mecanismo ajuda a explicar como um cisto parasitário aparentemente silencioso corrói gradualmente o tecido hepático e alimenta a inflamação crônica. Para os pacientes, o trabalho aponta para novos ângulos potenciais de tratamento além da cirurgia e dos antiparasitários padrão. Abordagens que reduzam o estresse oxidativo ou bloqueiem especificamente o inflamassoma NLRP3 podem, um dia, ajudar a proteger os hepatócitos, retardar a progressão da doença e reduzir o risco de complicações na echinococose cística.
Citação: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Palavras-chave: echinococose cística, inflamação hepática, piroptose, espécies reativas de oxigênio, inflamassoma NLRP3