Clear Sky Science · ru
ROS-NLRP3 участвует в ответе пироптоза на экскреторно‑секреторные продукты протосколексов Echinococcus granulosus в гепатоцитах
Почему крошечный паразит важен для здоровья печени
Кистозный эхинококкоз — это болезнь, вызываемая маленьким ленточным червёмом, который обычно обитает у животных, таких как овцы и собаки, но может случайно инфицировать человека. Паразит формирует заполненные жидкостью кисты, чаще всего в печени, которые могут годами тихо расти, прежде чем вызвать боль, проблемы с пищеварением или серьёзные осложнения. Врачи знают, что при этой инфекции повреждаются печёночные клетки, но точно не было ясно, каким образом присутствие паразита приводит к гибели клеток. В этом исследовании подробно изучается специфический «воспламеняющийся» тип гибели клеток, опосредованный реактивными видами кислорода и внутренней системой сигнализации, чтобы понять, как секреции паразита могут напрямую повреждать гепатоциты.
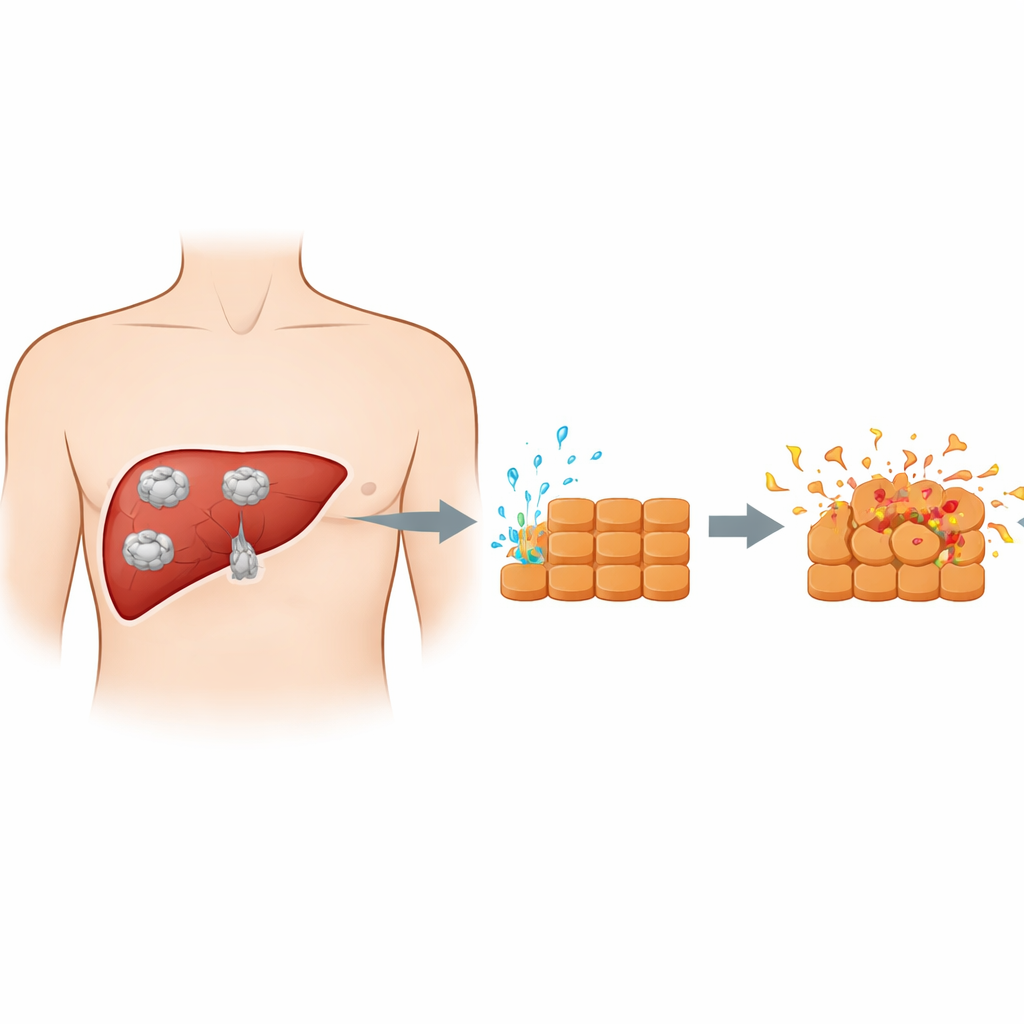
Как встречаются паразит и печёночные клетки
Когда человек проглатывает яйца паразита, молодые формы перемещаются из кишечника в печень и развиваются в кисты. Эти кисты не являются пассивными пузырями; растущий паразит постоянно выделяет смесь белков и других веществ в окружающие ткани. Ранее в исследованиях часто использовали весь содержимое кисты, которое также содержит множество компонентов хозяина, что затрудняло понимание собственно паразитарного вклада. В этом исследовании исследователи вместо этого собрали очищенные секреции ранней стадии паразита, называемой протосколексами. Затем они подвергли культивируемые в лаборатории печёночные клетки мыши воздействию этих экскреторно‑секреторных продуктов, создав более чистую модель прямого химического взаимодействия между паразитом и гепатоцитами по мере роста кисты.
Воспламеняющаяся форма гибели клеток в печени
Команда сосредоточилась на пироптозе — форме программируемой гибели клеток, отличной от спокойной, упорядоченной утилизации при нормальной клеточной регенерации. При пироптозе клетки набухают, их мембраны приобретают проницаемость, и они разрываются, выбрасывая воспалительные молекулы, которые привлекают иммунные клетки и усугубляют повреждение тканей. Этот процесс контролируется молекулярным комплексом, известным как инфламмасома, в частности вариантом с сенсором NLRP3. Когда исследователи обработали печёночные клетки секрециями паразита, они наблюдали классические признаки: снижение выживаемости клеток, повышенный выброс фермента LDH, указывающего на повреждение мембраны, увеличение числа погибших клеток в микроскопе и повышение уровней ключевых белков, связанных с пироптозом, ответственных за образование пор в мембране и высвобождение провоспалительных медиаторов.
Выключение сигнализации опасности
Чтобы проверить, действительно ли эта деструктивная реакция зависит от системы тревоги NLRP3, исследователи использовали малую молекулу MCC950, которая специфически блокирует активность NLRP3. Печёночные клетки, предварительно обработанные этим ингибитором, оказались значительно более устойчивыми при воздействии секреций паразита. Они демонстрировали лучшую выживаемость, меньше клеток с повреждёнными мембранами, снижение выброса LDH и уменьшение продукции воспалительных белков, связанных с пироптозом. При флуоресцентной визуализации количество видимого внутри клеток NLRP3 резко снизилось. В совокупности эти результаты указывают, что секреции паразита не просто неспецифически отравляют гепатоциты; напротив, они активно запускают в клетках собственные механизмы самоуничтожения и воспаления на основе NLRP3.
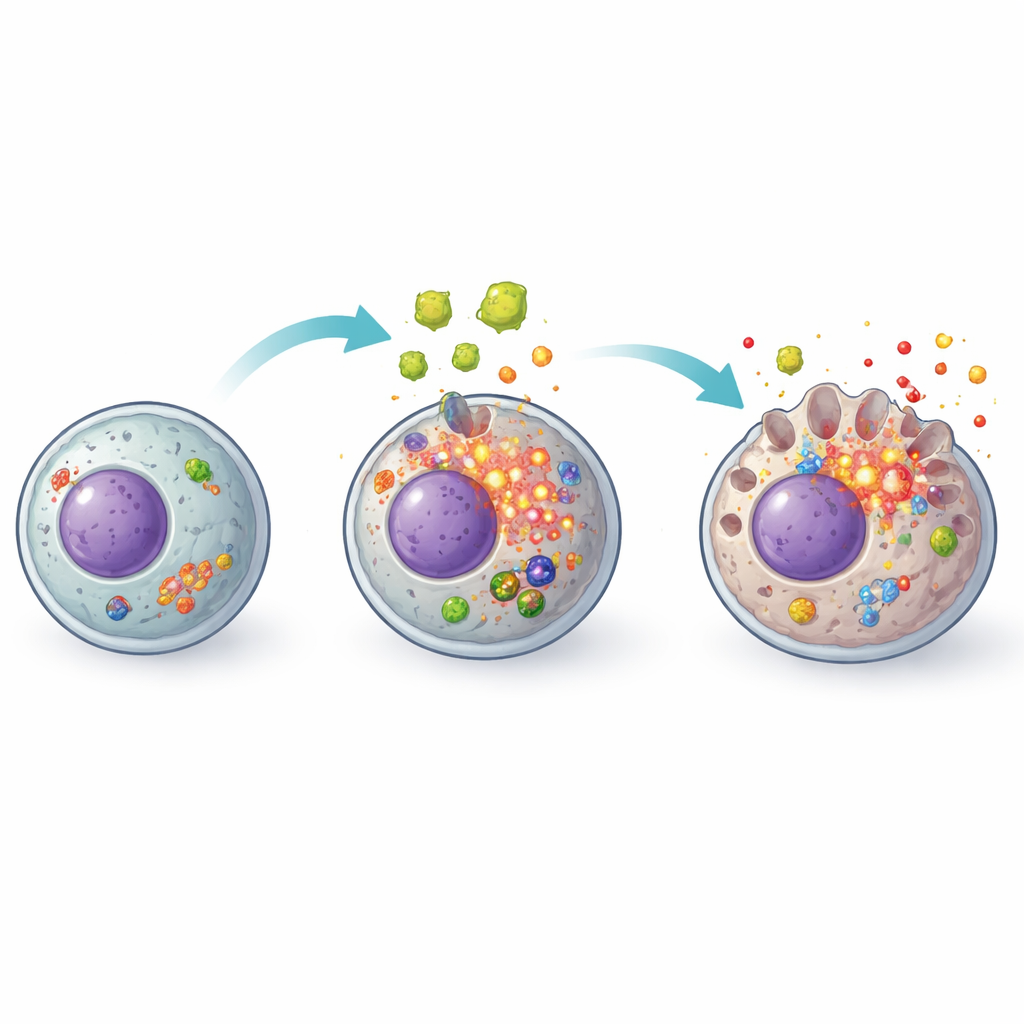
Искра: окислительный стресс внутри клетки
Далее исследование попыталось выяснить, что зажигает фитиль этой системы тревоги. Основным подозреваемым оказались реактивные виды кислорода — химически активные побочные продукты нормального метаболизма, которые становятся вредными при накоплении. Секреции паразита вызывали накопление в гепатоцитах высокого уровня этих реактивных молекул при ослаблении их антиоксидантных защит. Когда исследователи добавили N‑ацетилцистеин, известный антиоксидант, который клинически используется для защиты печени в других ситуациях, картина изменилась. Уровни реактивных видов кислорода снизились, маркеры антиоксидантной защиты восстановились, а активация комплекса NLRP3 и его нисходного пироптозного механизма была значительно ослаблена. Выживаемость клеток улучшилась, и выделение воспалительных молекул уменьшилось, что говорит о том, что окислительный стресс является ключевым верхнеуровневым триггером этой цепочки событий.
Что это значит для людей в группе риска
В совокупности результаты рисуют ясную картину: белки, выделяемые Echinococcus granulosus вокруг его печёночных кист, могут перегрузить соседние печёночные клетки реактивными видами кислорода, что, в свою очередь, активирует инфламмасому NLRP3 и приводит к взрывной, воспалительной форме гибели клеток. Этот механизм помогает объяснить, как кажущаяся тихой паразитарная киста постепенно разъедает печёночную ткань и подпитывает хроническое воспаление. Для пациентов работа указывает на новые потенциальные подходы к лечению помимо хирургии и стандартной антипаразитарной терапии. Подходы, снижающие окислительный стресс или специфически блокирующие инфламмасому NLRP3, могут в будущем помочь защищать печёночные клетки, замедлять прогрессирование заболевания и снижать риск осложнений при кистозном эхинококкозе.
Цитирование: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Ключевые слова: кистозный эхинококкоз, воспаление печени, пироптоз, реактивные виды кислорода, инфламмасома NLRP3