Clear Sky Science · es
ROS-NLRP3 participa en la respuesta de piroptosis a productos excretorios-secretorios de protóscilos de Echinococcus granulosus en hepatocitos
Por qué un parásito diminuto importa para la salud del hígado
La echinococosis quística es una enfermedad causada por un pequeño cestodo que suele vivir en animales como ovejas y perros, pero que puede infectar accidentalmente a las personas. El parásito forma quistes llenos de líquido, con mayor frecuencia en el hígado, que pueden crecer silenciosamente durante años antes de causar dolor, problemas digestivos o complicaciones graves. Los médicos saben que las células hepáticas se dañan durante esta infección, pero no estaba claro exactamente cómo la presencia del parásito se traduce en la muerte celular. Este estudio examina de cerca un tipo específico de muerte celular «inflamatoria», impulsada por moléculas llamadas especies reactivas de oxígeno y por un sistema de alarma interno, para entender cómo las secreciones del parásito pueden lesionar directamente a las células hepáticas.
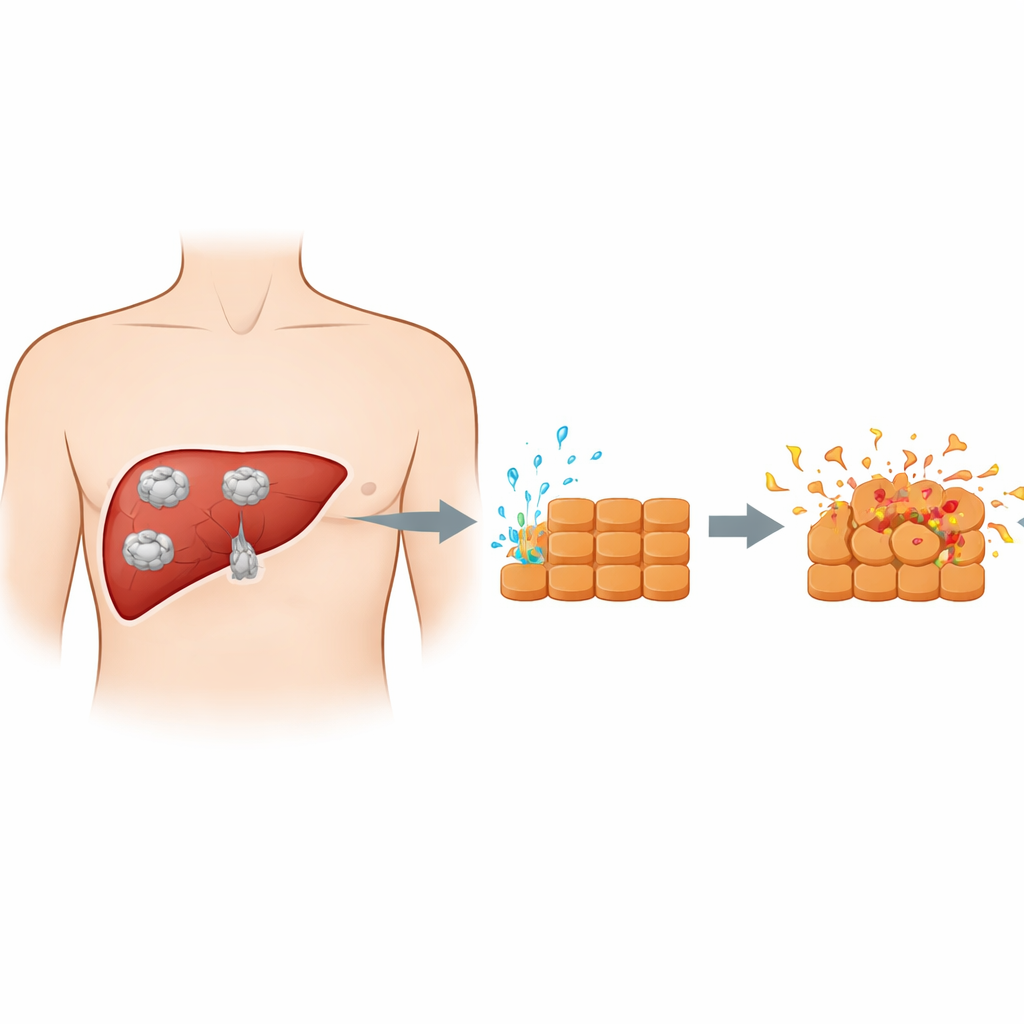
Cómo se encuentran el parásito y las células hepáticas
Cuando las personas ingieren huevos del parásito, las formas jóvenes viajan desde el intestino hasta el hígado y se desarrollan en quistes. Estos quistes no son simples burbujas pasivas; el parásito en crecimiento libera constantemente una mezcla de proteínas y otras sustancias en el tejido circundante. Trabajos anteriores a menudo emplearon el fluido quístico completo, que también contiene muchos componentes de origen del huésped, lo que dificulta distinguir lo que hace el propio parásito. En este estudio, los investigadores recogieron en su lugar secreciones purificadas de una etapa temprana del parásito llamada protóscilo. Luego expusieron a cultivos de células hepáticas de ratón a estos productos excretorios–secretorios, creando un modelo más limpio de la interacción química directa entre el parásito y las células hepáticas durante la expansión del quiste.
Una forma «ardiente» de muerte celular dentro del hígado
El equipo se centró en la piroptosis, una forma de muerte celular programada que difiere del apagado silencioso y ordenado observado en el recambio celular normal. En la piroptosis, las células se hinchan, sus membranas se perforan y estallan, liberando moléculas inflamatorias que atraen a células inmunitarias y agravan el daño tisular. Este proceso está controlado por una máquina molecular conocida como inflamasoma, en particular una variante centrada en una proteína sensor llamada NLRP3. Cuando los investigadores trataron las células hepáticas con las secreciones del parásito, observaron señales clásicas: menor supervivencia celular, aumento de la liberación de una enzima celular (LDH) que indica daño de membrana, más células muertas bajo el microscopio y niveles más altos de proteínas clave relacionadas con la piroptosis que impulsan la formación de poros en la membrana y la liberación de mediadores inflamatorios.
Apagando la alarma de peligro
Para comprobar si esta respuesta destructiva dependía realmente del sistema de alarma NLRP3, los investigadores utilizaron una pequeña molécula llamada MCC950 que bloquea específicamente la actividad de NLRP3. Las células hepáticas pretratadas con este inhibidor fueron mucho más resistentes al exponerse a las secreciones del parásito. Mostraron mejor supervivencia, menos células con membranas dañadas, menor liberación de LDH y reducción en la producción de proteínas inflamatorias asociadas con la piroptosis. En imágenes de fluorescencia, la cantidad de NLRP3 visible dentro de las células disminuyó notablemente. En conjunto, estos resultados indican que las secreciones del parásito no envenenan simplemente a las células hepáticas de forma inespecífica; en cambio, activan de forma activa el propio mecanismo de autodestrucción e inflamación de las células basado en NLRP3.
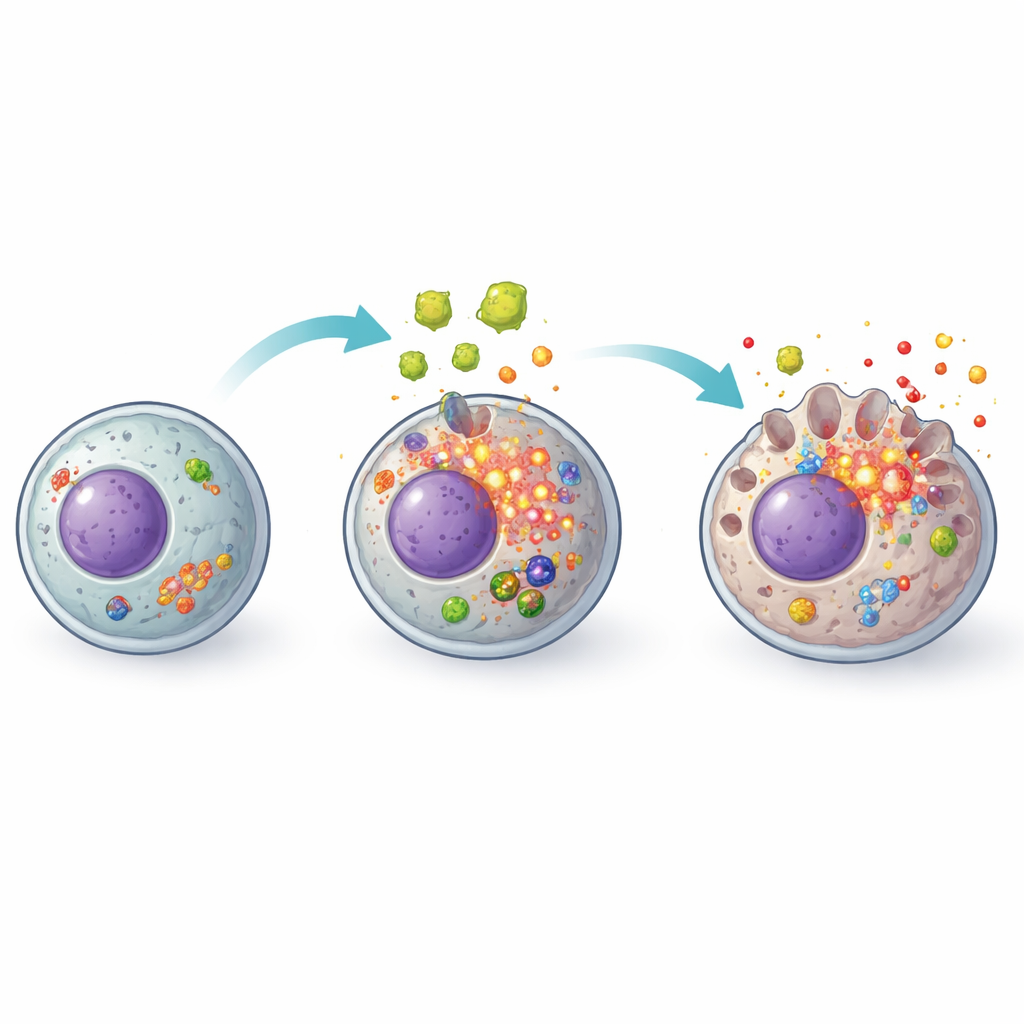
La chispa: estrés oxidativo dentro de la célula
El estudio investigó a continuación qué enciende la mecha de este sistema de alarma. Un sospechoso principal fueron las especies reactivas de oxígeno, subproductos químicamente reactivos del metabolismo normal que se vuelven dañinos cuando se acumulan. Las secreciones del parásito provocaron que las células hepáticas acumularan altos niveles de estas moléculas reactivas mientras debilitaban sus defensas antioxidantes. Cuando los investigadores añadieron N-acetilcisteína, un antioxidante bien conocido usado clínicamente para proteger el hígado en otros contextos, el panorama cambió. Los niveles de especies reactivas disminuyeron, los marcadores antioxidantes se recuperaron y la activación del complejo NLRP3 y su maquinaria de piroptosis aguas abajo se atenuó considerablemente. La supervivencia celular mejoró y se liberaron menos moléculas inflamatorias, lo que sugiere que el estrés oxidativo es un disparador upstream crucial para esta reacción en cadena.
Qué significa esto para las personas en riesgo
En conjunto, los hallazgos revelan una historia clara: las proteínas secretadas por Echinococcus granulosus alrededor de sus quistes hepáticos pueden sobrecargar a las células hepáticas cercanas con especies reactivas de oxígeno, que a su vez activan el inflamasoma NLRP3 y desencadenan una forma explosiva e inflamatoria de muerte celular. Este mecanismo ayuda a explicar cómo un quiste parasitario aparentemente silencioso erosiona gradualmente el tejido hepático y alimenta la inflamación crónica. Para los pacientes, el trabajo apunta a nuevos enfoques terapéuticos más allá de la cirugía y los antiparasitarios estándar. Estrategias que reduzcan el estrés oxidativo o bloqueen específicamente el inflamasoma NLRP3 podrían, algún día, ayudar a proteger las células hepáticas, ralentizar la progresión de la enfermedad y reducir el riesgo de complicaciones en la echinococosis quística.
Cita: Cao, J., Chen, J., Li, H. et al. ROS-NLRP3 participates in the pyroptosis response of excretory-secretory products from protoscoleces of Echinococcus granulosus in hepatocytes. Sci Rep 16, 14316 (2026). https://doi.org/10.1038/s41598-026-45127-7
Palabras clave: echinococosis quística, inflamación hepática, piroptosis, especies reactivas de oxígeno, inflamasoma NLRP3