Clear Sky Science · zh
一种新型Cu(II)-席夫碱配合物的合成、光谱学、表征、抗微生物、DNA相互作用、DFT与分子对接研究
为何一种以维生素为灵感的金属药物很重要
当今许多抗生素和抗癌药物正在丧失疗效,原因或是微生物产生了抗药性,或是副作用限制了患者可耐受的剂量。本研究探讨了一种创新思路:以叶酸——常见的维生素B9——为出发物构建一种新型铜基化合物,并检验该定制分子是否能杀伤细菌、结合DNA并抑制乳腺癌细胞的生长。通过将一种天然会靶向快速分裂细胞的营养分子与具有生物活性的金属结合,研究者旨在打造一种更智能、更具多功能性的治疗工具。
把常见维生素变成定制工具
研究团队以叶酸为起点,叶酸是细胞进行DNA合成与修复时使用的维生素,且常被癌细胞大量摄取。他们将叶酸化学连接到水杨醛(一种简单的芳香化合物),生成一种新的“席夫碱”配体——本质上是用于抓取金属离子的定制结构。当该配体遇到铜(II)离子时,形成了一个双铜核配合物:两个铜中心由有机骨架桥联。科学家制备了该铜—配体体系的常规(散装)与纳米尺寸两种形式,并用一系列标准实验技术仔细确认其结构,包括红外与可见光谱、核磁共振、质谱、磁学测量和热分析。他们还使用电子显微镜展示了纳米形态形成约15–27纳米的明确颗粒。 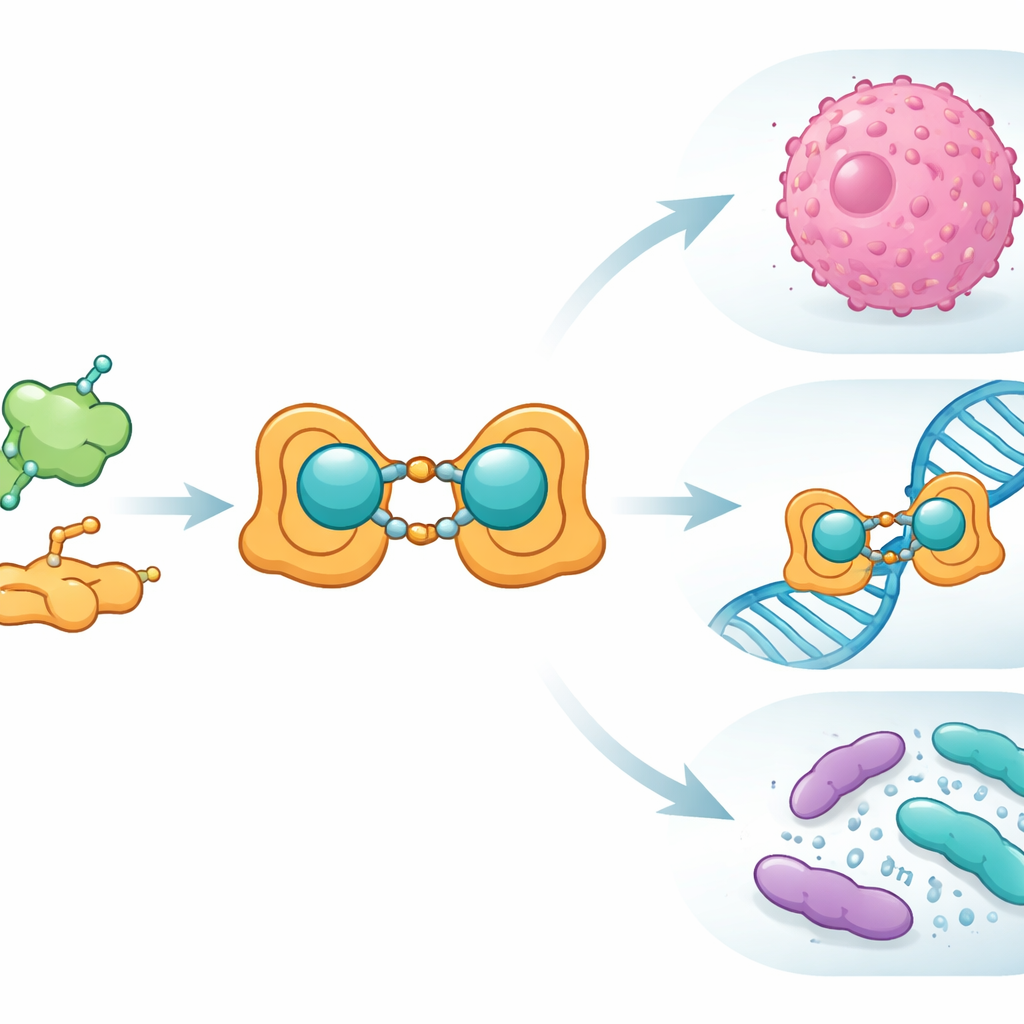
新化合物的行为表现
物理测量描绘出该化合物在形状与配位上的一致图景。红外信号的位移显示席夫碱配体的氮与氧原子都与铜形成了强烈配位,而磁学和电子自旋研究表明金属中心周围存在扭曲的四面体环境并且两个铜离子间有强相互作用。质谱与尺寸排阻色谱提示该配合物可组装成更高质量、类似聚合链的结构,由相邻单元间的相互作用稳定。为补充这些实验,研究者还采用现代量子化学计算,支持所提出的几何构型与电子结构。计算还表明,一旦铜被配位,化合物的前线轨道间能隙明显缩小,意味着体系更具反应性、易于电荷转移,并呈现增强的光学与电子响应性。
对细菌、DNA与癌细胞的检验
在掌握结构之后,团队考察了该铜配合物在生物环境中的表现。在针对常见细菌与真菌菌株的抗菌测试中,游离配体基本无效,但纳米尺寸的铜配合物对如大肠埃希菌(Escherichia coli)与金黄色葡萄球菌(Staphylococcus aureus)等致病细菌,以及白色念珠菌(Candida albicans)表现出明显的抑菌圈。随后,他们用三种方法研究化合物与DNA的相互作用:紫外吸收的变化、置换嵌入DNA碱基对间的荧光染料,以及溶液粘度测量。贯穿这些实验,铜配合物比单独配体与DNA结合得更强,并表现出类似经典插入式(intercalative)试剂的行为,细微地延长并解旋双螺旋。分子对接模拟(将分子“装入”来自细菌和真菌的蛋白结构中进行计算匹配)显示了有利的结合位点和负的相互作用能,再次证明铜配合物优于无金属的对应物。
对乳腺癌细胞的潜力
研究者随后用新分子处理人源MCF-7乳腺癌细胞。通过标准的细胞活力检测,他们发现游离的叶酸衍生配体活性相对较弱,需要较高浓度才能使细胞生长减半。相比之下,纳米级铜配合物在更低剂量下即可实现相同程度的生长抑制,活性接近参比化疗药顺铂(cisplatin),尽管整体仍稍逊一筹。叶酸片段可能有助于将配合物引导至过表达叶酸受体的癌细胞,而铜中心则可产生活性氧物种并扰乱DNA与关键酶。关于电荷分布与静电势的理论分析支持了这一图景,识别出特定的氮与氧原子作为向铜和生物靶点供电子的主要位点。 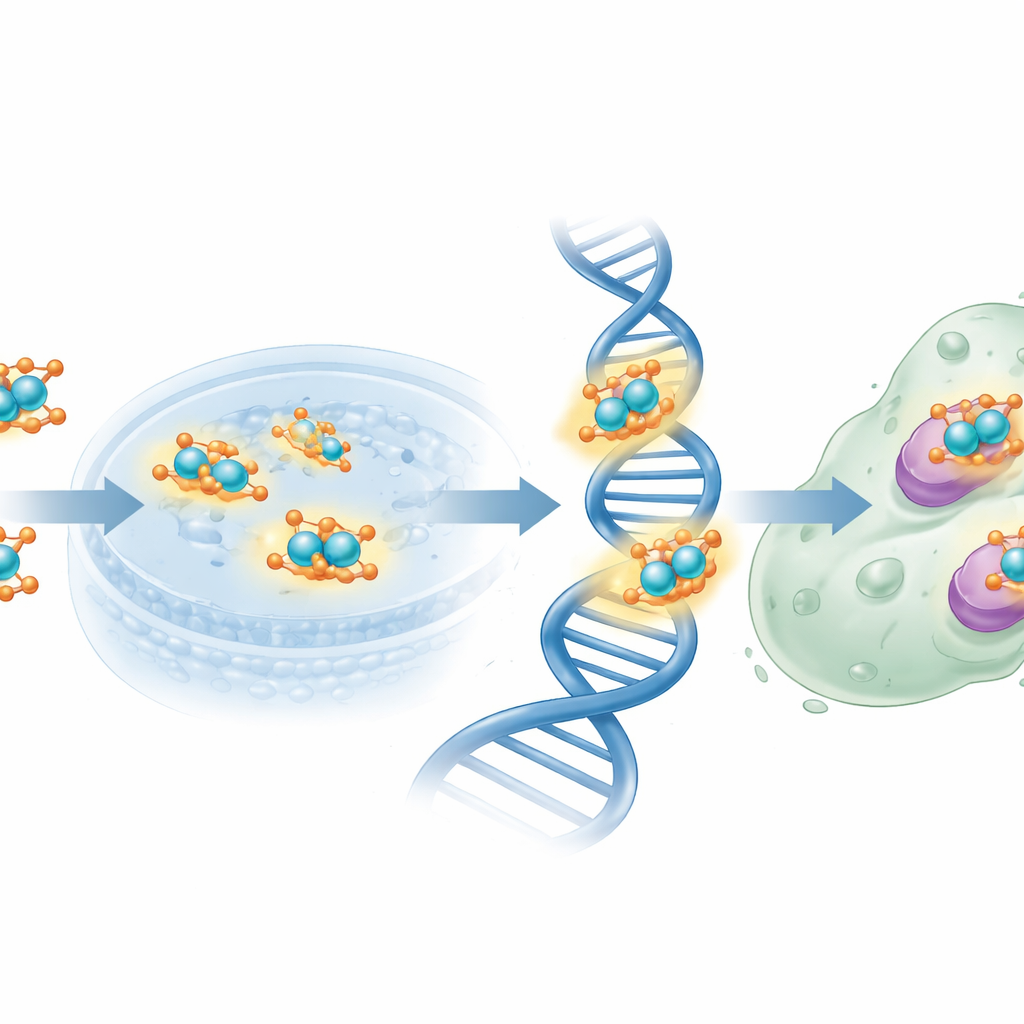
对未来药物的意义
通俗来说,这项研究表明,将维生素作为“地址标签”与活性金属中心巧妙结合,能把原本温和的有机分子转变为对抗微生物和癌细胞的多面手。基于叶酸的席夫碱本身活性有限,但当与铜配位并构造成双铜核的纳米级配合物后,它更容易插入DNA、干扰细菌的生理机制并减缓乳腺癌细胞的生长。虽然在此类化合物进入临床之前仍需大量工作——尤其是详尽的安全性与选择性研究——这些结果突出了一个有前景的设计策略:利用天然趋向快速生长细胞的营养分子作为金属配合物的支架,以在DNA与关键蛋白水平攻击疾病。
引用: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
关键词: 铜配合物, 叶酸, 席夫碱, DNA结合, 抗癌药物