Clear Sky Science · ar
تخليق، طيفية، توصيف، مضاد للميكروبات، تفاعل مع الحمض النووي، دراسات DFT والمحاكاة الجزيئية لمُركب جديد من نحاس(II)-شيف
لماذا يهم دواء معدني مستوحى من فيتامين
تفقد العديد من المضادات الحيوية وأدوية السرطان فاعليتها اليوم، إما لأن الميكروبات تطوّر مقاومة أو لأن الآثار الجانبية تقيد الجرعات التي يتحملها المرضى. تستكشف هذه الدراسة نهجاً مبتكراً: بناء مركب جديد قائم على النحاس مستمد من حمض الفوليك — فيتامين B9 المعروف — واختبار ما إذا كان هذا الجزيء المصمم يستطيع مهاجمة البكتيريا، والارتباط بالحمض النووي، وإبطاء نمو خلايا سرطان الثدي. بدمج مادة غذائية تسعى طبيعياً نحو الخلايا سريعة الانقسام مع معدن نشط بيولوجياً، يهدف الباحثون إلى إنشاء أداة علاجية أذكى وأكثر تنوعاً.
تحويل فيتامين شائع إلى أداة مصمَّمة
بدأ الفريق بحمض الفوليك، الفيتامين الذي تستخدمه خلاينا في بناء وإصلاح الحمض النووي والذي غالباً ما تحتفظ به خلايا السرطان. ربطوا حمض الفوليك كيميائياً بساليسيل ألدهيد، مركب عطري بسيط، لتكوين رابط جديد من نوع «قاعدة شيف» — في الأساس خطاف مُصمَّم لالتقاط أيون معدني. عندما التقى هذا الرابط بأيونات نحاس(II)، كوّن مُعقَّداً ثنائي النواة: مركبان نحاسيان مُرتبطان بالإطار العضوي. أعدّ العلماء هذا النظام النحاس–الرابط بأشكال عادية (جُملة) وبأحجام نانوية، وتحققوا من بنيته بدقة باستخدام مجموعة من تقنيات المختبر المعيارية، بما في ذلك طيف الأشعة تحت الحمراء والضوء المرئي، الرنين المغناطيسي النووي، مطياف الكتلة، القياسات المغناطيسية، والتحليل الحراري. كما استخدموا المجهر الإلكتروني لإظهار أن النسخة النانوية تُكوِّن جزيئات محددة جيداً بحجم يتراوح حوالي 15–27 نانومتر. 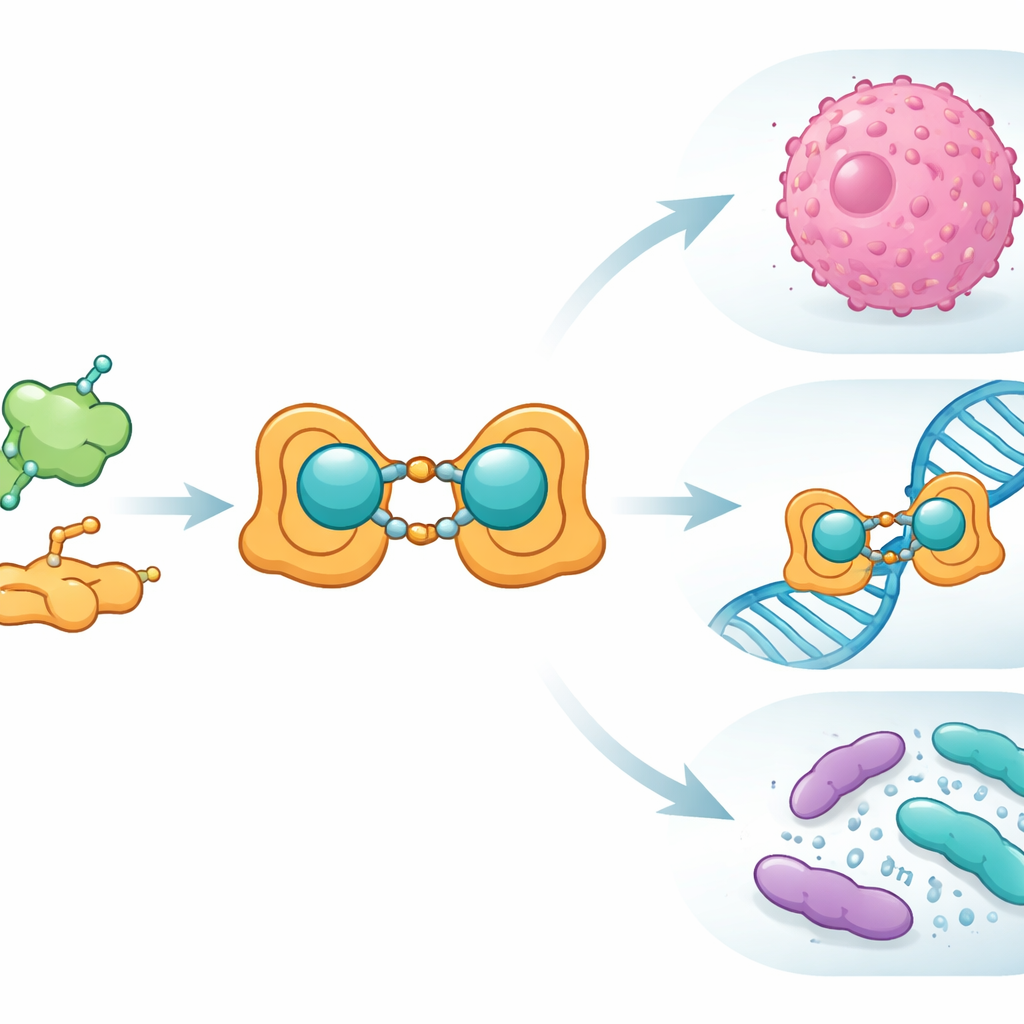
كيف يتصرف المركب الجديد
قدمت القياسات الفيزيائية صورة متسقة لشكل المركب وروابطه. كشفت تغيّرات في إشارات الأشعة تحت الحمراء أن كل من ذرات النيتروجين والأكسجين في رابط الشيف ترتبط بقوة بالنحاس، بينما أشارت الدراسات المغناطيسية ودراسات الدوران الإلكترولي إلى بيئة مشوهة رباعية الوجوه حول مراكز المعدن وتفاعل قوي بين أيوني النحاس. اقترحت مطيافية الكتلة وكروماتوغرافيا استبعاد الحجم أن المركب يمكن أن يتجمع إلى سلاسل شبيهة بالبوليمر ذات كتلة أعلى، مستقرة بتفاعلات بين الوحدات المتجاورة. لدعم هذه التجارب، لجأ الباحثون إلى حسابات كيمياء كمومية حديثة، والتي دعمت الهندسة المقترحة والبنية الإلكترونية. أظهرت الحسابات أيضاً أنه بوجود النحاس يرتبط تناقص كبير في فجوة الطاقة بين الأوربيتالات الحدية للمركب، ما يوحي بنظام أكثر تفاعلية وملاءمة لنقل الشحنة مع استجابة بصرية وإلكترونية معززة.
اختبار البكتيريا والحمض النووي وخلايا السرطان
مع البنية الموثقة، فحص الفريق كيف يتصرف المُعقَّد النحاسي الجديد في بيئات بيولوجية. في اختبارات مضادة للميكروبات ضد سلالات بكتيرية وفطرية شائعة، لم يُظهر الرابط الحر وحده فعالية تذكر، بينما أنتج المُعقَّد النانوي للنحاس مناطق واضحة من تثبيط النمو ضد بكتيريا مرتبطة بالأمراض مثل Escherichia coli وStaphylococcus aureus، وضد الخميرة Candida albicans. بعد ذلك، درسوا كيفية تفاعل المركبات مع الحمض النووي باستخدام ثلاث طرق: تغيّرات امتصاصية فوق بنفسجية، واستبدال صبغة فلورية تستقر بين قواعد الحمض النووي، وقياسات لزوجة المحلول. عبر هذه التجارب، ارتبط المُعقَّد النحاسي بالحمض النووي بقوة أكبر من الرابط وحده وتصرف بشكل مشابه للعوامل الكلاسيكية التي تدخل بين قواعد الحمض النووي، مطيلةً ومُرخيةً اللولب بشكل طفيف. أظهرت محاكاة الإرساء الجزيئي، التي تضع الجزيئات حسابياً داخل هياكل بروتينية من بكتيريا وفطريات، مناطق ربط ملائمة وطاقة تفاعل سالبة، مرة أخرى مع تفوق المُعقَّد النحاسي على نظيره الخالي من المعدن.
وعد ضد خلايا سرطان الثدي
ثم عرض الباحثون خلايا سرطان الثدي البشرية MCF-7 على المركبات الجديدة. باستخدام اختبار قياسي لبقاء الخلايا، وجدوا أن الرابط المستمد من الفولات الحر كان ضعيف الفاعلية نسبياً، حيث تطلّب تراكيز عالية لتقليل نمو الخلايا إلى النصف. بالمقابل، حقق المُعقَّد النانوي للنحاس نفس مستوى تثبيط النمو عند جرعات أقل بكثير، مقترباً من فعالية دواء العلاج الكيميائي القياسي سيسبلاتين، وإن كان لا يزال أقل قوة عامة. قد يساعد شظية حمض الفوليك في توجيه المركب نحو الخلايا السرطانية التي تُعبِّر مستقبلات الفولات بشكل مفرط، بينما يمكن لمراكز النحاس توليد أنواع تفاعلية وإحداث اضطراب في الحمض النووي والإنزيمات الأساسية. دعمت التحليلات النظرية لتوزيع الشحنة والجهد الكهربائي هذا التصور بتحديد ذرات نيتروجين وأكسجين معينة كمواقع أولية للتبرع بالإلكترونات للنحاس وللأهداف البيولوجية. 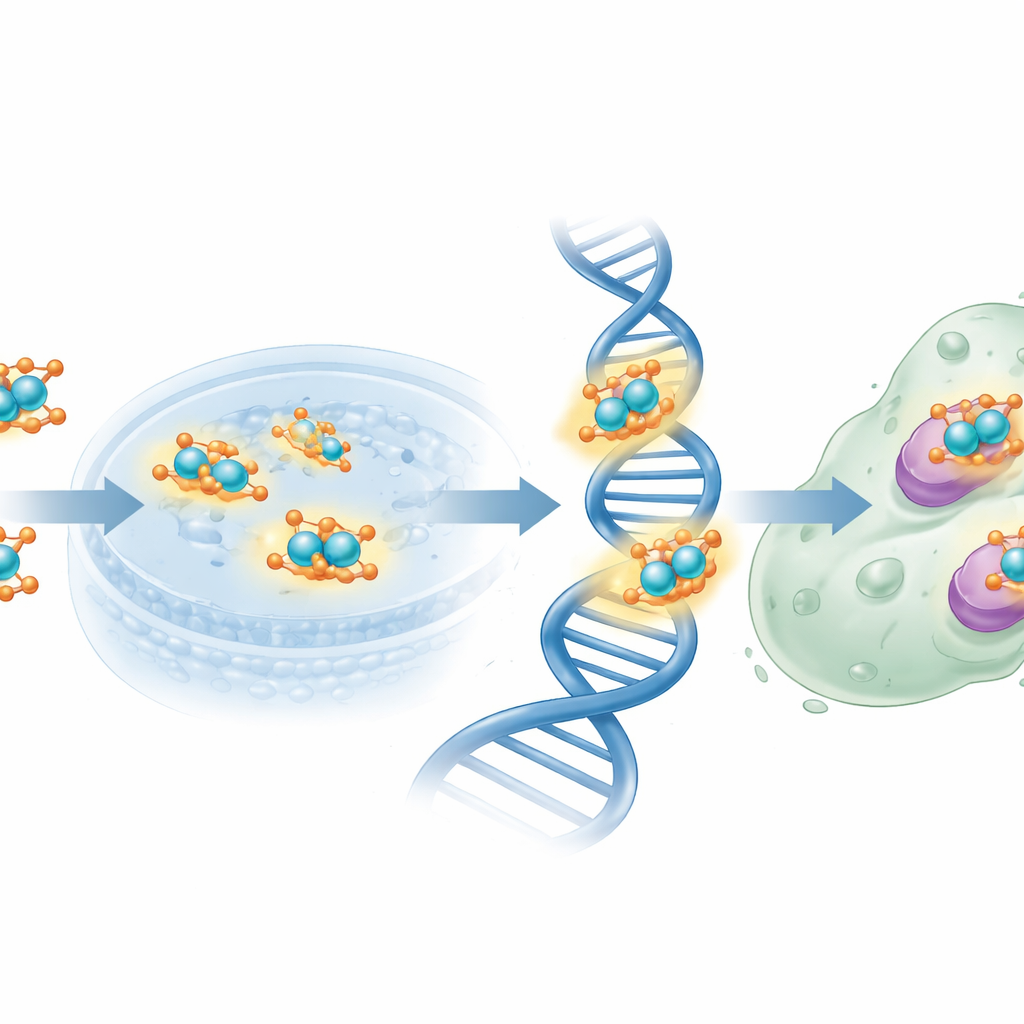
ماذا قد يعني هذا للأدوية المستقبلية
بعبارات مبسطة، تُظهر هذه الدراسة أن الجمع الذكي بين «عنوان» فيتامين وبين مركز معدني نشط يمكن أن يحول جزيئاً عضوياً ضعيف المفعول إلى سلاح متعدد الوظائف ضد الميكروبات وخلايا السرطان. قاعدة شيف القائمة على حمض الفوليك بمفردها نشاطها محدود، لكن عند اقترانها بالنحاس وتشكيلها كمُعقَّد ثنائي النواة على مقياس نانوي تصبح أكثر قدرة على التسلل إلى الحمض النووي، وتعطيل آليات البكتيريا، وإبطاء نمو خلايا سرطان الثدي. وبينما لا يزال أمام هذا النوع من المركبات الكثير ليُنجَز قبل أن يصل إلى العيادة — خصوصاً دراسات سلامة وانتقائية مفصّلة — تبرز النتائج استراتيجية تصميم واعدة: استخدام المغذيات التي تتجه طبيعياً إلى الخلايا سريعة النمو كقوالب لمُعقّدات معدنية تستطيع مهاجمة المرض على مستوى الحمض النووي والبروتينات الأساسية.
الاستشهاد: Mahmoud, E.G., Ismail, E.H., Abdel Aziz, A.A. et al. Synthesis, spectroscopic, characterization, antimicrobial, DNA interaction, DFT and molecular docking studies of a new Cu(II)-Schiff base complex. Sci Rep 16, 13636 (2026). https://doi.org/10.1038/s41598-026-44842-5
الكلمات المفتاحية: مُعقّدات النحاس, حمض الفوليك, قاعدة شيف, ارتباط بالحمض النووي, عوامل مضادة للسرطان